Konvertering af pKa til Ka:En hurtig vejledning for kemikere
afotostock/Shutterstock
Forstå dissociationskonstanten (Ka)
I Brønsted–Lowry-rammen donerer en syre en proton til et opløsningsmiddel, hvorved der dannes en konjugeret base og en konjugeret syre. Når vand er opløsningsmidlet, kan ligevægten skrives som:
HA + H2 O <=> H3 O + + A -
Syrens styrke kvantificeres af dissociationskonstanten Ka, defineret som forholdet mellem koncentrationerne af produkterne og reaktanterne (eksklusive vand i vandige opløsninger):
Ka =[H3 O + ][A - ]/[HA]
En større Ka indikerer, at reaktionen favoriserer den dissocierede form, hvilket betyder en stærkere syre. Omvendt afspejler en lille Ka en svagere syre.
Hvorfor pKa er mere praktisk
Ka-værdier spænder over mange størrelsesordener – fra så høje som 10 7 for stærke syrer til så lavt som 10 -12 for svage syrer. For at styre dette interval bruger kemikere den negative base-10-logaritme af Ka, kaldet pKa:
pKa =-log10 (Ka)
En stærk syre med Ka =10 7 har pKa =-7, mens en svag syre med Ka =10 -12 har pKa =12. Det omvendte forhold betyder, at en lavere pKa svarer til en stærkere syre.
Konvertering af pKa tilbage til Ka
Når du støder på en pKa-værdi i en referencetabel, men har brug for Ka til beregninger, skal du blot vende logaritmen:
Ka =10 -pKa
For heltals pKa-værdier (f.eks. -7) er konverteringen ligetil. For brøkværdier (f.eks. 7,5) kan du bruge en videnskabelig lommeregner eller slå resultatet op i en tabel. Husk, at operationen involverer basis-10-eksponentiering, ikke naturlige logaritmer.
Ved at bruge denne metode kan du hurtigt få Ka fra enhver rapporteret pKa, hvilket letter nøjagtige syre-base-beregninger.
 Varme artikler
Varme artikler
-
 Effektiv faktoropdeling:En trin-for-trin guideAf bidragyder • Opdateret 30. august 2022 Faktorer, angivet med udråbstegn, er et grundlæggende begreb i kombinatorik og sandsynlighed. De repræsenterer produktet af alle positive heltal op til et gi
Effektiv faktoropdeling:En trin-for-trin guideAf bidragyder • Opdateret 30. august 2022 Faktorer, angivet med udråbstegn, er et grundlæggende begreb i kombinatorik og sandsynlighed. De repræsenterer produktet af alle positive heltal op til et gi -
 Sådan konverteres Hertz til Motor RPM hurtigt og præcistAf Kim Lewis Opdateret:27. februar 2025 kl. 15.30 EST Filippo Carlot/Shutterstock Frekvens beskriver oscillerende bevægelser, såsom vibrationer fra en motor eller bølgen af et signal. Det måles i h
Sådan konverteres Hertz til Motor RPM hurtigt og præcistAf Kim Lewis Opdateret:27. februar 2025 kl. 15.30 EST Filippo Carlot/Shutterstock Frekvens beskriver oscillerende bevægelser, såsom vibrationer fra en motor eller bølgen af et signal. Det måles i h -
 Konverter grader til meter:En praktisk guide til jordafstandsberegningerFoto af Cathy Scola/Getty Images Selvom Jorden er lidt fladtrykt ved polerne, opfører den sig stort set som en kugle. På en sfærisk overflade kan afstanden mellem to punkter udtrykkes både som en vin
Konverter grader til meter:En praktisk guide til jordafstandsberegningerFoto af Cathy Scola/Getty Images Selvom Jorden er lidt fladtrykt ved polerne, opfører den sig stort set som en kugle. På en sfærisk overflade kan afstanden mellem to punkter udtrykkes både som en vin -
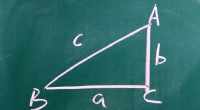 Sådan bestemmes den ukendte vinkel i enhver trekantZorabc/Shutterstock Trekantligninger er en fast bestanddel af geometri- og algebraforløb, og symbolet X bruges oftest til at betegne en ukendt vinkel. Ved at analysere markeringerne på trekanten og a
Sådan bestemmes den ukendte vinkel i enhver trekantZorabc/Shutterstock Trekantligninger er en fast bestanddel af geometri- og algebraforløb, og symbolet X bruges oftest til at betegne en ukendt vinkel. Ved at analysere markeringerne på trekanten og a
- Forskning viser, at gensplejsede vesikler bedre målretter mod kræftceller
- Hvornår blev teorien om relativitet først foreslået det?
- Forskere skaber miniature vidvinkelkameraer med flade metalenses
- Hvordan kan skrivende ligning for alfa-henfald af actinium-225?
- Er der flere stjerner end vores sol i Galaxy?
- Nøgletræk ved eukaryotisk mRNA:Afdækning og polyadenylering forklaret


