DNA nanorobotter finder og mærker cellulære mål
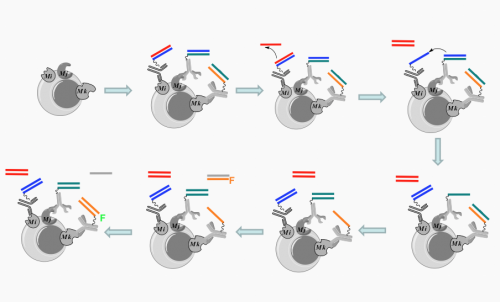
Denne grafik viser en molekylær robot (automat) i aktion. For at mærke celler (grå cirkel), der viser Mi, Mj, og Mk-receptorer, fem forskellige komponenter i en molekylær robot er indsat. Hver af de første tre komponenter består af DNA og et antistof; et antistof binder til hver receptor, bringe dets DNA (repræsenteret ved de farvede linjer) tæt sammen på cellen. Den fjerde DNA-komponent, repræsenteret ved den enkelte røde linje, starter derefter en kædereaktion ved at trække den røde DNA-streng væk fra det første antistof. Det får den blå DNA-streng til at ændre position, efterfulgt af den grønne DNA-streng. I det sidste trin, det sidste antistof trækker en fluorescerende DNA-streng (mærket F) fra den femte komponent, fuldføre robottens handling. Kredit:Milan Stojanovic, Ph.D./Columbia University Medical Center
Forskere ved Columbia University Medical Center, arbejder med deres samarbejdspartnere på Hospitalet for Specialkirurgi, har skabt en flåde af molekylære "robotter", der kan huse på specifikke menneskelige celler og mærke dem til medicinbehandling eller ødelæggelse.
Nanorobotterne - en samling af DNA-molekyler, nogle bundet til antistoffer - blev designet til at søge et specifikt sæt af menneskelige blodceller og fastgøre et fluorescerende mærke til celleoverfladerne. Detaljer om systemet blev offentliggjort 28. juli, 2013, i online-udgaven af Natur nanoteknologi .
"Dette åbner muligheden for at bruge sådanne molekyler til at målrette, behandle, eller dræbe specifikke celler uden at påvirke lignende sunde celler, " sagde undersøgelsens seniorforsker, Milan Stojanovic, PhD, lektor i medicin og i biomedicinsk teknik ved Columbia University Medical Center. "I vores eksperiment, vi mærkede cellerne med en fluorescerende markør; men vi kunne erstatte det med et lægemiddel eller med et toksin for at dræbe cellen."
Selvom andre DNA -nanorobotter er designet til at levere medicin til celler, Fordelen ved Stojanovics flåde er dens evne til at skelne cellepopulationer, der ikke deler et enkelt særpræg.
celler, herunder kræftceller, sjældent besidder en enkelt, eksklusiv funktion, der adskiller dem fra alle andre celler. Dette gør det svært at designe lægemidler uden bivirkninger. Lægemidler kan designes til at målrette kræftceller med en specifik receptor, men raske celler med samme receptor vil også blive målrettet.
Den eneste måde at målrette celler mere præcist på er at identificere celler baseret på en samling af funktioner. "Hvis vi ser efter tilstedeværelsen af fem, seks, eller flere proteiner på celleoverfladen, vi kan være mere selektive, " sagde Dr. Stojanovic. Store cellesorteringsmaskiner har evnen til at identificere celler baseret på flere proteiner, men indtil nu, molekylær terapi har ikke haft den evne.
Hvordan det virker
I stedet for at bygge et enkelt komplekst molekyle for at identificere flere træk ved en celleoverflade, Dr. Stojanovic og hans kolleger i Columbia brugte en anden, og potentielt nemmere, tilgang baseret på flere simple molekyler, som tilsammen danner en robot (eller automat, som forfatterne foretrækker at kalde det).
For at identificere en celle, der besidder tre specifikke overfladeproteiner, Dr. Stojanovic konstruerede først tre forskellige komponenter til molekylære robotter. Hver komponent bestod af et stykke dobbeltstrenget DNA bundet til et antistof specifikt for et af overfladeproteinerne. Når disse komponenter føjes til en samling af celler, robottens antistofdele binder til deres respektive proteiner (i figuren, CD45, CD3, og CD8) og arbejde sammen.
På celler, hvor alle tre komponenter er knyttet, en robot er funktionel, og en fjerde komponent (mærket 0 nedenfor) starter en kædereaktion blandt DNA-strengene. Hver komponent bytter en DNA-streng med en anden, indtil afslutningen af byttet, når det sidste antistof opnår en DNA-streng, der er fluorescensmærket.
Ved slutningen af kædereaktionen - som tager mindre end 15 minutter i en prøve af humant blod - er kun celler med de tre overfladeproteiner mærket med den fluorescerende markør.
"Vi har demonstreret vores koncept med blodceller, fordi deres overfladeproteiner er velkendte, men i princippet kunne vores molekyler udplaceres hvor som helst i kroppen, " sagde Dr. Stojanovic. Derudover, systemet kan udvides til at identificere fire, fem, eller endnu flere overfladeproteiner.
Nu skal forskerne vise, at deres molekylære robotter arbejder i et levende dyr; næste trin vil være eksperimenter med mus.
 Varme artikler
Varme artikler
-
 Nano -klaverer vuggevise kan betyde lagergennembrudNano klaver koncept:Arrays af guld, søjleunderstøttet bowtie nanoantennas (nederst til venstre) kan bruges til at optage forskellige musikalske noter, som vist i de eksperimentelt opnåede mørkfeltmikr
Nano -klaverer vuggevise kan betyde lagergennembrudNano klaver koncept:Arrays af guld, søjleunderstøttet bowtie nanoantennas (nederst til venstre) kan bruges til at optage forskellige musikalske noter, som vist i de eksperimentelt opnåede mørkfeltmikr -
 Carbon nanorør bedst til 3D -elektronikTo chips har sammenkoblinger, der er fyldt med tusindvis af carbon nanorør. Chipsene bindes derefter med klæbemiddel, så carbon -nanorørene bringes direkte i kontakt. En forbindelse ved hjælp af to så
Carbon nanorør bedst til 3D -elektronikTo chips har sammenkoblinger, der er fyldt med tusindvis af carbon nanorør. Chipsene bindes derefter med klæbemiddel, så carbon -nanorørene bringes direkte i kontakt. En forbindelse ved hjælp af to så -
 Magnetiske nanopartikelkæder tilbyder ny teknik til styring af bløde robotterEn selektiv aktivering af sidearmene på en blød robot i et vandret ensartet magnetfelt. Kredit:Sumeet Mishra, North Carolina State University Forskere fra North Carolina State University har udvik
Magnetiske nanopartikelkæder tilbyder ny teknik til styring af bløde robotterEn selektiv aktivering af sidearmene på en blød robot i et vandret ensartet magnetfelt. Kredit:Sumeet Mishra, North Carolina State University Forskere fra North Carolina State University har udvik -
 Videnskab giver ny måde at kigge ind i porerDe veje, fluorescerende partikler tager, når de diffunderer gennem en porøs nanoskala struktur, afslører arrangementet af porerne gennem en teknik udviklet af forskere ved Rice University. Kredit:Land
Videnskab giver ny måde at kigge ind i porerDe veje, fluorescerende partikler tager, når de diffunderer gennem en porøs nanoskala struktur, afslører arrangementet af porerne gennem en teknik udviklet af forskere ved Rice University. Kredit:Land
- Gør navngivning og shaming af gymnasier med store undervisningsstigninger en forskel?
- Indonesien Sinabung -vulkan frigiver tårnhøj askesøjle
- Var nu stressede? Historien viser dens ældste følelse
- Hvilke elementer kan kobolt kombinere med?
- Forskere rapporterer om en ny måde at producere kurvet elektronik på
- Amazon køber eero:Hvad betyder det for prisen på Wi-Fi-routere?


