Forskere bruger lys udsendt fra nanopartikler til at kontrollere biologiske processer

De nye nanopartikler fluorescerer enten røde eller grønne afhængigt af energien fra infrarødt lys, der bruges til at excitere dem. Kredit:National University of Singapore
Den biologiske teknik 'optogenetics' bruger lys til at kontrollere celler i levende væv, der er blevet genetisk modificeret til at være lysfølsomme. Imidlertid, der er begrænset kontrol over processer som denne, da lyset kan aktivere flere gener på én gang, og dybt gennemtrængende lys er ofte nødvendigt for at nå generne i levende væv.
Nu, forskere fra NUS har udviklet en metode til at give mere kontrol til denne proces, ved at bruge specialdesignede nanopartikler og nanoclusters (kaldet 'superballs'). Disse nanopartikler og superbolde kan udsende forskellige farver af lys, når de exciteres af lasere ved forskellige bølgelængder. Disse forskellige farver af lys kan derefter bruges til at udløse specifikke biologiske processer.
For at aktivere lysfølsomme gener, holdet ledet af professor Zhang Yong fra NUS Biomedical Engineering brugte nanopartiklerne og superboldene til at 'opkonvertere' nær-infrarødt (NIR) lys til højere energier af synligt lys. Da NIR-lys er dybt gennemtrængende, denne tilgang kan bruges til mange dybtliggende vævsbehandlinger.
Nanopartikler til at kontrollere hjerterytmen
Prof Zhang og hans team opfandt nye nanopartikler, der udsender enten rødt eller grønt lys, afhængig af bølgelængden af den NIR-stråling, der bruges til at excitere dem. Nanopartiklerne udstråler rødt lys, når de exciteres af en laserstråle med en bølgelængde på 980 nanometer, og grønt lys, når laserstrålens bølgelængde er reduceret til 808 nanometer.
Ud over at være to forskellige farver, lyset, der udsendes fra disse nanopartikler, kan bruges til tovejsaktivering. Dette er forskelligt fra nuværende optogenetiske terapier, der bruger nanopartikler, som kun kan aktiveres på en monodirektional måde. "Som sådan, vi kan indviklet manipulere en biologisk proces, eller nogle trin i processen, i forskellige retninger eller programmatisk, " forklarede prof Zhang.
Forskerne viste, at det var muligt at bruge disse partikler til at kontrollere slaghastigheden i modificerede hjerte-muskelceller. Ved optisk at styre to lysaktiverede kanaler kendt som Jaws og VChR1 i samme celle, de var i stand til at ændre hjerteslagets hastighed. Det røde lys bremsede pulsen, og det grønne lys fremskyndede det.
Disse nanopartikler består af en indre kerne, som er rig på erbium, omgivet af lag af ytterbium og neodym-doterede materialer. "For at generere sådanne ortogonale fluorescensemissioner, Vi skal normalt dope flere lanthanidioner ind i nanokrystallerne. I vores undersøgelse, dette opnås ved kun at bruge én ion." Denne innovation fra forskerne sikrer, at de ortogonale emissioner alle kommer fra erbium-ioner.
Med hensyn til dette materielle gennembrud og applikationsinnovation, Prof Zhang sagde, "Denne demonstration giver et stort skridt fremad mod programmerbar multi-directional pathway control, og tilbyder også spændende muligheder for anvendelser i mange andre synergistisk interaktive biologiske processer såsom diagnostik og terapier."
Resultaterne af denne undersøgelse blev offentliggjort i tidsskriftet Naturkommunikation den 27. september 2019 og blev rapporteret som et forskningshøjdepunkt den 4. oktober 2019.
Superbolde til at aktivere kræftmedicin
Ud over de nye nanopartikler, Prof Zhang og hans team syntetiserede for nylig klynger af to forskellige nanopartikler, som de kaldte 'superbolde'. På samme måde som de nye nanopartikler, disse superbolde udsender forskelligt farvet lys, når de exciteres med forskellige bølgelængder af NIR-stråling. De udstråler rødt lys, når de exciteres af en laserstråle med en bølgelængde på 980 nanometer, og UV/blåt lys, når laserstrålens bølgelængde er reduceret til 808 nanometer.
Disse nye superbolde blev derefter brugt til at forbedre en fotodynamisk kræftbehandlingsprocedure.
Da superboldene var energisk begejstrede for at udstråle rødt lys, de kunne komme ind i en celle. Næste, de var begejstrede for at udstråle UV/blåt lys for at øge cellens følsomhed over for reaktive oxygenarter. Endelig, de var begejstrede for at udstråle rødt lys igen for at aktivere lysfølsomme lægemidler til at producere reaktive oxygenarter. Disse reaktive oxygenarter kan derefter inducere drab af tumorceller.
Med dette forskningsgennembrud, NUS-forskerne har udviklet en enkel, brugervenlig metode til at syntetisere disse superbolde. Formen, størrelse og endda excitations-/emissionsbølgelængderne for superboldene kan ændres afhængigt af den nødvendige applikation.
Resultaterne fra denne undersøgelse blev offentliggjort i Naturkommunikation den 8. oktober 2019.
Næste skridt
Anvendelsen af disse nanopartikler og superbolde er talrige. "Dette vil være af interesse for biologer og klinikere inden for forskellige områder, især dem, der arbejder med fototerapi, herunder fotodynamisk terapi, fototermisk terapi, lysstyret lægemiddel/genlevering, og optogenetik, " sagde prof Zhang
Til de næste forskningsfaser, Prof Zhang forklarede, "Ultimativt, Formålet med dette projekt er at bruge trådløs elektronik sammen med nanopartikler til forbedrede fotodynamiske terapier, som kan behandle store tumorer i dybe væv." forskerne vil fortsætte med at udvikle nye materialer og opfinde innovative applikationer på dette område.
 Varme artikler
Varme artikler
-
 Anvendelse af nanoteknologi i kosmetik og lægemidlerProfessor Dr. Mahiran Basri. Kredit:Universiti Putra Malaysia Brugen af olier og fedtstoffer er blevet succesfuldt diversificeret, resulterer i en innovation formuleret gennem nanoteknologi, der
Anvendelse af nanoteknologi i kosmetik og lægemidlerProfessor Dr. Mahiran Basri. Kredit:Universiti Putra Malaysia Brugen af olier og fedtstoffer er blevet succesfuldt diversificeret, resulterer i en innovation formuleret gennem nanoteknologi, der -
 Ny DNA-origami-motor slår hastighedsrekord for nanomaskinerSeksten DNA-strenge, stablet fire gange fire, danner DNA-motorens stråleformede chassis (i gråt). Bits af DNA (i grønt) stikker ud fra chassiset som små fødder. Motoren er drevet af RNA lagt på et spo
Ny DNA-origami-motor slår hastighedsrekord for nanomaskinerSeksten DNA-strenge, stablet fire gange fire, danner DNA-motorens stråleformede chassis (i gråt). Bits af DNA (i grønt) stikker ud fra chassiset som små fødder. Motoren er drevet af RNA lagt på et spo -
 Magneter overtrumfer metallisk:Magnetiske felter kan blokere ledningsevnen for kulstofnanorørRice University professor Junichiro Kono, stående, og kandidatstuderende Thomas Searles satte sig for at studere interaktioner mellem magnetiske felter og elektrisk ladede partikler og fandt ud af, at
Magneter overtrumfer metallisk:Magnetiske felter kan blokere ledningsevnen for kulstofnanorørRice University professor Junichiro Kono, stående, og kandidatstuderende Thomas Searles satte sig for at studere interaktioner mellem magnetiske felter og elektrisk ladede partikler og fandt ud af, at -
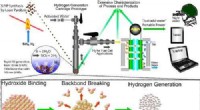 Nanosilicon splitter hurtigt vand uden lys, varme, eller elektricitetIllustration af den tværfaglige tilgang til fremstilling af brint gennem siliciumoxidation. Fremgangsmåden indebærer syntetisering af siliciumnanopartikler, silicium-vand-reaktionen, der genererer hyd
Nanosilicon splitter hurtigt vand uden lys, varme, eller elektricitetIllustration af den tværfaglige tilgang til fremstilling af brint gennem siliciumoxidation. Fremgangsmåden indebærer syntetisering af siliciumnanopartikler, silicium-vand-reaktionen, der genererer hyd
- Sådan halveres miljøpåvirkningen af din julemiddag
- Forbedret repræsentation af solvariabilitet i klimamodeller (opdatering)
- 80 % af de voksne i USA har haft alvorlige problemer, økonomisk usikkerhed under pandemi
- USA er stadig stagneret med hensyn til sårbarhed og parathed til klimaændringer, nye data viser
- Singing for science:Hvordan kunsten kan hjælpe elever, der kæmper mest
- Store molekyler fra kostfibre kan ændre tarmmiljøet gennem fysiske kræfter


