Direkte nanopartikler direkte til tumorer

Kredit:CC0 Public Domain
Moderne kræftbehandlinger har til formål at angribe tumorceller, mens de sparer sundt væv. Et tværfagligt team af forskere ved Helmholtz-Zentrum Dresden-Rossendorf (HZDR) og FU Berlin har gjort vigtige fremskridt på dette område:forskerne har produceret små nanopartikler, der er designet til specifikt at målrette kræftceller. De kan navigere direkte til tumorcellerne og visualisere dem ved hjælp af avancerede billeddannelsesteknikker. Både i petriskåle og dyremodeller, forskerne var i stand til effektivt at guide nanopartiklerne til kræftcellerne. Det næste trin er at kombinere den nye teknik med terapeutiske tilgange.
HZDR -forskerne starter med små, biokompatible nanopartikler fremstillet af såkaldte dendritiske polyglyceroler, der fungerer som bærermolekyler. "Vi kan ændre disse partikler og introducere forskellige funktioner, "forklarer Dr. Kristof Zarschler, forskningsassistent ved HZDR's Institute of Radiopharmaceutical Cancer Research. "For eksempel, vi kan vedhæfte et antistoffragment til partiklen, der specifikt binder sig til kræftceller. Dette antistoffragment er vores målgruppe, der leder nanopartiklen til tumoren. "
Målet for de modificerede nanopartikler er et antigen kendt som EGFR (epidermal vækstfaktorreceptor). Ved visse former for kræft, såsom brystkræft eller hoved og nakke tumorer, dette protein overudtrykkes på overfladen af cellerne. "Vi var i stand til at vise, at vores designede nanopartikler fortrinsvis interagerer med kræftcellerne via disse receptorer, "bekræfter Dr. Holger Stephan, leder af Nanoscalic Systems Group på HZDR. "I kontroltest med lignende nanopartikler, der var blevet modificeret med et uspecifikt antistof, betydeligt færre nanopartikler akkumuleret ved tumorcellerne. "
Forskerne undersøgte intensivt nanopartiklernes adfærd både i cellekulturer og i en dyremodel. Til dette formål, de gav nanopartiklerne yderligere reporterkarakteristika, som Kristof Zarschler forklarer:"Vi brugte to komplementære muligheder. Ud over antistofferne, vi fastgjorde farvestofmolekyler og radionuklider til nanopartiklerne. Farvestofmolekylet udsender i det nær infrarøde spektrum, der trænger ind i vævet og kan visualiseres med et passende mikroskop. Farvestoffet afslører således, hvor nanopartiklerne præcist er placeret. "Radionuklidet, kobber-64, opfylder et lignende formål. Det udsender stråling, der detekteres af en PET -scanner (positronemissionstomografi). Signalerne kan derefter konverteres til et tredimensionelt billede, der visualiserer fordelingen af nanopartikler i organismen.
Fremragende egenskaber i levende organismer
Ved hjælp af disse billedteknikker, forskere har kunnet vise, at akkumulering af nanopartikler i tumorvævet når maksimalt to dage efter administration til mus. De mærkede nanopartikler elimineres efterfølgende via nyrerne uden at være en byrde for kroppen. "De er tilsyneladende ideelle i størrelse og egenskaber, "siger Holger Stephan." Mindre partikler filtreres ud af blodet på få timer og har derfor kun en kortsigtet effekt. Hvis, på den anden side, partiklerne er for store, de ophobes i milten, lever eller lunger og kan ikke fjernes fra kroppen via nyrerne og blæren. "Samspillet mellem nanopartiklerne med en nøjagtig størrelse på tre nanometer og de vedhæftede antistoffragmenter har tydeligvis en positiv indflydelse på fordelingen og fastholdelsen af antistoffet i organismen såvel som på sin udskillelsesprofil.
I fremtidige forsøg, HZDR -forskerne vil teste, om de kan ændre deres system til at bære andre komponenter. Kristof Zarschler beskriver planerne:"Du kan tage disse nanopartikler og funktionalisere dem med et aktivt stof. Derefter kan du levere et lægemiddel direkte til tumoren. Dette kan være et terapeutisk radionuklid, der ødelægger tumorcellerne." Det er også muligt at vedhæfte antistoffragmenter, der er specifikke for andre proteiner end EGFR, til at målrette mod forskellige typer kræft.
 Varme artikler
Varme artikler
-
 Fysikere skaber kulmagnetisme ved at fjerne atomer fra grafitDette 3D -billede, opnået med et scanningstunnelmikroskop, viser en enkelt isoleret atomær stilling. Forskerne identificerede tilstedeværelsen af en skarp resonanstop oven på individuelle ledige sti
Fysikere skaber kulmagnetisme ved at fjerne atomer fra grafitDette 3D -billede, opnået med et scanningstunnelmikroskop, viser en enkelt isoleret atomær stilling. Forskerne identificerede tilstedeværelsen af en skarp resonanstop oven på individuelle ledige sti -
 Røntgen udløste nano-bobler til at målrette mod kræftDr. Wei Deng, CNBP. Kredit:CNBP Innovative lægemiddelfyldte nano-bobler, i stand til med succes at blive udløst i kroppen af røntgenstråler, er udviklet af forskere, baner vejen for en ny række
Røntgen udløste nano-bobler til at målrette mod kræftDr. Wei Deng, CNBP. Kredit:CNBP Innovative lægemiddelfyldte nano-bobler, i stand til med succes at blive udløst i kroppen af røntgenstråler, er udviklet af forskere, baner vejen for en ny række -
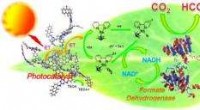 Kunstigt fotosyntesesystem får effektivitetsboost fra grafenIllustration af det kunstige fotosyntesesystem ved hjælp af en grafen-baseret fotokatalysator til at producere myresyre fra kuldioxid under synligt lys. Billedkredit:Yadav, et al. ©2012 American Chemi
Kunstigt fotosyntesesystem får effektivitetsboost fra grafenIllustration af det kunstige fotosyntesesystem ved hjælp af en grafen-baseret fotokatalysator til at producere myresyre fra kuldioxid under synligt lys. Billedkredit:Yadav, et al. ©2012 American Chemi -
 Selvsamlende nanopartikelarrays kan skifte mellem et spejl og et vindueVed at finjustere afstanden mellem nanopartikler i et enkelt lag, forskere har lavet et filter, der kan skifte mellem et spejl og et vindue. Udviklingen kan hjælpe forskere med at skabe specielle mat
Selvsamlende nanopartikelarrays kan skifte mellem et spejl og et vindueVed at finjustere afstanden mellem nanopartikler i et enkelt lag, forskere har lavet et filter, der kan skifte mellem et spejl og et vindue. Udviklingen kan hjælpe forskere med at skabe specielle mat
- Kølematerialer superhurtigt
- Sierra snowpack på 61%, da ny tørke truer for Californien denne sommer
- Hvor meget bevis er nok til at erklære en ny menneskeart?
- Polymerer går sammen om at levere
- Sådan Find X og Y Afbrydelser af Kvadratiske Ligninger
- Plastmikrofibre fundet for første gang i afføring af vilde dyr, fra sydamerikanske pels sæler


