Forskere opdager nye funktioner i molekylær elevator

Molekylær elevator. Kredit:Daria Sokol/MIPT
Biofysikere fra Moskva Institut for Fysik og Teknologi og University of Groningen i Holland har visualiseret en næsten komplet transportcyklus af pattedyrglutamattransportørhomologen fra archaea. De bekræftede, at transportmekanismen ligner en elevator:En "dør" åbnes, ioner og substratmolekyler kommer ind, døren lukker, og de bevæger sig gennem membranen. Formentlig fungerer pattedyrstransportørerne på samme måde, så denne opdagelse er potentielt vigtig for at udvikle nye behandlinger for skizofreni og andre psykiske sygdomme forårsaget af fejl i disse transportører. Forskningen blev offentliggjort i tidsskriftet Naturkommunikation .
Nerveimpulser bevæger sig gennem menneskekroppen i form af kemiske signaler eller elektriske ladninger, som ionstrømme. Neuroner, cellerne i nervesystemet, kan generere og formidle elektriske signaler. En neuron består af en cellelegeme med fremspring af to typer:flere dendritter og en enkelt axon. Cellekroppen og dendritterne fungerer som en antenne, der opfanger signaler fra andre neuroner. Ved at opsummere og behandle alle indgangssignalerne, neuronen genererer sine egne impulser, der derefter sendes videre til den tilstødende neuron. Den elektriske impuls i et axon ligner den elektriske strøm i ledninger, men den bæres af natrium- og calciumioner, frem for elektroner. Det sagt, elektrisk signaloverførsel er kun mulig inden for en neuron. Signalerne transmitteret mellem neuroner er af kemisk karakter og involverer særlige strukturer, kaldes synapser.
Signalet i en synapse bæres normalt af kemikalier kaldet neurotransmittere. En neuron frigiver neurotransmittere i den synaptiske kløft, og den modtagende neurons membran genkender neurotransmitteren via en dedikeret receptor.
Et andet skjult, men vigtigt trin i denne proces er, at neurotransmittermolekylerne skal fjernes fra den synaptiske kløft for at muliggøre den næste pulsoverførsel. Ellers, den modtagende neuron vil blive overstimuleret. Neurotransmittere ryddes ud af dedikerede transportører, der pumper disse molekyler fra den synaptiske kløft tilbage i cellelegemet. Disse transportører er placeret enten i synapser af neuroner eller i de såkaldte glialceller, som giver støtte og beskyttelse til neuroner (fig. 1).
Glutamat er den vigtigste excitatoriske neurotransmitter i den menneskelige hjerne. Når glutamat frigives til den synaptiske kløft, dette ophidser den næste neuron i sekvensen. Det menneskelige nervesystem har også hæmmende neurotransmittere, for eksempel GABA (gamma-aminosmørsyre), som snuser ethvert potentiale i neuronen ud, når det frigives.
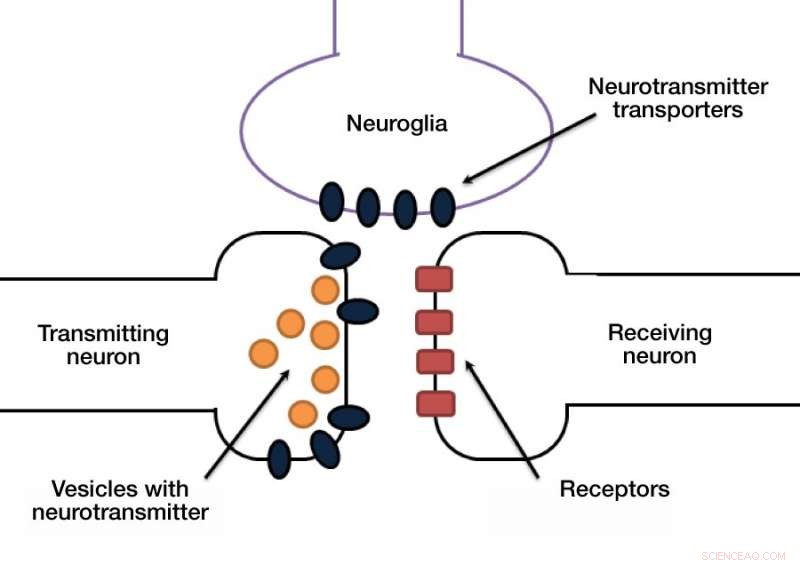
Figur 1. Synapse Credit:Anastasia Vlasova/MIPT
Glutamat -transportøren fjerner glutamat fra den synaptiske kløft. Denne proces er afgørende for den menneskelige hjernes funktion. Hæmningen af glutamatfjernelse fra kløften er forbundet med mange neurodegenerative sygdomme og psykiske lidelser, herunder skizofreni.
Ganske ofte kan vi lære meget om nogen ved blot at se på deres slægtninge. Det samme gælder for evolutionære lignende proteiner, kaldet homologer. Gruppen af russiske og hollandske forskere har løst et konformationelt ensemble af aspartattransportøren fra archaea, som er homolog med glutamattransportørerne hos mennesker.
Indtil for nylig, Røntgenkrystallografi var hovedteknikken til at studere 3-D strukturer af proteiner. Den største udfordring ved denne metode er krystallisering af proteiner for at opnå diffraktionsbilleder fra krystaller. Membranproteiner har en tendens til ikke let at danne velfungerende krystaller.
For at overvinde denne flaskehals, en anden teknik kaldet kryo-elektronmikroskopi kan bruges. I cryo-EM bestråles en forglaset prøve af en elektronstråle, og de indsamlede billeder kombineres, hvilket giver en tredimensionel rekonstruktion af proteinet. Den opnåede model analyseres og kan bruges til at designe nye lægemidler.
Strukturen af pattedyrglutamattransportørhomologen blev bestemt ved hjælp af et kryo-elektronmikroskop ved University of Groningen i Holland. Disse proteiner består af tre individuelle molekyler, derfor danner de trimere. Hver individuel protomer består af to dele:den ubevægelige del, der er fastgjort i membranen, og det mobile transportdomæne, der ligner en elevator. Undersøgelsen har afsløret 15 protomerstrukturer (i fem trimere), herunder mellemliggende konformationer. Teamet bekræftede også uafhængige bevægelser af transportdomæner.
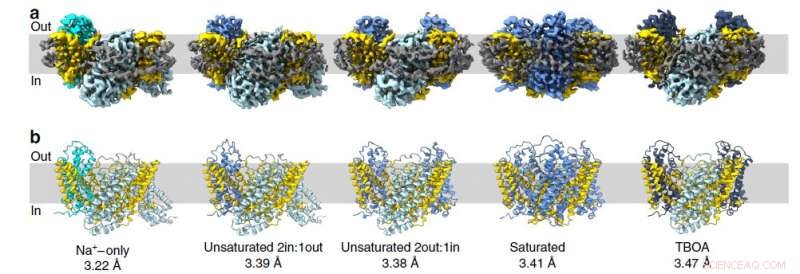
Figur 2. Glutamattransportørens struktur fra archaea i forskellige tilstande. Hvert billede repræsenterer et øjebliksbillede, hvor protomerer præsenteres i følgende tilstande:indadgående åben (stålblå), mellemliggende udad lukket apo (cyan), mellemliggende udad lukket asp (kornblomstblå), udadgående TBOA (mørkeblå) Kredit:Valentina Arkhipova et al./Nature Communications
"Disse strukturer hjælper os med at forklare, hvordan disse proteiner forhindrer natriumlækage, "lederen af MIPT -laboratoriet for strukturel elektronmikroskopi af biologiske systemer, Forklarede Albert Guskov. "Ligesom i en elevator, transportdomænet har en dør, og så længe det holder åbent, elevatoren vil ikke bevæge sig. Men når natriumionerne og substratet - i dette tilfælde, aspartatmolekylerne - ind i elevatoren, døren lukker, og det går. Så, hvis der kun er natriumioner til stede, det er ikke nok til at lukke døren. "
"Dette gør transporten meget effektiv, hvilket er særlig vigtigt i tilfælde af humane proteiner, da det ikke kun handler om at spise aspartatet op - som i archaea - men om informationsoverførsel mellem neuroner, "tilføjede forskeren.
Laboratoriet for strukturel elektronmikroskopi af biologiske systemer, ledet af professor Guskov, etablerer en moderne videnskabelig infrastruktur på MIPT, muliggøre fuld-cyklus forskning om enkeltpartikel kryo-EM i Rusland. I 2019, teamet lancerede en forskningsplatform baseret på kryo-elektronmikroskop FEI Polara G2 med yderligere planer om at opgradere det til det topmoderne mikroskop.
"Laboratoriets kompetencer er meget efterspurgte i det russiske videnskabelige samfund, og det ekspanderende internationale akademiske netværk giver adgang til moderne videnskabelig infrastruktur. Sådan infrastruktur åbner nye muligheder for at studere de grundlæggende spørgsmål om biologi, såsom mekanismerne for ionkanalers og transportørers funktioner, interaktioner inden for proteinkomplekser, osv. Det hjælper os også med at finde industrielle partnere, der ville forske i at anvende vores fund inden for lægemiddeldesign og andre steder i medicin, "Professor Guskov kommenterede.
 Varme artikler
Varme artikler
-
 Ny teknik lader læger forudsige sygdommens sværhedsgradForsker Guangfu Wang, PhD, fra University of Virginia School of Medicine, hjulpet med at udvikle den nye teknik, der vil lade læger bedre diagnosticere sygdom og forudsige patientforløb. Kredit:Josh B
Ny teknik lader læger forudsige sygdommens sværhedsgradForsker Guangfu Wang, PhD, fra University of Virginia School of Medicine, hjulpet med at udvikle den nye teknik, der vil lade læger bedre diagnosticere sygdom og forudsige patientforløb. Kredit:Josh B -
 Løbeelektronik ved hjælp af lysKonventionelt printkort. (PhysOrg.com) -- Hvis du åbner næsten enhver elektronisk gadget, du vil se forskellige elementer, der fungerer ved hjælp af elektriske kredsløb, fortæller Nader Engheta
Løbeelektronik ved hjælp af lysKonventionelt printkort. (PhysOrg.com) -- Hvis du åbner næsten enhver elektronisk gadget, du vil se forskellige elementer, der fungerer ved hjælp af elektriske kredsløb, fortæller Nader Engheta -
 Forskere skaber perfekte nanoscrolls fra grafenes ufuldkomne formEt elektronmikroskopibillede viser mange eksempler på nanoscrolls. Indsatsen zoomer ind på en enkelt nanoscroll og afslører dens koniske karakter. Fremtidens vandfiltre kan være lavet af milliarde
Forskere skaber perfekte nanoscrolls fra grafenes ufuldkomne formEt elektronmikroskopibillede viser mange eksempler på nanoscrolls. Indsatsen zoomer ind på en enkelt nanoscroll og afslører dens koniske karakter. Fremtidens vandfiltre kan være lavet af milliarde -
 Forskere opnår første direkte observation af facetdannelse i nanokuberBerkeley Lab-forskere fandt ud af, at forskelle i ligandmobilitet under krystallisering forårsager lavindeksfacetterne -- {100}, {110} og {111} - for at stoppe med at vokse på forskellige tidspunkter,
Forskere opnår første direkte observation af facetdannelse i nanokuberBerkeley Lab-forskere fandt ud af, at forskelle i ligandmobilitet under krystallisering forårsager lavindeksfacetterne -- {100}, {110} og {111} - for at stoppe med at vokse på forskellige tidspunkter,
- Støvede støvsugere kan være astronauternes største sundhedsrisiko
- Cryptominers drømmer om rebound efter priskrak
- Hvorfor er vi nødt til at spare på vand?
- Langtidslogningsundersøgelse viser virkninger på chimpanser og gorillaer i Republikken Congo
- Er fremtiden for arbejde nødvendigvis glamourøs? Digitale nomader og van-liv
- Er universets skjulte stof blevet opdaget?


