Hvordan man får flere kræftbekæmpende nanopartikler derhen, hvor der er brug for dem
Kredit:CC0 Public Domain
University of Toronto Engineering forskere har opdaget en dosistærskel, der i høj grad øger leveringen af kræftbekæmpende lægemidler til en tumor.
At bestemme denne tærskel giver en potentielt universel metode til at måle nanopartikeldosering og kan hjælpe med at fremme en ny generation af cancerterapi, billeddiagnostik og diagnostik.
"Det er en meget simpel løsning, justering af dosis, men resultaterne er meget kraftfulde, " siger MD/Ph.D.-kandidat Ben Ouyang, der ledede forskningen under supervision af professor Warren Chan.
Deres resultater blev offentliggjort i dag i Naturmaterialer , leverer løsninger på et problem med narkotikalevering, som Chan og forskere tidligere har rejst for fire år siden i Naturanmeldelser Materialer .
Nanoteknologiske bærere bruges til at levere lægemidler til kræftsteder, hvilket igen kan hjælpe en patients reaktion på behandlingen og reducere bivirkninger, såsom hårtab og opkastning. Imidlertid, i praksis, få injicerede partikler når tumorstedet.
I den Naturanmeldelser Materialer papir, holdet undersøgte litteratur fra det sidste årti og fandt ud af, at på median, kun 0,7 procent af de kemoterapeutiske nanopartikler gør det til en målrettet tumor.
"Løftet om nye lægemidler afhænger af vores evne til at levere dem til målstedet, " forklarer Chan. "Vi har opdaget et nyt princip for at forbedre leveringsprocessen. Dette kan være vigtigt for nanoteknologi, genom redaktører, immunterapi, og andre teknologier."
Chans hold så leveren, som filtrerer blodet, som den største barriere for levering af nanopartikler. De antog, at leveren ville have en tærskel for optagelseshastighed - med andre ord, når organet bliver mættet med nanopartikler, det ville ikke være i stand til at holde trit med højere doser. Deres løsning var at manipulere dosen for at overvælde organets filtrerende Kupffer-celler, som beklæder leverkanalerne.
Forskerne opdagede, at injicering af en baseline på 1 billion nanopartikler i mus, in vivo, var nok til at overvælde cellerne, så de ikke kunne optage partikler hurtigt nok til at holde trit med de øgede doser. Resultatet er en leveringseffektivitet på 12 procent til tumoren.
"Der er stadig meget arbejde at gøre for at øge de 12 procent, men det er et stort skridt fra 0,7, " siger Ouyang. Forskerne testede også grundigt, om overvældende Kupffer-celler førte til nogen risiko for toksicitet i leveren, hjerte eller blod.
"Vi testede guld, silica, og liposomer, " siger Ouyang. "I alle vores studier, uanset hvor højt vi pressede dosis, vi har aldrig set nogen tegn på toksicitet."
Holdet brugte dette tærskelprincip til at forbedre effektiviteten af en klinisk brugt og kemoterapifyldt nanopartikel kaldet Caelyx. Deres strategi krympede tumorer 60 procent mere sammenlignet med Caelyx alene ved en fast dosis af kemoterapien, doxorubicin.
Fordi forskernes løsning er enkel, de håber at se tærsklen have positive implikationer i selv nuværende nanopartikel-doseringskonventioner for humane kliniske forsøg. De beregner, at den menneskelige tærskel ville være omkring 1,5 kvadrillion nanopartikler.
"Der er en enkelhed ved denne metode og afslører, at vi ikke behøver at redesigne nanopartiklerne for at forbedre leveringen, " siger Chan. "Dette kunne overvinde et stort leveringsproblem."
 Varme artikler
Varme artikler
-
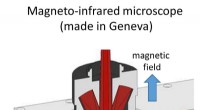 On-demand kontrol af terahertz og infrarøde bølgerDen eksperimentelle enhed, der fokuserede infrarød og terahertz-stråling på små prøver af ren grafen i magnetfeltet, bygget af UNIGE-teamet. Kredit:UNIGE, Ievgeniia Nedoliuk Evnen til at kontrolle
On-demand kontrol af terahertz og infrarøde bølgerDen eksperimentelle enhed, der fokuserede infrarød og terahertz-stråling på små prøver af ren grafen i magnetfeltet, bygget af UNIGE-teamet. Kredit:UNIGE, Ievgeniia Nedoliuk Evnen til at kontrolle -
 Små nanokrystaller skaber en lysere fremtid for tv-seere, undersøgelse finderKredit:ACS Curtin University-forskere har opdaget bittesmå grønnere nanokrystaller, der kan manipuleres til at producere billeder og belysning af høj kvalitet i elektroniske enheder såsom fjernsyn
Små nanokrystaller skaber en lysere fremtid for tv-seere, undersøgelse finderKredit:ACS Curtin University-forskere har opdaget bittesmå grønnere nanokrystaller, der kan manipuleres til at producere billeder og belysning af høj kvalitet i elektroniske enheder såsom fjernsyn -
 Forskers nanopartikelnøgle til ny malariavaccineDenne selvsamlende protein-nanopartikel er afhængig af stive proteinstrukturer kaldet spiralspoler (blå og grøn i billedet) for at skabe en stabil ramme, som forskere kan vedhæfte malariaparasitantige
Forskers nanopartikelnøgle til ny malariavaccineDenne selvsamlende protein-nanopartikel er afhængig af stive proteinstrukturer kaldet spiralspoler (blå og grøn i billedet) for at skabe en stabil ramme, som forskere kan vedhæfte malariaparasitantige -
 Biomimetiske nanosvampe absorberer toksiner frigivet af bakterielle infektioner og giftIngeniører ved University of California, San Diego har opfundet en nanosvamp, der sikkert kan fjerne en bred klasse af farlige toksiner fra blodbanen, inklusive toksiner produceret af MRSA, E coli ,
Biomimetiske nanosvampe absorberer toksiner frigivet af bakterielle infektioner og giftIngeniører ved University of California, San Diego har opfundet en nanosvamp, der sikkert kan fjerne en bred klasse af farlige toksiner fra blodbanen, inklusive toksiner produceret af MRSA, E coli ,
- Ultra-lyse tidlige galakser kan være mindre almindelige, end vi tror
- Zoom for at fokusere på sikkerhed, privatliv, CEO siger, som brug boomer under coronakrisen
- Afrikanske krokodiller levede i Spanien for seks millioner år siden
- En ny undersøgelse skulle være det sidste søm for åbne kontorlandskaber
- Lavstrømsforskning på Colorado River kaster lys over en eventuel ny normal for Grand Canyon
- Underjordisk lagring af kulstof fanget direkte fra luften - grønt og økonomisk


