Ny nanoinducer af interferoner fundet til cancerimmunterapi
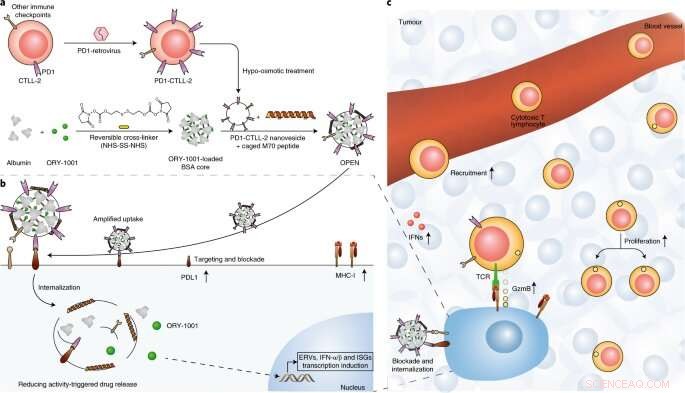
Fig. 1:Skematisk illustration af forberedelsen og virkningsmekanismen for OPEN. Kredit:DOI:10.1038/s41565-021-00972-7
Kræftimmunterapi såsom immun checkpoint blokade (ICB) er en revolutionerende behandling mod tumorer ved at styrke immunovervågningen og endda inducere langsigtet sygdomskontrol.
Type I interferoner (IFN'er) er nøglekoordinatorer for interaktion mellem tumor og immunsystem. Nedsat IFN-signalering er forbundet med dårlig prognose hos patienter med tyktarmskræft, melanom, triple-negativ brystkræft, osv. Nuværende IFN supplerende terapi medfører nogle gange alvorlige bivirkninger og IFN-induceret multigen resistens-program til ICB.
I en undersøgelse offentliggjort i Natur nanoteknologi , et forskerhold ledet af Li Yaping og Zhang Pengcheng fra Shanghai Institute of Materia Medica fra det kinesiske videnskabsakademi (CAS) demonstrerede, at de paradoksale virkninger af IFN supplerende terapi kunne løses ved hjælp af en T-lymfocytmembran-dekoreret epigenetisk nanoinducer af IFN'er (OPEN ).
Forskerne manipulerede først genetisk en programmeret dødsreceptor 1 (PD1)-overudtrykkende cytotoksisk T-cellelinje, og brugte derefter membranen af disse celler til at omslutte proteinnanopartikler fyldt med ORY-1001, en hæmmer af lysin-specifik histon demethylase 1 (LSD1), at skabe ÅBEN.
De afslørede, at OPEN forbedrede den intratumorale akkumulering af ORY-1001 og lokal produktion af IFN'er efter intravenøs administration, og demonstrerede, at IFN'erne øgede tumorinfiltration, proliferation og aktivitet af tumorspecifikke cytotoksiske T-celler og antigenvisning af tumorceller.
Udover, de beviste, at den IFN-inducerede programmerede dødsligand 1 (PDL1) og andre immuncheckpoint-molekyler let blev neutraliseret ved efterfølgende OPEN. Denne sekventielle proces genopfyldte specifikt intratumorale IFN'er og lindrede IFN-induceret immunundvigelse, og dermed hæmme tumorvækst i flere tumormodeller.
"Undersøgelsen demonstrerer en elegant strategi til at løse de paradoksale virkninger af IFN supplerende terapi ved hjælp af epigenetisk nanoinducer af IFN'er. Det er en milepæl inden for nanomedicin for sikrere og mere effektiv cancerimmunterapi, " sagde prof. Zhao Yuliang, en akademiker i CAS.
"Dette er den første forskning, der uddyber det store potentiale af epigenetisk nanomedicin i cancerimmunterapi. Nanomedicinen har betydelig klinisk translationsværdi på grund af dens fordele i tumormålrettet levering og immun checkpoint blokade, " sagde prof. Hao Xishan, en akademiker fra Chinese Academy of Engineering (CAE).
 Varme artikler
Varme artikler
-
 Rustbeskyttelse mod nanokapslerGenlukkelige korrosionsbeholdere:Kapslerne åbner, når de reduceres, og kaliumioner vandrer ind i polymerskallen. Så snart korrosionen standser, polymeren oxideres, kapslerne lukker og frigiver kaliumi
Rustbeskyttelse mod nanokapslerGenlukkelige korrosionsbeholdere:Kapslerne åbner, når de reduceres, og kaliumioner vandrer ind i polymerskallen. Så snart korrosionen standser, polymeren oxideres, kapslerne lukker og frigiver kaliumi -
 Med en enkel belægning, nanotråde viser en dramatisk stigning i effektivitet og følsomhedDette er et nærbillede af en belagt nanotråd. Kredit:Hilsen af Ken Crozier, Harvard School of Engineering and Applied Sciences. Ved at påføre en belægning på individuelle silicium nanotråde, for
Med en enkel belægning, nanotråde viser en dramatisk stigning i effektivitet og følsomhedDette er et nærbillede af en belagt nanotråd. Kredit:Hilsen af Ken Crozier, Harvard School of Engineering and Applied Sciences. Ved at påføre en belægning på individuelle silicium nanotråde, for -
 Nanosfærer strækker grænserne for harddisklagring(PhysOrg.com) -- Et nyt magnetisk optagemedie bestående af bittesmå nanosfærer er blevet udtænkt af europæiske forskere. Teknologien kan føre til harddiske i stand til at gemme mere end tusind milliar
Nanosfærer strækker grænserne for harddisklagring(PhysOrg.com) -- Et nyt magnetisk optagemedie bestående af bittesmå nanosfærer er blevet udtænkt af europæiske forskere. Teknologien kan føre til harddiske i stand til at gemme mere end tusind milliar -
 Forskere udvikler nye tumor-krympende nanopartikler til at bekæmpe kræft, forhindre gentagelseKredit:CC0 Public Domain Et forskerhold fra Mayo Clinic har udviklet en ny type kræftbekæmpende nanopartikel, der sigter mod at formindske brystkræfttumorer, samtidig med at det forhindrer tilbage
Forskere udvikler nye tumor-krympende nanopartikler til at bekæmpe kræft, forhindre gentagelseKredit:CC0 Public Domain Et forskerhold fra Mayo Clinic har udviklet en ny type kræftbekæmpende nanopartikel, der sigter mod at formindske brystkræfttumorer, samtidig med at det forhindrer tilbage
- Hvad er Gummiegenskaber?
- Transformativ forskning urealistisk at forudsige, videnskabsmænd fortæller bevillingsorganer
- Hjælper voksne med at finde rundt i beslutningen om at flytte sammen med forældrene igen
- Livslange anonymitetsordrer:fungerer de stadig i de sociale mediers tidsalder?
- Arkæologer fejrer den spektakulære opdagelse af jernalderens skatte
- Forskere er pionerer med ny teknik til at omdanne brugte mælkeflasker til kajakker og lagertanke


