Nanostoffer fra lamaer kunne give cellespecifik medicin til mennesker
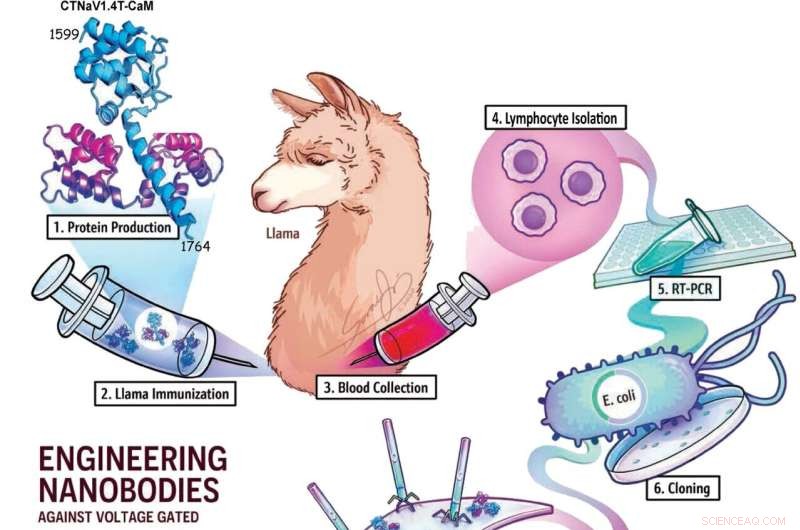
Grafisk abstrakt. Kredit:Sora Ji
I "proof of concept"-eksperimenter med mus og humane celler og væv siger Johns Hopkins Medicine-forskere, at de har designet bittesmå proteiner, kaldet nanobodies, afledt af lama-antistoffer, som potentielt kan bruges til at levere målrettet medicin til menneskelige muskelceller. Forskerne siger, at evnen til mere præcist at målrette sådanne væv kunne fremme søgen efter sikrere, mere effektive måder at lindre smerte under operation, behandle uregelmæssige hjerterytmer og kontrollere anfald.
Resultaterne af eksperimenterne blev offentliggjort den 21. februar i Journal of Biological Chemistry .
Nanobodies er små versioner af proteiner kaldet antistoffer, der markerer potentielle patogener til ødelæggelse af immunsystemet. Forskere ved ikke, hvorfor de kun findes i nogle arter, såsom kamelider og hajer, men siden deres opdagelse i 1980'erne har forskere studeret dem til brug som et forskningsværktøj og leveringssystem til anti-cancermedicin med blandet succes.
Forskerne ved Johns Hopkins var opmærksomme på sådanne eksperimenter, og de havde mistanke om, at nanobodies kunne være nyttige som et værktøj til at binde sig til en celles natriumionkanaler, som fungerer som en slags kontakt, der kan lede kemiske signaler, der tænder eller slukker for muskelceller.
Ni varianter af disse kontakter vises i den menneskelige krop, hver specifik for en type væv, såsom muskel eller nerve. Fordi kanalproteinerne kun har små forskelle indbyrdes, kan de fleste medikamenter ikke skelne mellem dem, hvilket udgør sikkerhedsrisici, når de forsøger at bruge dem sammen med lægemidler som anæstetika. Eksisterende lægemidler, siger forskerne, blokerer smerte og beroliger en patient ved at "slukke" for natriumionkanalerne i nerver og skeletmuskulatur, men kan også farligt sænke hjertefrekvensen og forstyrre hjerterytmen.
Andre undersøgelser, siger Johns Hopkins Medicine-forskere, har faktisk vist, at nanobodies kan bruges til at transportere en last, en evne, der kunne fremme indsatsen for at levere medicin til specifikke natriumionkanaler og eliminere sådanne bivirkninger.
"Det er grunden til, at klinikere og farmaceutiske virksomheder er interesserede i at finde lægemidler, der kan modulere disse kanaler - enten til at tænde eller slukke - tydeligt," siger Sandra Gabelli, Ph.D., lektor i medicin ved Johns Hopkins University School of Medicine .
Gabelli erkendte, at den lille størrelse af nanostoffer kunne gøre det muligt for dem at binde til områder, der er utilgængelige for større molekyler, såsom større antistoffer, der ofte bruges til lignende applikationer.
I deres proof of concept-eksperimenter screenede Gabellis forskerhold et meget stort bibliotek med 10 millioner nanobodies for at udvikle dem som proteinbiologiske stoffer, der potentielt kunne skelne mellem natriumionkanalerne i musklerne kontra dem i nerverne.
I samarbejde med Manu Ben-Johny ved Columbia University har forskerne knyttet et fluorescerende "reporter"-molekyle til nanolegemerne, der lyser op, når det interagerer med natriumkanalen. Ved at overvåge gløden fandt forskerne ud af, at to nanobodies, Nb17 og Nb82, er knyttet til natriumionkanalerne, der er specifikke for skeletmuskulaturen og hjertemusklen.
Forskerne testede også nanobodies stabilitet ved forskellige temperaturer, en nøglefaktor i udvikling og levering af lægemidler til klinikker. Forskerholdet fandt ud af, at nanobodies Nb17 og Nb82 var modstandsdygtige over for temperaturer op til henholdsvis 168,8 og 150,8 grader Fahrenheit, hvilket indikerer, at disse nanobodies ville forblive hyldestabile under normale forhold.
Forskerne planlægger derefter at afbilde nanobody- og natriumionkanalerne bundet sammen for at afsløre mere om, hvordan denne interaktion fungerer. + Udforsk yderligere
Miniature lama-antistoffer kan hjælpe med at bekæmpe SARS-CoV-2-varianter
Sidste artikelDetektering af virus i et nålestik
Næste artikelNy billedbehandlingsmetode gør små robotter synlige i kroppen
 Varme artikler
Varme artikler
-
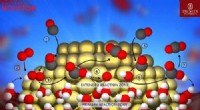 Gulds uventede oxidationsaktivitet:Afkodning af vandets rolle i guld -nanokatalyseSkematisk fremstilling af den laveste energibane for CO-oxidation på guld-titania-katalysatorer. Vandlaget på titania -understøtningen forlænger reaktionszonen på guld -nanoklyngen og tilvejebringer p
Gulds uventede oxidationsaktivitet:Afkodning af vandets rolle i guld -nanokatalyseSkematisk fremstilling af den laveste energibane for CO-oxidation på guld-titania-katalysatorer. Vandlaget på titania -understøtningen forlænger reaktionszonen på guld -nanoklyngen og tilvejebringer p -
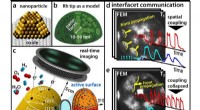 Nanopartikler:Kemiens komplekse rytme(a) Moderne katalysatorer består af nanopartikler; (b) En Rhodium-spids som model for en nanopartikel; (c) Sporing af en kemisk reaktion i realtid med et feltemissionsmikroskop (d) Ved lave temperatur
Nanopartikler:Kemiens komplekse rytme(a) Moderne katalysatorer består af nanopartikler; (b) En Rhodium-spids som model for en nanopartikel; (c) Sporing af en kemisk reaktion i realtid med et feltemissionsmikroskop (d) Ved lave temperatur -
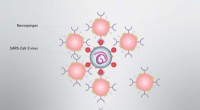 Nanosvampe kunne opsnappe SARS-CoV-2 coronavirus-infektionI laboratorieforsøg, både lungecelle- og immuncelletyper af nanosvampe fik SARS-CoV-2-virussen til at miste næsten 90% af sin virale infektivitet på en dosisafhængig måde. Viral infektivitet er et mål
Nanosvampe kunne opsnappe SARS-CoV-2 coronavirus-infektionI laboratorieforsøg, både lungecelle- og immuncelletyper af nanosvampe fik SARS-CoV-2-virussen til at miste næsten 90% af sin virale infektivitet på en dosisafhængig måde. Viral infektivitet er et mål -
 Fundamentale fotoresistkemifund kunne hjælpe med at udvide Moores lovNår lave koncentrationer af tværbinder tilsættes til resisten (venstre), det er i stand til at mønstre mindre funktioner og kræver ikke længere, dyre eksponeringer som med høje koncentrationer af tvær
Fundamentale fotoresistkemifund kunne hjælpe med at udvide Moores lovNår lave koncentrationer af tværbinder tilsættes til resisten (venstre), det er i stand til at mønstre mindre funktioner og kræver ikke længere, dyre eksponeringer som med høje koncentrationer af tvær
- At spise lokal og plantebaseret kost:hvordan man fodrer byer bæredygtigt
- Et nyt ruminstrument fanger sit første soludbrud
- Solvindprøver antyder ny fysik af massive soludslip
- Små magneter kan rumme hemmeligheden bag nye kvantecomputere
- Biokemikere forbinder syntetisk forbindelse med produktion af sulthormoner
- Hvorfor bruges natrium i DNA-ekstraktion?


