Bryde barrierer i lægemiddellevering med bedre lipid nanopartikler
Mange sygdomme kan med succes behandles i det simple miljø i en cellekulturskål, men for at behandle rigtige mennesker med succes, skal lægemiddelagenten tage en rejse gennem det uendeligt mere komplekse miljø i vores kroppe og ankomme intakt inde i de berørte celler. Denne proces, kaldet medicinafgivelse, er en af de vigtigste barrierer inden for medicin.
Et samarbejde mellem Lawrence Berkeley National Laboratory (Berkeley Lab) og Genentech, et medlem af Roche-gruppen, arbejder på at bryde igennem nogle af flaskehalse ved levering af lægemidler ved at designe de mest effektive lipid-nanopartikler (LNP'er) - små sfæriske poser lavet af fedtmolekyler der indkapsler terapeutiske midler, indtil de dokker med cellemembraner og frigiver deres indhold. Det første lægemiddel til at bruge LNP'er blev godkendt i 2018, men leveringsmetoden steg til global fremtræden med Pfizer og Moderna mRNA COVID-vaccinerne.
"Det er et ret smart system, for hvis man bare leverer selve RNA'et til den menneskelige krop, bliver RNA'et nedbrudt af nukleaser og kan ikke let krydse cellemembranen på grund af dens størrelse og ladning, men LNP'erne leverer det sikkert ind i cellen, " forklarede co-lead forfatter Chun-Wan Yen, en senior hovedforsker i Genentechs Small Molecule Pharmaceutical Sciences-gruppe.
LNP'er bliver nu bredt udforsket som et leveringssystem for vacciner mod andre infektionssygdomme eller terapeutiske vacciner mod cancer. Levedygtigheden af disse nye applikationer vil være afhængig af, hvor godt lipidkapperne smelter sammen med målceller, hvor stabile lægemiddel-LNP-formuleringerne er i opbevaring (så de har en lang holdbarhed), og hvor stabile de er i kroppen (så de kan give langvarig lægemiddelaktivitet).
Alle disse egenskaber styres af blandingen af molekyler, der bruges til at skabe LNP, og den resulterende 3D-struktur af partiklen. Holdet under Yen og andre medledere Greg Hura og Michal Hammel, begge Berkeley Lab-biofysikere, har i flere år studeret, hvordan man tuner strukturen af LNP'er til ønskede egenskaber.
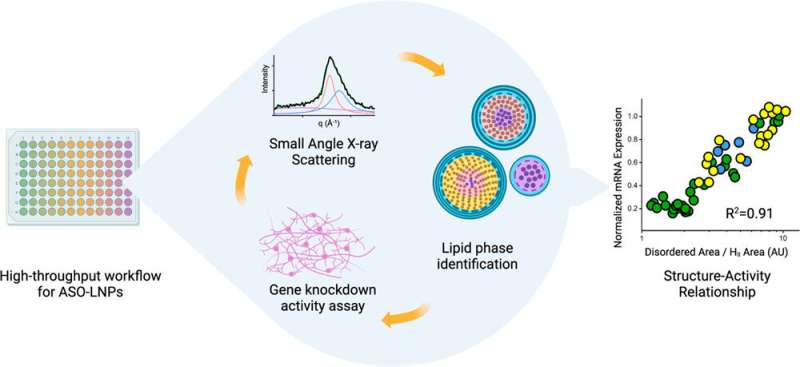
Deres seneste papir, udgivet for nylig i ACS Nano , dokumenterer, hvordan en workflow med høj gennemstrømning giver dem mulighed for at producere og karakterisere LNP'er med rekordhastighed. Undersøgelsen omfatter også den første nogensinde demonstration af, hvordan LNP-struktur korrelerer med aktiviteten af dets indhold, som til denne undersøgelse var et anti-sense oligonukleotid (ASO). ASO'er er små udsnit af RNA eller DNA-basepar, der blokerer genekspression ved at binde sig til strenge af mRNA og forhindre dem i at blive oversat til proteiner. ASO'er er en fantastisk måde at behandle sygdomme forårsaget af defekte proteiner eller overflod af et protein. Men ligesom mRNA er de modtagelige for roving-nukleaser - enzymer, der nedbryder RNA og DNA - og celler optager dem ikke uden videre.
Forskerne opdagede, at ASO-bærende LNP'er med pænt ordnede, tætpakkede interne strukturer førte til bedre lyddæmpning af et defekt gen i menneskelige neuroner, der er forbundet med en degenerativ sygdom, sammenlignet med LNP'er, der havde en mere uordnet struktur. Resultaterne var fra cellulære aktiviteter, ikke fra dyreforsøg, så der er stadig mere arbejde forude, men teamet er spændte på at bygge videre på denne indsigt ved hjælp af de komplementære værktøjer fra hver institution.

"Vi genererer LNP'erne i high-throughput, og Greg og Michals team kan tilbyde high-throughput-analysen," sagde Yen. "Hvis man tjekker udgivelsen i dag, laver de typisk bare en eller to formuleringer, men for os er det anderledes. Vi kan generere store datasæt, og jeg tror, det er grunden til, at vi kan have dette meget unikke og fede fund."
"Dette papir beskriver virkelig den metode, som vi vil anvende på de tusindvis af andre formuleringer, som vi har til hensigt at karakterisere," tilføjede Hura, som er en del af Berkeley Labs Biosciences-område. "Vi håber, at dette vil være en generel metode for folk til at optimere deres lipid-nanopartikler. Hvad enten det er vacciner, og igen, har vaccinerne fået den største opmærksomhed hidtil eller længere. Denne type terapi har en meget bred anvendelse ud over det. ."
Sådan bygger man en lipid-nanopartikel
Strukturerne af LNP'er påvirkes af, hvordan du blander dem, hvad du blander sammen og i hvilken rækkefølge. LNP'er har fire ingredienser - ioniserbare lipider, hjælpefosfolipider, kolesterol og polyethylenglycol-lipider (PEG-lipider) - og hver ingrediens har forskellige former. Plus, de kan kombineres i forskellige forhold, hvilket fører til et eksponentielt antal mulige formler. Yderligere komplicerer sagerne, LNP'erne ændrer sig med tiden. En formulering, der begynder som en pæn, tætpakket kugle vil til sidst forvandles til en mere uordnet struktur.
Forskere hos Genentech udviklede en robot-drevet arbejdsgang, der kan generere hundredvis af LNP-formuleringer på blot et par timer. Prøver af hver formulering bringes derefter til Berkeley Lab for at udføre small-angle X-ray scattering (SAXS) ved Advanced Light Source, en cirkulær partikelaccelerator, der skaber røntgenstråler med forskellige energier.
Den biologiske SAXS-strålelinje kan hurtigt behandle mange prøver, og i modsætning til andre former for røntgendiffraktion på biologiske materialer, behøver prøverne ikke at blive frosset eller krystalliseret - hvilket kan ændre strukturen af LNP'erne og forhindre forskerne i at opdage, hvad LNP'er ville se ud ved fysiologiske temperaturer i den menneskelige krop. SAXS giver dem også mulighed for at tage snapshots af LNP'er på bestemte tidspunkter for at bestemme deres strukturelle levetid.
Derudover bruger Genentech-teamet en accelereret proces til at studere, hvordan LNP'er påvirker genekspression i deres målceller. Ved at kombinere alle disse fremskyndede teknikker er hele samarbejdet i stand til at screene potentielle LNP'er med en hidtil uset hastighed.
Yen planlægger at fortsætte med at bruge SAXS-strålelinjen til at studere små detaljer, såsom hvordan en ændring på 1 % i ingredienskoncentration eller brug af en ny maskine under produktionen kan påvirke LNP's cellulære aktivitet, såvel som store spørgsmål, såsom om LNP'er opfører sig anderledes, hvis de er transport af andre lasttyper, og hvordan de interagerer med forskellige målceller.
"Vi ved, at mRNA LNP'er virker, men der er stadig et stort vidensgab," sagde Yen. "Derfor føler jeg, at vores papir er en pioner på dette område, og forhåbentlig kan vi også generere mere data og forståelse for fremtidige applikationer."
Flere oplysninger: Michal Hammel et al., Korrelering af strukturen og gendæmpningsaktiviteten af oligonukleotidfyldte lipid-nanopartikler ved brug af røntgenspredning med lille vinkel, ACS Nano (2023). DOI:10.1021/acsnano.3c01186
Journaloplysninger: ACS Nano
Leveret af Lawrence Berkeley National Laboratory
 Varme artikler
Varme artikler
-
 Ny målemetode afslører, at der kan være mere plastik på end i din salatKredit:Pixabay Det er nu muligt at måle, hvor mange plastikpartikler der er i vores mad. Kinesiske videnskabsmænd og professor Willie Peijnenburg fra Leiden Universitet anvendte deres nye metode ti
Ny målemetode afslører, at der kan være mere plastik på end i din salatKredit:Pixabay Det er nu muligt at måle, hvor mange plastikpartikler der er i vores mad. Kinesiske videnskabsmænd og professor Willie Peijnenburg fra Leiden Universitet anvendte deres nye metode ti -
 Multifunktionel nanofiber beskytter mod eksplosionerPara-aramid nanofiberplader oven på Twaron®-plader efter fragmentsimuleringsprojektiltestning. Kredit:Grant Gonzalez/Harvard SEAS Siden Første Verdenskrig, langt størstedelen af amerikanske kamp
Multifunktionel nanofiber beskytter mod eksplosionerPara-aramid nanofiberplader oven på Twaron®-plader efter fragmentsimuleringsprojektiltestning. Kredit:Grant Gonzalez/Harvard SEAS Siden Første Verdenskrig, langt størstedelen af amerikanske kamp -
 Smart mobilværktøj kan bruges til at diagnosticere og behandle alvorlige sygdommePrototyper af den beregningssensor, der er designet af maskinlæring, er vist. Kredit:Aydogan Ozcan/UCLA At finde praktiske løsninger til at opdage proteiner, kræftbiomarkører, vira og andre små ge
Smart mobilværktøj kan bruges til at diagnosticere og behandle alvorlige sygdommePrototyper af den beregningssensor, der er designet af maskinlæring, er vist. Kredit:Aydogan Ozcan/UCLA At finde praktiske løsninger til at opdage proteiner, kræftbiomarkører, vira og andre små ge -
 Topologiske grafen -nanoribber fanger elektroner til nye kvantematerialerScanning af tunnelmikroskopbillede af et topologisk nanoribbon -supergitter. Elektroner er fanget i grænsefladerne mellem brede båndsegmenter (som er topologisk ikke-trivielle) og smalle båndsegmenter
Topologiske grafen -nanoribber fanger elektroner til nye kvantematerialerScanning af tunnelmikroskopbillede af et topologisk nanoribbon -supergitter. Elektroner er fanget i grænsefladerne mellem brede båndsegmenter (som er topologisk ikke-trivielle) og smalle båndsegmenter
- Kaster nyt lys over opladning af lithium-ion-batterier
- Hvorfor klimabevægelsen skal gøre mere for at mobilisere ældre
- AI er kommet for at blive. Nu skal vi sikre, at alle får gavn
- Et rullebart tv? LGs seneste OLED TV-fjernsyn har en futuristisk 'wow'-faktor
- Udfordringer i forsyningskæden forbliver, når stater begynder at genåbne
- Maskinlæring tilbyder en ny måde at designe kirale krystaller på


