Mikrobiomundersøgelser hjælper med at udforske behandlinger for genetiske lidelser
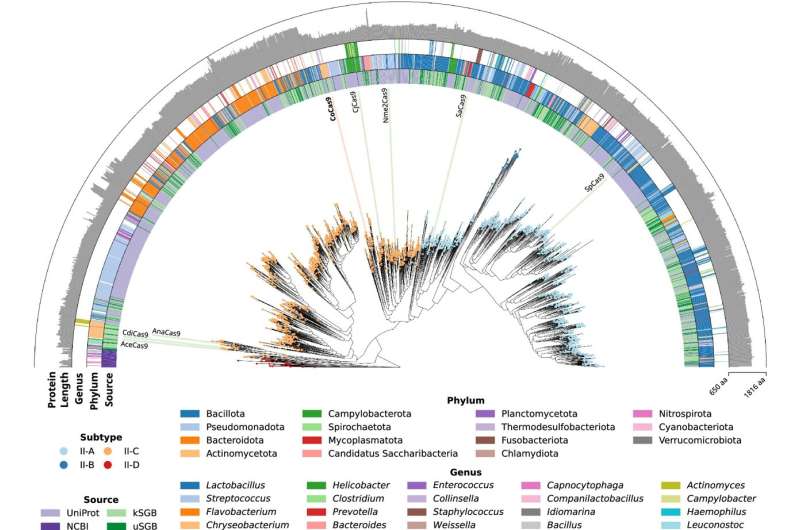
Et samarbejde har ført til identifikation, i en bakterie i tarmen, af nye CRISPR-Cas9 molekyler, der kunne have et klinisk potentiale til at behandle genetiske sygdomme som retinitis pigmentosa, gennem sub-retinale injektioner. Anna Cereseto og Nicola Segata fra Department of Cellular, Computational and Integrative Biology ved University of Trento er gået sammen og kombineret deres ekspertise for at udvikle nye terapier til behandling af genetiske sygdomme.
En undersøgelse, med Anna Cereseto og Nicola Segata som korresponderende og seniorforfattere, er blevet offentliggjort i Nature Communications .
Forskere over hele verden undersøger genomiske terapier for at finde nye behandlinger for genetiske lidelser. Genomredigering ved hjælp af CRISPR-Cas9-systemet er baseret på brugen af Cas9-proteinet, der fungerer som en molekylær saks, der kan programmeres til at foretage specifikke modifikationer i genomet for at skære eller erstatte skadelige DNA-sekvenser og korrigere de mutationer, der forårsager sygdomme.
Denne bioteknologi blev opdaget i 2012 i USA og har allerede ført til én godkendt behandling, et lægemiddel mod seglcellesygdom.
Nu bringer undersøgelsen udført af University of Trento genomisk forskning et skridt fremad.
"Sammenlignet med andre CRISPR-Cas9-tilgange er den, vi har identificeret, præcis og effektiv og mere kompakt. Dette nye CRISPR-Cas9-molekyle, som demonstreret af vores eksperimenter i nethinden, vil lettere blive leveret til de organer, der skal behandlet i terapier for genetiske sygdomme," siger Anna Cereseto, der siden 2018 har været involveret i undersøgelser af den genomiske redaktør med udviklingen af evoCas9.
Det er nødvendigt at udvide rækken af CRISPR-Cas-værktøjer for at fremskynde udviklingen af terapier til genetiske sygdomme. Dette kan laves ved at modificere naturlige enzymer, som det var tilfældet med evoCas9, men at opdage allerede udviklede enzymer, der kan virke, giver store fordele.
Samarbejdet med laboratoriet for Computational Metagenomics af Nicola Segata har gjort det muligt for laboratoriet for Molekylær Virologi af Anna Cereseto at kaste lys over en enorm naturreserve af CRISPR-Cas9-systemer, hvorfra man kan trække nye værdifulde værktøjer til redigering af menneskets genom.
"Ved at forhøre en mikrobiom genom-database, som vi har skabt over flere år, opdagede vi et stort antal Cas9 med interessante egenskaber til genomredigering," siger Anna Cereseto og Nicola Segata.
"Vi har opdaget en stor variation af CRISPR-Cas9 i de bakterier, der bebor tarmen. Vi har især identificeret CoCas9 nukleasen, en meget aktiv gruppe af enzymer med en lille molekylær størrelse, omkring tusind aminosyrer, i Collinsella, en bakterieslægt, der ofte findes i menneskets tarme."
"Sekventeringen af hele mikrobiomet ved hjælp af en metagenomisk tilgang, efterfulgt af laboratorierekonstruktionen af de samlede genomer, har ført til identifikation af en stor variation af arter. Opdagelsen af en samling af nye Cas9-nukleaser, herunder CoCas9, gør genomet redigeringsværktøj endnu større," påpeger de.
De konkluderer:"Vanskeligheden ved administration hæmmer stadig udviklingen af terapier til genetiske sygdomme. CoCas9, takket være dens lille størrelse, viser imidlertid potentiale for genterapiapplikationer og er derfor en potentiel kandidat til optimering gennem tekniske tilgange, som fortjener yderligere undersøgelser . Vi arbejder allerede på kliniske udviklingsprojekter."
Flere oplysninger: Eleonora Pedrazzoli et al, CoCas9 er en kompakt nuklease fra det menneskelige mikrobiom til effektiv og præcis genomredigering, Nature Communications (2024). DOI:10.1038/s41467-024-47800-9
Journaloplysninger: Nature Communications
Leveret af University of Trento
 Varme artikler
Varme artikler
-
 Dinosaur-mumie:Forskere mener, at de har fundet en af de bedst bevarede dinosaurer nogensindeKredit:Royal Tyrrell Museum, Drumheller, Canada Forskere i Canada har opdaget dele af, hvad de mener er en fuld dinosaur-mumie, anbragt i en bjergskråning, meddelte University of Reading i Storbrit
Dinosaur-mumie:Forskere mener, at de har fundet en af de bedst bevarede dinosaurer nogensindeKredit:Royal Tyrrell Museum, Drumheller, Canada Forskere i Canada har opdaget dele af, hvad de mener er en fuld dinosaur-mumie, anbragt i en bjergskråning, meddelte University of Reading i Storbrit -
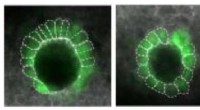 Genetiske instruktioner fra mor satte mønsteret for embryonal udviklingEt organ kaldet Kupffers vesikel, som hjælper med at specificere venstre og højre side af den udviklende fisk, er asymmetrisk formet i et vildtypeembryo (til venstre), men er mere symmetrisk i fravær
Genetiske instruktioner fra mor satte mønsteret for embryonal udviklingEt organ kaldet Kupffers vesikel, som hjælper med at specificere venstre og højre side af den udviklende fisk, er asymmetrisk formet i et vildtypeembryo (til venstre), men er mere symmetrisk i fravær -
 Byafgrøder kan have højere udbytter end konventionelt landbrugBylandbrug kan bruge både grønne områder, som denne fælleshave, og grå rum såsom tage og lodrette vægge til at dyrke mad til byen. Kredit:Roots in the City Community Garden i Liverpool Efterhånden
Byafgrøder kan have højere udbytter end konventionelt landbrugBylandbrug kan bruge både grønne områder, som denne fælleshave, og grå rum såsom tage og lodrette vægge til at dyrke mad til byen. Kredit:Roots in the City Community Garden i Liverpool Efterhånden -
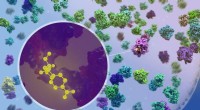 Se antibiotika i aktion inde i en patogen bakterieForskere brugte kryo-elektrontomografi til at visualisere, hvordan antibiotika binder sig til ribosomer inde i bakterier. Kredit:Isabel Romero Calvo/EMBL Hver levende celle er afhængig af proteiner
Se antibiotika i aktion inde i en patogen bakterieForskere brugte kryo-elektrontomografi til at visualisere, hvordan antibiotika binder sig til ribosomer inde i bakterier. Kredit:Isabel Romero Calvo/EMBL Hver levende celle er afhængig af proteiner
- Dyb rumkommunikation via fjerne fotoner
- New York Citys affaldsdilemmaer - og muligheder
- Hvorfor er det tydeligere at se rummet gennem et infrarødt teleskop?
- Kødædere ved, at det at spise andre kødædende kroppe overfører sygdomme
- Sådan fungerer antropologi
- Sådan beregnes arealet af en cirkel med diameter


