Nyt værktøj afkoder komplekse, enkeltcellede genomiske data
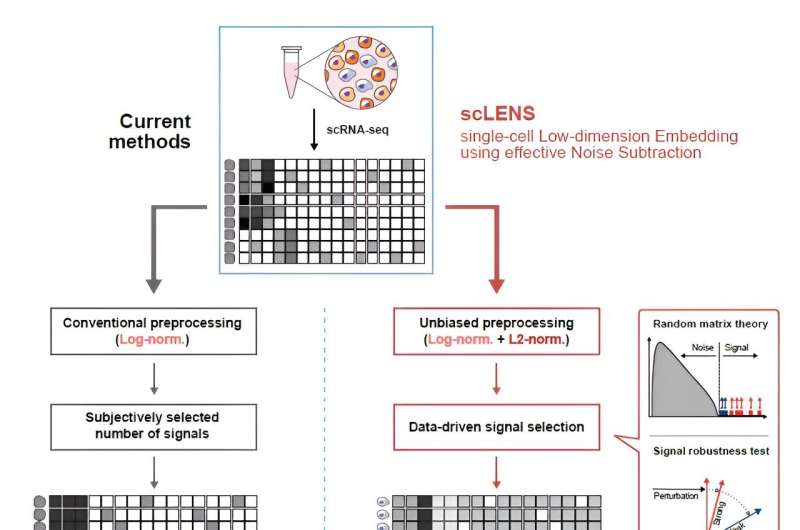
Oplåsning af biologisk information fra komplekse enkeltcellede genomiske data er netop blevet nemmere og mere præcist, takket være det innovative scLENS-værktøj udviklet af Biomedical Mathematics Group inden for IBS Center for Mathematical and Computational Sciences ledet af Chief Investigator Kim Jae Kyoung, som også er professor ved KAIST. Dette repræsenterer et betydeligt spring fremad inden for enkeltcellet transkriptomik.
Forskningen er publiceret i tidsskriftet Nature Communications .
Enkeltcellet genomisk analyse er en avanceret teknik, der måler genekspression på det individuelle celleniveau, og afslører cellulære ændringer og interaktioner, der ikke er observerbare med traditionelle genomiske analysemetoder. Når den anvendes på kræftvæv, kan denne analyse afgrænse sammensætningen af forskellige celletyper i en tumor, give indsigt i, hvordan kræft skrider frem og identificere nøglegener involveret i hvert stadium af progression.
På trods af det enorme potentiale ved enkeltcellet genomisk analyse har det altid været en udfordring at håndtere den enorme mængde data, som den genererer. Mængden af data dækker ekspressionen af titusindvis af gener på tværs af hundreder til tusinder af individuelle celler. Dette resulterer ikke kun i store datasæt, men introducerer også støjrelaterede forvrængninger, som delvist opstår på grund af strømmålingsbegrænsninger.
Den korresponderende forfatter Kim Jae Kyoung fremhævede:"Der er sket et bemærkelsesværdigt fremskridt inden for eksperimentelle teknologier til analyse af enkeltcellede transkriptomer i løbet af det sidste årti. Men på grund af begrænsninger i dataanalysemetoder har der været en kamp for fuldt ud at udnytte værdifulde data opnået gennem omfattende omkostninger og tid."
Forskere har udviklet adskillige analysemetoder gennem årene for at skelne biologiske signaler fra denne støj. Nøjagtigheden af disse metoder har imidlertid været mindre end tilfredsstillende. Et kritisk problem er, at bestemmelse af signal- og støjtærskler ofte afhænger af subjektive beslutninger fra brugerne.
Det nyudviklede scLENS-værktøj udnytter Random Matrix Theory og Signal robusthed test for automatisk at differentiere signaler fra støj uden at stole på subjektivt brugerinput.
Første forfatter Kim Hyun udtalte:"Tidligere måtte brugerne vilkårligt bestemme tærsklen for signal og støj, hvilket kompromitterede reproducerbarheden af analyseresultater og indførte subjektivitet. scLENS eliminerer dette problem ved automatisk at detektere signaler ved kun at bruge den iboende struktur af dataene."
Under udviklingen af scLENS identificerede forskere de grundlæggende årsager til unøjagtigheder i eksisterende analysemetoder. De fandt ud af, at almindeligt anvendte dataforbehandlingsmetoder forvrænger både biologiske signaler og støj. Den nye forbehandlingsmetode, som scLENS tilbyder, er fri for sådanne forvrængninger.
Ved at løse problemer relateret til støjtærskel, bestemt af subjektivt brugervalg og signalforvrængning i konventionel dataforbehandling, overgår scLENS væsentligt eksisterende metoder med hensyn til nøjagtighed. Derudover automatiserer scLENS den besværlige proces med valg af signaldimension, hvilket giver forskere mulighed for at udtrække biologiske signaler bekvemt og automatisk.
Ci Kim tilføjede, "scLENS løser store problemer inden for enkeltcellet transkriptomdataanalyse, hvilket væsentligt forbedrer nøjagtigheden og effektiviteten gennem hele analyseprocessen. Dette er et glimrende eksempel på, hvordan fundamentale matematiske teorier kan drive innovation inden for biovidenskabelig forskning, hvilket giver forskere mulighed for at mere svar hurtigt og præcist på biologiske spørgsmål og afslør livets hemmeligheder, der tidligere var skjult."
Flere oplysninger: Hyun Kim et al., scLENS:datadrevet signaldetektion til unbiased scRNA-seq dataanalyse, Nature Communications (2024). DOI:10.1038/s41467-024-47884-3
Journaloplysninger: Nature Communications
Leveret af Institute for Basic Science
 Varme artikler
Varme artikler
-
 Biodiversitetens rødder:Hvordan proteiner adskiller sig på tværs af arterKredit:Pixabay/CC0 Public Domain For bedre at forstå, hvad der driver biologisk mangfoldighed på Jorden, har forskere historisk set på genetiske forskelle mellem arter. Men dette giver kun en del a
Biodiversitetens rødder:Hvordan proteiner adskiller sig på tværs af arterKredit:Pixabay/CC0 Public Domain For bedre at forstå, hvad der driver biologisk mangfoldighed på Jorden, har forskere historisk set på genetiske forskelle mellem arter. Men dette giver kun en del a -
 Mitokondriel omsætning:Forskere opdager, hvad der får cellebatterier til at løbe tørGrafisk abstrakt. Kredit:Molecular Cell (2022). DOI:10.1016/j.molcel.2022.06.004 Forskere ved University of Toronto har opdaget, hvordan mitokondriel omsætning - en kritisk cellulær funktion - begy
Mitokondriel omsætning:Forskere opdager, hvad der får cellebatterier til at løbe tørGrafisk abstrakt. Kredit:Molecular Cell (2022). DOI:10.1016/j.molcel.2022.06.004 Forskere ved University of Toronto har opdaget, hvordan mitokondriel omsætning - en kritisk cellulær funktion - begy -
 Styrkelse af citronfrugt for bedre at modstå klimaændringerKredit:Asociación RUVID Forskning fra afdelingen for landbrugsvidenskab og den naturlige verden ved Universitat Jaume I i Castellón, Spanien, har identificeret generne inden for citronfrugt, som b
Styrkelse af citronfrugt for bedre at modstå klimaændringerKredit:Asociación RUVID Forskning fra afdelingen for landbrugsvidenskab og den naturlige verden ved Universitat Jaume I i Castellón, Spanien, har identificeret generne inden for citronfrugt, som b -
 Bakterier får modstand fra konkurrenterBakteriekonkurrence i mikroskala:T6SS (grøn, magenta) medieret drab og lysis af konkurrerende bakterier kan føre til DNA-frigivelse (cyan) og efterfølgende genoverførsel. Kredit:Universität Basel
Bakterier får modstand fra konkurrenterBakteriekonkurrence i mikroskala:T6SS (grøn, magenta) medieret drab og lysis af konkurrerende bakterier kan føre til DNA-frigivelse (cyan) og efterfølgende genoverførsel. Kredit:Universität Basel
- Til salg:unikt stykke jord i strategisk arktisk øhav
- Selvhelbredende flydende metal-elastomerer
- Glukoseovervågende kontaktlinse ville have en transparent sensor
- Målrettet tekniske problemer tilstopper butikker med lange kassekøer
- Dobbelts katalysator muliggør høj omdannelse af syngas til flydende carbonhydrider i benzininterva…
- Bliver du virkelig bevidst efter at være halshugget?


