En ny tilgang til at bestemme, hvordan kræftfremkaldende bakterier finder deres mål
Kræftfremkaldende bakterier, såsom Helicobacter pylori og Fusobacterium nucleatum, har evnen til at kolonisere specifikke steder i den menneskelige krop og bidrage til udviklingen af kræft. At forstå de mekanismer, hvorved disse bakterier finder deres mål, er afgørende for at udvikle effektive forebyggelses- og behandlingsstrategier. Her foreslår vi en ny tilgang, der kombinerer avancerede molekylære teknikker og beregningsmodellering for at belyse de molekylære interaktioner og signalveje involveret i bakteriel målretning.
1. Isolering og kultur af bakteriestammer:
- Isoler og dyrk de specifikke kræftfremkaldende bakteriestammer af interesse (f.eks. H. pylori og F. nucleatum).
- Bekræft deres identitet ved hjælp af molekylære metoder såsom polymerasekædereaktion (PCR) eller hel-genom-sekventering.
2. Værtsvævsprøveindsamling:
- Indhent sunde og cancerøse vævsprøver fra berørte individer (f.eks. mavevæv for H. pylori og kolorektalt væv for F. nucleatum).
- Sikre ordentlige etiske overvejelser og informeret samtykke.
3. Molekylær profilering af værtsvæv:
- Udfør transkriptomanalyse (RNA-seq) på både raske og kræftvævsprøver for at identificere differentielt udtrykte gener.
- Analysere ekspressionsmønstrene for gener involveret i celleadhæsion, inflammation og immunrespons.
4. Bakteriel adhæsionsanalyse:
- Samdyrkning af de kræftfremkaldende bakteriestammer med dyrkede værtsceller (f.eks. gastriske epitelceller eller colonocytter).
- Vurder bakteriel adhæsion til værtsceller ved hjælp af mikroskopi og kvantitative assays (f.eks. krystalviolet farvning).
5. Identifikation af bakterielle adhæsionsfaktorer:
- Isoler og karakteriser de bakterielle overfladeproteiner eller molekyler, der er ansvarlige for adhæsion til værtsceller.
- Anvend teknikker som proteomik og immunfluorescensfarvning til at identificere specifikke adhæsiner.
6. Computational Modeling and Docking Studies:
- Udfør molekylære docking-undersøgelser for at forudsige interaktionerne mellem bakterielle adhæsiner og potentielle værtscellereceptorer.
- Brug beregningsværktøjer til at simulere bindingsaffiniteter og konformationelle ændringer under adhæsionsprocessen.
7. Funktionel validering:
- Design og udfør eksperimenter for at validere de forudsagte interaktioner.
- Brug stedstyret mutagenese eller blokerende antistoffer til at vurdere virkningen af specifikke adhæsiner på bakteriel målretning og kolonisering.
8. Analyse af signalveje:
- Undersøg de nedstrøms signalveje aktiveret ved bakteriel adhæsion til værtsceller.
- Analysere ekspressionen af nøglesignalmolekyler og transkriptionsfaktorer involveret i inflammation og kræftudvikling.
9. In Vivo dyremodeller:
- Etablere dyremodeller (f.eks. musemodeller) for at studere bakteriel kolonisering og tumorudvikling i et kontrolleret miljø.
- Vurdere bakteriernes målretningseffektivitet og kræftfremkaldende potentiale in vivo.
10. Dataintegration og systembiologi:
- Integrer de eksperimentelle data fra molekylær profilering, adhæsionsassays, beregningsmodellering og dyreforsøg.
- Udvikle modeller på systemniveau til at forstå de komplekse interaktioner mellem de kræftfremkaldende bakterier og værtsmiljøet.
Ved at kombinere disse tilgange sigter vi mod at give en omfattende forståelse af, hvordan kræftfremkaldende bakterier finder deres mål. Denne viden vil bidrage til udviklingen af nye terapeutiske strategier til at hæmme bakteriel kolonisering og reducere risikoen for kræftudvikling forbundet med disse bakterier.
 Varme artikler
Varme artikler
-
 Hvorfor stinker stinkplanten?Burde de mennesker ikke holde næsen? Denne sjældne blomstrende ligblomst er en af omkring et dusin eller har blomstret i USA i det sidste århundrede. Se flere ligblomstbilleder. David McNew/Newsmake
Hvorfor stinker stinkplanten?Burde de mennesker ikke holde næsen? Denne sjældne blomstrende ligblomst er en af omkring et dusin eller har blomstret i USA i det sidste århundrede. Se flere ligblomstbilleder. David McNew/Newsmake -
 Nye fund tydeliggør thyroids rolle i pattedyrs sæsonmæssige ændringerKredit:Mary Ann Liebert, Inc., forlag Forskere har nu en bedre forståelse af den rolle, som skjoldbruskkirtelhormoner, det væv, der producerer dem, og de biokemiske veje, som de virker på, har til
Nye fund tydeliggør thyroids rolle i pattedyrs sæsonmæssige ændringerKredit:Mary Ann Liebert, Inc., forlag Forskere har nu en bedre forståelse af den rolle, som skjoldbruskkirtelhormoner, det væv, der producerer dem, og de biokemiske veje, som de virker på, har til -
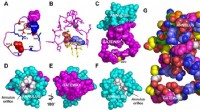 Undersøgelse foreslår ny mekanisme til lipidtransporterStrukturelle detaljer af gateway/ring-komplekset. A, B Rygraden i gatewayen (magenta). A De basiske (blå, stick) og sure (røde, stick) aminosyrerester af gatewayen (rest 564-592, magenta) fra ABCA1-st
Undersøgelse foreslår ny mekanisme til lipidtransporterStrukturelle detaljer af gateway/ring-komplekset. A, B Rygraden i gatewayen (magenta). A De basiske (blå, stick) og sure (røde, stick) aminosyrerester af gatewayen (rest 564-592, magenta) fra ABCA1-st -
 At handle eller ikke at handle? At bryde elfenbenslåsenElefant nær Kruger National Park. Kredit:Duan Biggs Debatten om, hvorvidt lovlig handel med elfenben skal have lov til at finansiere bevarelse af elefanter, eller helt forbudt at stoppe krybskytte
At handle eller ikke at handle? At bryde elfenbenslåsenElefant nær Kruger National Park. Kredit:Duan Biggs Debatten om, hvorvidt lovlig handel med elfenben skal have lov til at finansiere bevarelse af elefanter, eller helt forbudt at stoppe krybskytte
- Forskelle mellem nord- og sydvendt skråninger
- Hvordan at studere (robot) duenavigation ændrede min mening om deres intellekt
- Kan vi fortælle nogens kulturelle gruppe fra den måde, de griner på?
- Dyrkning af HCA -krystaller
- Hvad driver havniveaustigningen? Rapporten advarer om en fods stigning inden for tre årtier og hypp…
- Forskere opdager, at nøglen til sikrere batterier ligger på overfladen


