At forstå, hvordan DNA reparerer sig selv, kan føre til bedre kræftbehandling
DNA, livets plan, er modtagelig for skader fra både interne og eksterne kilder, såsom UV-stråling, frie radikaler og kemoterapi. For at bevare sin integritet og forhindre mutationer, der kan føre til kræft og andre sygdomme, har celler udviklet sofistikerede DNA-reparationsmekanismer. Ved at forstå disse selvreparationsprocesser kan videnskabsmænd udvikle mere effektive og målrettede kræftbehandlinger.
Typer af DNA-reparationsmekanismer:
Der er adskillige DNA-reparationsmekanismer, som hver især er ansvarlige for at håndtere specifikke typer skader. Her er to nøgleveje involveret i DNA-reparation:
1. Base Excision Repair (BER):
BER retter sig specifikt mod og reparerer beskadigede eller modificerede individuelle baser i DNA-molekylet. Denne mekanisme er afgørende for at korrigere almindelige kemiske ændringer forårsaget af miljøfaktorer og cellulære processer.
2. Nukleotidudskæringsreparation (NER):
NER er ansvarlig for at fjerne større dele af DNA, der indeholder beskadigede nukleotider, herunder omfangsrige læsioner induceret af UV-stråling eller visse kemiske midler.
Målretning af DNA-reparation i kræftbehandling:
Mens DNA-reparation er afgørende for celleoverlevelse, udviser kræftceller ofte defekter eller overaktivering i deres reparationsveje. Dette kan gøre dem modstandsdygtige over for behandlinger, der sigter mod at forårsage DNA-skader. Ved at manipulere eller udnytte DNA-reparationsmekanismer kan nye terapeutiske strategier designes til at øge effektiviteten af kræftbehandlinger og overvinde lægemiddelresistens:
en. Forbedring af kemoterapirespons:
Ved at hæmme eller modulere visse DNA-reparationsveje kan cancerceller gøres mere modtagelige for DNA-skadelige kemoterapeutiske midler, hvilket øger behandlingens effektivitet.
b. Målretning af reparationsproteininteraktioner:
Målretning af proteiner involveret i DNA-reparationskomplekser eller forstyrrende interaktioner inden for disse komplekser er dukket op som en lovende strategi til sensibilisering af cancerceller over for terapier.
c. Syntetisk dødelighedstilgang:
Syntetiske dødelige interaktioner opstår, når hæmningen af to separate gener eller veje fører til celledød. Ved at målrette specifikke DNA-reparationsveje sammen med andre sårbarheder i kræftceller, kan syntetiske dødelige strategier anvendes til selektivt at inducere celledød i kræftceller.
d. Forbedring af immunterapi:
DNA-reparationsmangler kan føre til øgede mutationsrater og generering af unormale proteiner, hvilket gør kræftceller mere synlige for immunsystemet. Stimulering af antitumor-immunresponser ved at modulere DNA-reparationsveje kan forbedre effektiviteten af immunterapier.
Udfordringer og fremtidige retninger:
Mens målretning mod DNA-reparationsmekanismer rummer et enormt potentiale for kræftbehandling, skal flere udfordringer overvindes:
en. Kompleksitet og redundans:
Den mangefacetterede natur af DNA-reparation og tilstedeværelsen af flere overlappende veje kan komplicere terapeutiske strategier.
b. Toksicitet og modstand:
Hæmning af DNA-reparationsveje kan føre til systemiske toksiciteter, og cancerceller kan udvikle resistensmekanismer over tid.
c. Præcision og specificitet:
Design af terapier, der selektivt retter sig mod kræftceller og samtidig skåner sundt væv, er fortsat et kritisk problem.
På trods af disse udfordringer fortsætter igangværende forskning med at optrevle de indviklede mekanismer for DNA-reparation, hvilket gør fremskridt i retning af at udvikle innovative kræftbehandlinger, der udnytter disse sårbarheder og forbedrer patienternes resultater. Ved præcist at manipulere DNA-reparationsveje lover fremtiden for kræftbehandling mere effektive og personlige terapier, der er skræddersyet til individuelle patientbehov.
 Varme artikler
Varme artikler
-
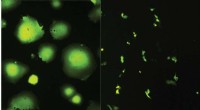 Målretning mod et enkelt protein kan behandle en bred vifte af viraMæslingevirus undertrykkes (til højre), når et nøgleprotein, SPCA1, er nedsat i værten. Kredit:Hans-Heinrich Hoffmann De fleste lægemidler, der bekæmper vira, er designet til at målrette individue
Målretning mod et enkelt protein kan behandle en bred vifte af viraMæslingevirus undertrykkes (til højre), når et nøgleprotein, SPCA1, er nedsat i værten. Kredit:Hans-Heinrich Hoffmann De fleste lægemidler, der bekæmper vira, er designet til at målrette individue -
 Simulering af hvalesex med kadaverdele giver indsigt i marin kopulationForm korrespondance af mandlige og kvindelige kønsorganer. Silikone vaginal endocast er på linje med den oppustede penisspids i kønsmodne:(a) har Q5 marsvin (Phocoena phocoena), b) almindelige flasken
Simulering af hvalesex med kadaverdele giver indsigt i marin kopulationForm korrespondance af mandlige og kvindelige kønsorganer. Silikone vaginal endocast er på linje med den oppustede penisspids i kønsmodne:(a) har Q5 marsvin (Phocoena phocoena), b) almindelige flasken -
 Hvordan udvikler genomer sig mellem arter? Team udforsker 3D-strukturens nøglerolle i mandlige køn…Kredit:CC0 Public Domain En undersøgelse ledet af forskere ved Universitat Autònoma de Barcelona (UAB) og University of Kent afslører, hvordan genomets tredimensionelle struktur af mandlige kønscel
Hvordan udvikler genomer sig mellem arter? Team udforsker 3D-strukturens nøglerolle i mandlige køn…Kredit:CC0 Public Domain En undersøgelse ledet af forskere ved Universitat Autònoma de Barcelona (UAB) og University of Kent afslører, hvordan genomets tredimensionelle struktur af mandlige kønscel -
 Hvordan gendannelse af overfyldte skove kan give flere forskellige fordeleSkovgenopretningsprojekter som det ved French Meadows i Tahoe National Forest (ovenfor) hjælper med at reducere naturbrandens sværhedsgrad og tilbyder forbedrede økosystemtjenester, hvilket resulterer
Hvordan gendannelse af overfyldte skove kan give flere forskellige fordeleSkovgenopretningsprojekter som det ved French Meadows i Tahoe National Forest (ovenfor) hjælper med at reducere naturbrandens sværhedsgrad og tilbyder forbedrede økosystemtjenester, hvilket resulterer
- Genopvågnet gejser forudsiger ikke Yellowstone vulkanudbrud, viser undersøgelse
- I rummet, USA ser en rival i Kina
- Nanopartikler af risklid viser lovende som et overkommeligt og målrettet anticancermiddel
- Materialeforskere skaber stofalternativer til batterier til bærbare enheder
- SmallGEOs første flyvning når kredsløb
- Sådan finder du acceleration med hastighed & Distance


