Hvad er en diatomisk reaktion?
Diatomiske reaktioner kan enten være eksoterme eller endoterme. Ved eksoterme reaktioner frigives energi, når bindingerne mellem atomerne eller molekylerne dannes. Ved endoterme reaktioner absorberes energi, når bindingerne brydes.
Et af de mest almindelige eksempler på en diatomisk reaktion er forbrændingen af brintgas og oxygengas til dannelse af vanddamp. I denne reaktion reagerer to brintatomer og et oxygenatom og danner to vandmolekyler, der frigiver energi i form af varme og lys.
Et andet eksempel på en diatomisk reaktion er reaktionen mellem carbonmonoxid og oxygengas til dannelse af carbondioxid. I denne reaktion reagerer et kuliltemolekyle og to oxygenmolekyler og danner to kuldioxidmolekyler, der frigiver energi i form af varme.
Diatomiske reaktioner er også vigtige i studiet af atmosfærisk kemi. For eksempel er reaktionen mellem nitrogengas og oxygengas til dannelse af nitrogenoxider en diatomisk reaktion, der bidrager til dannelsen af smog.
Diatomiske reaktioner er en grundlæggende del af kemien og spiller en rolle i mange forskellige processer, lige fra forbrænding af brændstoffer til dannelsen af atmosfæriske forurenende stoffer.
Sidste artikelHvad er et udtryk for lov (kkonstant)?
Næste artikelHvad er hybridisering af xeo2?
 Varme artikler
Varme artikler
-
 Beyond AlphaFold:AI udmærker sig ved at skabe nye proteinerProteiner designet med et ultrahurtigt softwareværktøj kaldet ProteinMPNN var meget mere tilbøjelige til at folde op efter hensigten. Kredit:Ian Haydon, UW Medicine Institute for Protein Design I l
Beyond AlphaFold:AI udmærker sig ved at skabe nye proteinerProteiner designet med et ultrahurtigt softwareværktøj kaldet ProteinMPNN var meget mere tilbøjelige til at folde op efter hensigten. Kredit:Ian Haydon, UW Medicine Institute for Protein Design I l -
 Fuglenes flyvehastighed er mere kompleks end tidligere antagetKredit:CC0 Public Domain Fuglenes flyvehastighed er mere kompleks, end forskning tidligere har formået at vise. I en ny undersøgelse fra Lunds Universitet i Sverige, forskere har fundet ud af, at
Fuglenes flyvehastighed er mere kompleks end tidligere antagetKredit:CC0 Public Domain Fuglenes flyvehastighed er mere kompleks, end forskning tidligere har formået at vise. I en ny undersøgelse fra Lunds Universitet i Sverige, forskere har fundet ud af, at -
 Mere end 38 procent af den neotropiske papegøjebestand på det amerikanske kontinent er truet af me…Fangst til kæledyrshandel har været en af de største trusler for bevarelsen af vilde papegøjer. Kredit:Igor Berkunsky Mere end 38 procent af den neotropiske papegøjebestand på det amerikanske
Mere end 38 procent af den neotropiske papegøjebestand på det amerikanske kontinent er truet af me…Fangst til kæledyrshandel har været en af de største trusler for bevarelsen af vilde papegøjer. Kredit:Igor Berkunsky Mere end 38 procent af den neotropiske papegøjebestand på det amerikanske -
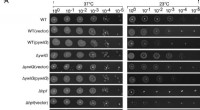 Undersøgelse identificerer mekanismer, der fremmer bakteriel overlevelseInaktivering af ywlG undertrykker kuldefølsomheden af en Δhpf-nul mutant på en mediumafhængig måde. Komplementering med plasmid-kodet ywlG og hpf bekræftede den YwlG-medierede suppression og HPF-afh
Undersøgelse identificerer mekanismer, der fremmer bakteriel overlevelseInaktivering af ywlG undertrykker kuldefølsomheden af en Δhpf-nul mutant på en mediumafhængig måde. Komplementering med plasmid-kodet ywlG og hpf bekræftede den YwlG-medierede suppression og HPF-afh
- Første 3D-printede protonledende membran baner vej for skræddersyede energilagringsenheder
- Et nyt værktøj til at tænde og slukke for proteiner
- Hvad er nanoskala?
- Mobilteknologi går til hundene ... bogstaveligt talt
- Skovbrande stiger, da undersøgelse advarer om fare for luftkvaliteten
- Borgervidenskabsmænd inviteret til at deltage i søgen efter nye verdener


