Hvad er de vigtigste træk ved syrer?
Kemiske egenskaber:
* smag: Syrer har en sur smag. (Forsigtig:Smag aldrig et ukendt stof!)
* reaktion med baser: Syrer reagerer med baser for at danne salt og vand. Dette kaldes neutralisering.
* reaktion med metaller: Mange syrer reagerer med metaller for at producere brintgas og et salt.
* ph: Syrer har en pH -værdi mindre end 7.
* Konduktivitet: Syrer udfører elektricitet, når de opløses i vand.
* tilstedeværelse af brintioner: Syrer frigiver brintioner (H+), når de opløstes i vand. Det er det, der gør dem sure.
Fysiske egenskaber:
* udseende: Syrer kan være væsker, faste stoffer eller gasser.
* opløselighed: Mange syrer er opløselige i vand.
Nøglekoncepter:
* Stærke syrer: Disse ioniseres fuldstændigt i vand og frigiver en høj koncentration af brintioner. Eksempler inkluderer saltsyre (HCI), svovlsyre (H₂so₄) og salpetersyre (HNO₃).
* svage syrer: Disse ioniserer kun delvist i vand og frigiver en lavere koncentration af brintioner. Eksempler inkluderer eddikesyre (ch₃cooh), citronsyre og kulsyre (H₂co₃).
Vigtig note: Syrer kan være ætsende og farlige. Håndter dem altid med omhu og følg sikkerhedsretningslinjerne.
 Varme artikler
Varme artikler
-
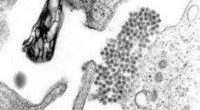 Myg er mere tilbøjelige til at overføre dengue-virus i varmt vejrEt TEM-mikrografi, der viser dengue-virusvirioner (klyngen af mørke prikker nær midten). Billede:CDC Dengue-virus vokser og spreder sig hurtigere i myg ved højere temperaturer, men går langsomme
Myg er mere tilbøjelige til at overføre dengue-virus i varmt vejrEt TEM-mikrografi, der viser dengue-virusvirioner (klyngen af mørke prikker nær midten). Billede:CDC Dengue-virus vokser og spreder sig hurtigere i myg ved højere temperaturer, men går langsomme -
 På Mexicos caribiske kyst vokser bjerge af tangArbejdere, der blev ansat af beboere, fjerner sargassum-tang fra Soliman-bugten, nord for Tulum, Quintana Roo-staten, Mexico, onsdag den 3. august 2022. Kredit:AP Photo/Eduardo Verdugo At skrabe de
På Mexicos caribiske kyst vokser bjerge af tangArbejdere, der blev ansat af beboere, fjerner sargassum-tang fra Soliman-bugten, nord for Tulum, Quintana Roo-staten, Mexico, onsdag den 3. august 2022. Kredit:AP Photo/Eduardo Verdugo At skrabe de -
 Sådan fungerer naturligt udvalgHummingbird Image Gallery Rufous kolibri ( Selasphorus rufus ). En kolibrier lange næb og tunge udviklede sig til at lade fuglen nå dybt ind i en blomst til nektar. Se mere kolibrier billede
Sådan fungerer naturligt udvalgHummingbird Image Gallery Rufous kolibri ( Selasphorus rufus ). En kolibrier lange næb og tunge udviklede sig til at lade fuglen nå dybt ind i en blomst til nektar. Se mere kolibrier billede -
 Hvorfor krydsede elefanten vejen? I Malaysia, de forsøger at finde svaretKredit:University of Nottingham Kroppen af en elefantkalv ligger på siden af en fjerntliggende motorvej i den nordlige del af Peninsular Malaysia-øst-vest motorvejen flankeres af to tilflugtss
Hvorfor krydsede elefanten vejen? I Malaysia, de forsøger at finde svaretKredit:University of Nottingham Kroppen af en elefantkalv ligger på siden af en fjerntliggende motorvej i den nordlige del af Peninsular Malaysia-øst-vest motorvejen flankeres af to tilflugtss


