Banebrydende lab-on-a-chip opdager kræft hurtigere, billigere og mindre invasivt
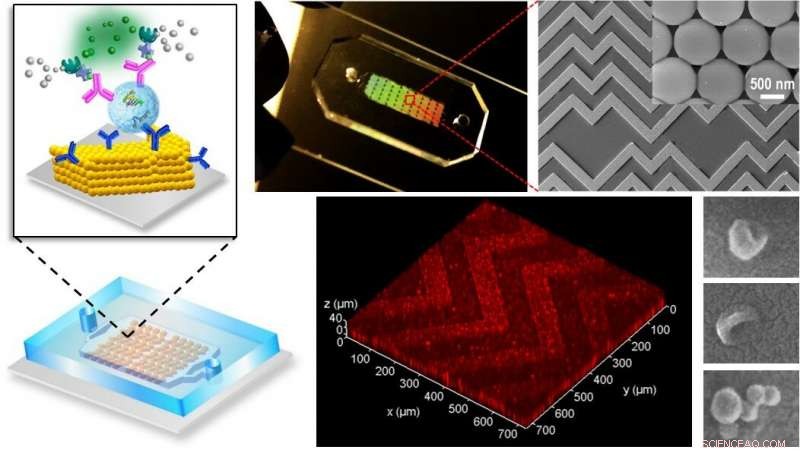
Den nye lab-on-a-chips nøgleinnovation er en 3D nanoingeniørmetode, der blander og sanser biologiske elementer baseret på et sildebensmønster, der almindeligvis findes i naturen, skubbe exosomer i kontakt med chippens føleoverflade meget mere effektivt i en proces kaldet "masseoverførsel". Kredit:KU / University of Kansas
En ny ultrafølsom diagnostisk enhed opfundet af forskere ved University of Kansas, University of Kansas Cancer Center og KU Medical Center kunne tillade læger at opdage kræft hurtigt fra en dråbe blod eller plasma, fører til hurtigere interventioner og bedre resultater for patienterne.
"lab-on-a-chip" til "væskebiopsi"-analyse, rapporteret i dag i Natur biomedicinsk teknik , detekterer exosomer - små pakker af biologisk information produceret af tumorceller for at stimulere tumorvækst eller metastasere.
"Historisk set, folk troede, at exosomer var som 'affaldsposer', som celler kunne bruge til at dumpe uønsket cellulært indhold, " sagde hovedforfatter Yong Zeng, Docking Family Scholar og lektor i kemi ved KU. "Men i det sidste årti, videnskabsmænd indså, at de var ret nyttige til at sende beskeder til modtagerceller og kommunikere molekylær information, der er vigtig i mange biologiske funktioner. I bund og grund, tumorer udsender exosomer, der pakker aktive molekyler, der afspejler de biologiske egenskaber i forældrecellerne. Mens alle celler producerer exosomer, tumorceller er virkelig aktive sammenlignet med normale celler."
Den nye lab-on-a-chip nøgleinnovation er en 3-D nanoingeniørmetode, der blander og sanser biologiske elementer baseret på et sildebensmønster, der almindeligvis findes i naturen, skubbe exosomer i kontakt med chippens føleoverflade meget mere effektivt i en proces kaldet "masseoverførsel".
"Folk har udviklet smarte ideer til at forbedre masseoverførsel i mikroskalakanaler, men når partikler bevæger sig tættere på sensoroverfladen, de er adskilt af et lille mellemrum af væske, der skaber stigende hydrodynamisk modstand, " sagde Zeng. "Her, vi udviklede en 3-D nanoporøs sildebensstruktur, der kan dræne væsken i dette hul for at bringe partiklerne i hård kontakt med overfladen, hvor sonder kan genkende og fange dem."
Zeng sammenlignede chippens nanoporer med en million små køkkenvaske:"Hvis du har en vask fyldt med vand og mange bolde, der flyder på overfladen, hvordan får du alle kuglerne i kontakt med bunden af vasken, hvor sensorer kan analysere dem? Den nemmeste måde er at dræne vandet."
At udvikle og teste den banebrydende mikrofluidisk enhed, Zeng gik sammen med en tumor-biomarkørekspert og KU Cancer Centers vicedirektør Andrew Godwin ved KU Medical Centers afdeling for patologi og laboratoriemedicin, samt kandidatstuderende Ashley Tetlow i Godwins Biomarker Discovery Lab. Samarbejdspartnerne testede chippens design ved hjælp af kliniske prøver fra ovariecancerpatienter, at finde chippen kunne påvise tilstedeværelsen af kræft i en minimal mængde plasma.
"Vores samarbejdsundersøgelser fortsætter med at bære frugt og fremme et område, der er afgørende inden for kræftforskning og patientbehandling - nemlig, innovative værktøjer til tidlig opdagelse, " sagde Godwin, der fungerer som kanslerens fornemme formand og professor i biomedicinske videnskaber og professor og direktør for molekylær onkologi, patologi og laboratoriemedicin på KU Lægecenter. "Dette studieområde er især vigtigt for kræftformer såsom æggestokke, da langt de fleste kvinder er diagnosticeret på et fremskredent stadium, når desværre, sygdommen er for det meste uhelbredelig."
Hvad mere er, de nye mikrofluidchips udviklet på KU ville være billigere og nemmere at lave end sammenlignelige designs, giver mulighed for bredere og mindre omkostningskrævende test for patienter.
"Det, vi skabte her, er en 3-D nanomønstermetode uden behov for noget fancy nanofabrikationsudstyr - en bachelor eller endda en gymnasieelev kan gøre det i mit laboratorium, " sagde Zeng. "Dette er så enkelt og billigt, at det har et stort potentiale til at omsætte til kliniske omgivelser. Vi har samarbejdet med Dr. Godwin og andre forskningslaboratorier på KU Cancer Center og afdelingen for molekylær biovidenskab for yderligere at udforske teknologiens translationelle anvendelser."
Ifølge Zeng, med mikrofluidchippens design nu bevist ved brug af ovariecancer som model, chippen kan være nyttig til at opdage en lang række andre sygdomme.
"Nu, vi ser på cellekulturmodeller, dyremodeller, og også kliniske patientprøver, så vi laver virkelig noget translationel forskning for at flytte enheden fra laboratoriemiljøet til flere kliniske applikationer, " sagde han. "Næsten alle pattedyrceller frigiver exosomer, så anvendelsen er ikke kun begrænset til kræft i æggestokkene eller en hvilken som helst type kræft. Vi arbejder med folk for at se på neurodegenerative sygdomme, bryst- og tyktarmskræft, for eksempel."
På KU's Lawrence campus, Zeng arbejdede med et team, herunder postdoc Peng Zhang, kandidatstuderende Xin Zhou i Institut for Kemi, samt Mei He, KU adjunkt i kemi og kemiteknik.
Denne forskning blev støttet af tilskud fra National Institutes of Health, herunder en fælles R21 (CA1806846) og en R33 (CA214333) bevilling mellem Zeng og Godwin og KU Cancer Centers Biospecimen Repository Core Facility, finansieret delvist af et National Cancer Institute Cancer Center Support Grant (P30 CA168524).
 Varme artikler
Varme artikler
-
 Moodys:AT&T laver en bedømmelsesfejl i deres HBO Max-priserKredit:CC0 Public Domain AT&Ts streamingtjeneste, HBO Max, har endnu ikke debuteret, men kreditbureauet Moodys Investors Service forudsiger allerede, at kunder kan få klistermærkechok. I et forsk
Moodys:AT&T laver en bedømmelsesfejl i deres HBO Max-priserKredit:CC0 Public Domain AT&Ts streamingtjeneste, HBO Max, har endnu ikke debuteret, men kreditbureauet Moodys Investors Service forudsiger allerede, at kunder kan få klistermærkechok. I et forsk -
 Forebyggelse af cybersikkerhedsangreb ligger i strategiske, tredjepartsinvesteringer, undersøgelse …Kredit:CC0 Public Domain Virksomheder, der er interesseret i at beskytte sig selv og deres kunder mod cyberangreb, skal investere i sig selv og de leverandører, der håndterer deres data, ifølge ny
Forebyggelse af cybersikkerhedsangreb ligger i strategiske, tredjepartsinvesteringer, undersøgelse …Kredit:CC0 Public Domain Virksomheder, der er interesseret i at beskytte sig selv og deres kunder mod cyberangreb, skal investere i sig selv og de leverandører, der håndterer deres data, ifølge ny -
 Apple løser FaceTime-fejl, der tillader aflytningI denne 30. okt. 2018, fil foto Apples nye MacBook Air-computere vises under virksomhedens fremvisning af nye produkter i Brooklyn-bydelen New York. Apple Inc. melder indtjening tirsdag d. 29. januar,
Apple løser FaceTime-fejl, der tillader aflytningI denne 30. okt. 2018, fil foto Apples nye MacBook Air-computere vises under virksomhedens fremvisning af nye produkter i Brooklyn-bydelen New York. Apple Inc. melder indtjening tirsdag d. 29. januar, -
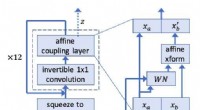 WaveGlow:Et flow-baseret generativt netværk til at syntetisere taleWaveGlow netværk. Kredit:Prenger, Valle, og Catanzaro. Et team af forskere ved NVIDIA har for nylig udviklet WaveGlow, et flow-baseret netværk, der kan generere tale af høj kvalitet fra melspektro
WaveGlow:Et flow-baseret generativt netværk til at syntetisere taleWaveGlow netværk. Kredit:Prenger, Valle, og Catanzaro. Et team af forskere ved NVIDIA har for nylig udviklet WaveGlow, et flow-baseret netværk, der kan generere tale af høj kvalitet fra melspektro
- Intent Lab Digital Satisfaction Index afslører et stejlt fald i forbrugernes tillid til internettet
- Sådan beregnes volumen fra centimeter
- Vedvarende energi kan redde den naturlige verden, men hvis du ikke var forsigtig, det vil også gør…
- Forskere opdager, hvordan en nanokatalysator fungerer på atomniveau
- Ny nanopartikelteknologi udviklet til at behandle aggressiv kræft i skjoldbruskkirtlen
- Sådan fungerer F-15'erne


