Forskere finder en cellulær backup-plan for at holde jernniveauet helt rigtigt
Jern er afgørende for cellernes funktion, men overskydende jern kan beskadige celler. Derfor, celler har sofistikerede molekylære mekanismer til konstant at fornemme og justere jernniveauer. Forstyrrelser i cellulær jernmetabolisme påvirker, efter nogle skøn, mere end en tredjedel af verdens befolkning. Ud over velkendte lidelser som anæmi, forårsaget af generelt utilstrækkelige niveauer af jern i den menneskelige krop, jernmangel kan forringe hjernefunktionen hos de unge og reducere muskelstyrken hos voksne. Jern kan være dysreguleret på niveauet af individuelle celler i neurologiske lidelser såsom Parkinsons sygdom, og forstyrret jernmetabolisme bidrager til medfødte tilstande såsom Friedrichs ataksi.
Forskere i Nutritional Sciences-afdelingen ved University of Wisconsin har afsløret en ny forbindelse i netværket af checks and balances, der ligger til grund for cellulær jernregulering. Forskningen vil blive offentliggjort i 22. september -udgaven af Journal of Biological Chemistry .
Når jernniveauet i menneskelige og andre pattedyrsceller er lave, jern regulerende proteiner, eller IRP'er, spring i aktion. IRP'er forhindrer jern, der kommer ind i celler, i at blive opbevaret forkert, lader cellen bruge jern til at producere essentielle jernholdige proteiner. Når der er overskydende jern, IRP'er er inaktive, hvilket fører til øget jernlagring og derved sænke dets potentielle toksicitet og reservere det til, når jerntilgængeligheden er reduceret. For meget eller for lidt IRP-aktivitet kan være farligt for celler.
Richard Eisensteins forskningsgruppe ved University of Wisconsin undersøger, hvad der styrer IRP'ers aktivitet. I årtier, Det er blevet antaget, at den vigtigste metode, hvormed IRP-1 inaktiveres, involverer essentielle forbindelser kaldet jern-svovlklynger. Når der er nok jern i cellen, en jern-svovl-klynge indsættes i IRP-1, inaktivere den. Dermed, aktiveringen eller undertrykkelsen af IRP-1 er direkte relateret til, hvor meget jern der er tilgængeligt i cellen til at producere jern-svovl-klynger.
Imidlertid, der var nogle beviser for en anden metode, hvormed IRP-1 kunne stoppes, når det ikke var nødvendigt:nemlig, at et protein kaldet FBXL5 kunne tilføje molekylære tags til IRP-1 for at fortælle cellen om at nedbryde proteinet helt.
"Ideen om, at IRP1 også er reguleret af proteinnedbrydning, var kontroversiel, da den først blev opdaget af andre, " sagde Eisenstein. "Der har været en tro på, at IRP1 virkelig blev reguleret af denne jern-svovl-klyngemekanisme, og at proteinnedbrydningsmekanismen ikke var så vigtig."
For at teste, om dette var tilfældet, Eisensteins hold udførte eksperimenter, hvor de undertrykte produktionen af jern-svovlklynger. Selv når produktionen af jern-svovlklynger blev reduceret, IRP-1-aktivitet kunne stadig undertrykkes. Holdet bekræftede, at dette faktisk skyldtes aktiviteten af FBXL5. Dette understøttede ideen om, at nedbrydning af proteiner var en backup-mekanisme, der reducerede IRP-1-virkning i celler med højt jern.
Resultaterne har betydning for forståelsen af, hvordan jern opfattes, bruges og reguleres i forskellige væv. Forskellige væv har forskellige iltniveauer, men jern-svovl-klyngeproduktionssystemet fungerer bedst ved lav ilt, mens FBXL5 fungerer bedst ved høj ilt. Derfor, disse to systemer kan afveje at tage føringen i at kontrollere IRP-1 i forskellige dele af kroppen. Fordi jern-svovlklynger og FBXL5 spiller mange forskellige vigtige roller i cellevækst, denne balance mellem disse funktioner kan hjælpe forskellige typer celler med at kontrollere, hvordan de bruger jern.
"Sygdomme i jernmetabolisme forårsaget af diæt eller af genetiske forstyrrelser er store folkesundhedsproblemer, " sagde Eisenstein. "For at bekæmpe sådanne sygdomme og udvikle effektive behandlinger til dem, der er ramt af dem, det er vigtigt at forstå jernsansende og jernregulerende veje."
Sidste artikelForskere udvikler forfalskede sprit-detektionsanordninger
Næste artikelLipidvesikler erstatter blod i ny bakterietest
 Varme artikler
Varme artikler
-
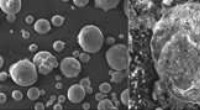 En hårdere ledende keramik til lavere omkostningerScanningselektronmikrofotografier, der viser (venstre mod højre) de rå Ti-partikler, de fladtrykte Ti-partikler efter formaling, og det endelige sintrede Al 2 O 3 -TiN ledende komposit. Kredit:W.
En hårdere ledende keramik til lavere omkostningerScanningselektronmikrofotografier, der viser (venstre mod højre) de rå Ti-partikler, de fladtrykte Ti-partikler efter formaling, og det endelige sintrede Al 2 O 3 -TiN ledende komposit. Kredit:W. -
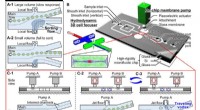 Banebrydende oprensning af fossilt pollen ved hjælp af en ny storpartikel-on-chip sortererKonceptuelle billeder af det foreslåede on-chip sorteringssystem for store partikler baseret på spatiotemporalt genererede rejsehvirvler. (A) Konceptuelle billeder af konventionel partikelsortering på
Banebrydende oprensning af fossilt pollen ved hjælp af en ny storpartikel-on-chip sortererKonceptuelle billeder af det foreslåede on-chip sorteringssystem for store partikler baseret på spatiotemporalt genererede rejsehvirvler. (A) Konceptuelle billeder af konventionel partikelsortering på -
 Forskere udvikler molekylær kode for melanin-lignende materialerPolymere pigmenter blev fremstillet ved guidet oxidation af peptidsamlinger. Kredit:Matej Vakula, NYC Forskere har længe vidst, at melanin - de pigmenter, der giver farve til huden, hår og øjne -
Forskere udvikler molekylær kode for melanin-lignende materialerPolymere pigmenter blev fremstillet ved guidet oxidation af peptidsamlinger. Kredit:Matej Vakula, NYC Forskere har længe vidst, at melanin - de pigmenter, der giver farve til huden, hår og øjne - -
 Afslører strukturen af et uhåndgribeligt kvalitetskontrolenzymFigur 1:Illustration, der viser den konformationelle fleksibilitet af UGGT og dets evne til at omspænde klientproteiner af forskellig størrelse. Kredit:Diamond Light Source Strukturen af det kri
Afslører strukturen af et uhåndgribeligt kvalitetskontrolenzymFigur 1:Illustration, der viser den konformationelle fleksibilitet af UGGT og dets evne til at omspænde klientproteiner af forskellig størrelse. Kredit:Diamond Light Source Strukturen af det kri
- Gennemsigtig arkitektur
- CyLab-forskere foreslår nye regler for retfærdighed på internettet
- Den femte kvartet:Spændt neonfund kan afsløre stjernekvaliteter
- Fakta om den amerikanske solformørkelse den 21. august
- En ny teknik gør det muligt for forskere at oprette rigtige systemkartografiske kort i forskellige …
- Skal forældre hjælpe deres børn med lektier?


