Alkoholer som kulstofradikale forstadier
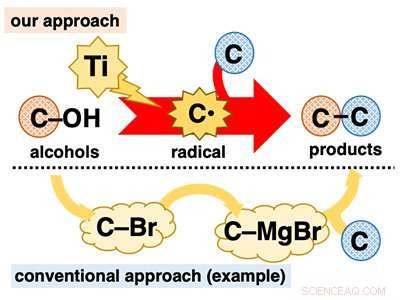
Direkte brug af alkoholer til C-C bindingsdannelsesreaktioner. Kredit:Kanazawa University
Alkoholer spiller en afgørende rolle i organisk syntese, fordi de er allestedsnærværende og kan bruges i en række veletablerede transformationer. Imidlertid, i C-C bindingsdannelsesreaktioner, på trods af at det er centralt for organisk syntese, alkoholer bruges for det meste indirekte. Mange alkoholbaserede reaktioner nødvendiggør kedelig præ-transformation af hydroxygruppen (C-OH) til andre funktionelle grupper, såsom halogener (f.eks. C-Br) før dannelse af C-C-binding (figur 1).
Udviklingen af et-trins C-C-bindingsdannelsesreaktioner ved anvendelse af alkoholer er yderst ønskelig, fordi det realiserer anvendelsen af allestedsnærværende materialer uden byrden ved en procedure i flere trin. En måde at nå dette mål på er direkte at omdanne alkoholer til kendte reaktive mellemprodukter, der øjeblikkeligt undergår C-C-bindingsdannelsesreaktioner. Vi forestillede os, at vi kunne opnå dette ved hjælp af lavværdige titaniumreagenser. Lavvalent titanium er en elektroneliminator og en meget oxofil art. På grund af disse funktioner, det forventes, at lavvalent titanium kan ekstrahere et oxygenatom fra alkohol, spaltning af C-O-bindingen i en elektronreduktion for at generere den tilsvarende carbonradikal (C*). Kulradikalen er et ekstremt reaktivt mellemprodukt, der let undergår forskellige reaktioner, herunder C-C bindingsdannelse.
Resultater
Behandling af 2-naphthalenemethanol med et lavværdigt titaniumreagens gav en blanding af to C-O-spaltede produkter fra hydrogenering og dimerisering (figur 2). Disse reaktioner var i sig selv ikke særlig nyttige; imidlertid, de var begge tegn på dannelsen af benzylradikale arter. Med dette foreløbige resultat, vi forventede, at tilsætning af radikalfangende midler ville have råd til koblingsprodukterne mellem benzylradikalen og fangstmidlerne, afbryde hydrogenerings- og dimeriseringsreaktionerne. Ja, tilsætningen af acrylonitril som et fangstmiddel gav koblingsproduktet mellem benzylradikalen og acrylonitril som det fremherskende produkt.
Det bedste resultat blev opnået, når det lavværdige titaniumreagens blev fremstillet ud fra TiCl4 (kollidin) og manganpulver. Denne alkoholbaserede direkte C-C-bindingsdannelsesreaktion blev med succes påført en række benzylalkoholderivater. Bemærkelsesværdigt, både benzylalkoholer med elektrondonerende og tilbagetrækningssubstituenter på den aromatiske ring var egnede til denne reaktion. Desuden, ud over primære alkoholer, sekundære og tertiære alkoholer var også egnede på trods af den betydelige stigning i sterisk hindring. Flere elektronmangel andre alkener end acrylonitril var også gode reaktanter. Med hensyn til det praktiske, denne reaktion er omkostningseffektiv og let at gennemføre, i det mindste i laboratorieskala. TiCl 4 (kollidin) er stabil under opbevaring, tolerant over for kort eksponering for luft, og koster kun cirka 10 JPY/mmol.
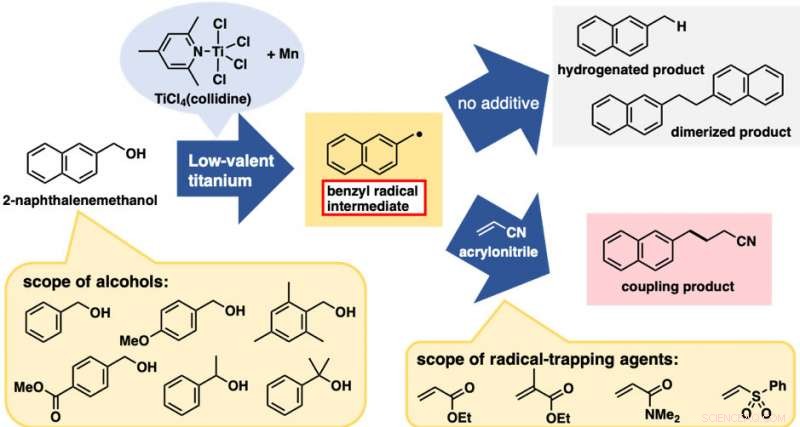
Alkoholbaserede direkte radikale C-C-bindingsdannelsesreaktioner. Øverste pil:reaktioner uden fældemiddel. Nedre pil:reaktioner med radikalfangende midler (elektronmangel-alkener). Kredit:Kanazawa University
Betydning og fremtidsudsigter
Betydningen af denne metode er, at den muliggør direkte brug af alkoholer som kulstofradikale ækvivalenter. Vi har forbundet allestedsnærværende alkoholer med akkumuleret viden om radikale reaktioner. Vi mener, at dette arbejde vil fremskynde forskning i andre alkoholbaserede radikale reaktioner i den nærmeste fremtid.
Sidste artikelLægemiddel mod superbakterier fundet i kråbær
Næste artikelCelleadfærd, engang indhyllet i mystik, afsløres i nyt lys
 Varme artikler
Varme artikler
-
 Kobberkatalyseret enantioselektiv trifluormethylering af benzylradikaler udvikletKredit:CC0 Public Domain Forskere fra Shanghai Institute of Organic Chemistry ved det kinesiske videnskabsakademi (CAS) har udviklet den første kobberkatalyserede enantioselektive trifluormethyler
Kobberkatalyseret enantioselektiv trifluormethylering af benzylradikaler udvikletKredit:CC0 Public Domain Forskere fra Shanghai Institute of Organic Chemistry ved det kinesiske videnskabsakademi (CAS) har udviklet den første kobberkatalyserede enantioselektive trifluormethyler -
 Imaging den kemiske struktur af individuelle molekyler, atom for atomBrookhaven Lab-fysiker Percy Zahl med det ikke-kontaktede atomkraftmikroskop, han tilpassede og brugte på Center for Functional Nanomaterials (CFN) til at afbilde nitrogen- og svovlholdige molekyler i
Imaging den kemiske struktur af individuelle molekyler, atom for atomBrookhaven Lab-fysiker Percy Zahl med det ikke-kontaktede atomkraftmikroskop, han tilpassede og brugte på Center for Functional Nanomaterials (CFN) til at afbilde nitrogen- og svovlholdige molekyler i -
 Nikkelatom hjælper med at reducere kuldioxidFigur 1:At vide, hvordan en nikkeljernsulfidkatalysator hjælper med at reducere kuldioxid til kulilte og andre kulbaserede produkter, kan føre til teknologier, der kan omdanne kuldioxid i atmosfæren t
Nikkelatom hjælper med at reducere kuldioxidFigur 1:At vide, hvordan en nikkeljernsulfidkatalysator hjælper med at reducere kuldioxid til kulilte og andre kulbaserede produkter, kan føre til teknologier, der kan omdanne kuldioxid i atmosfæren t -
 Det biologisk nedbrydelige batteri, der er 3D-printet, engangs og lavet af papirDet biologisk nedbrydelige batteri består af fire lag, alle flyder ud af en 3D-printer efter hinanden. Det hele bliver så foldet sammen som en sandwich, med elektrolytten i midten. Billede:Gian Vaitl
Det biologisk nedbrydelige batteri, der er 3D-printet, engangs og lavet af papirDet biologisk nedbrydelige batteri består af fire lag, alle flyder ud af en 3D-printer efter hinanden. Det hele bliver så foldet sammen som en sandwich, med elektrolytten i midten. Billede:Gian Vaitl
- Ny metode til masseproduktion af grafen udviklet
- Et univers med oligarker:Reioniseringsæra sandsynligvis arbejdet for de mest massive, lysende galak…
- Gammelt pigment kan øge energieffektiviteten
- Klimaændringer øger behovet for vanddiplomati
- Fjernarbejde vil stressteste internettet - og dele skal repareres, siger ekspert
- Supercomputere uden spildvarme


