Kemikere løser vedvarende problem efter fire årtier

Kredit:Leiden University
Efter næsten fire årtier, Leider og Eindhoven kemikere har løst diskussionen om den korrekte model vedrørende den enkleste kemiske reaktion i heterogen katalyse, som er afgørende for brændselsceller. Ved hjælp af en unik buet platinoverflade, Ludo Juurlink og ph.d. kandidat Richard van Lent fra Leiden og Michael Gleeson fra DIFFER viste, hvilken model der korrekt beskriver reaktionen af brint. De offentliggjorde deres fund i Videnskab den 11. januar.
I næsten fire årtier har der været en heftig debat i den kemiske litteratur:hvilken af de to eksisterende modeller for reaktion af brint til en platinkatalysator er korrekt (se boks)? Traditionelle metoder var ikke tilstrækkelige nok til at bevise dette. Leidens kemiker Ludo Juurlink og Michael Gleeson fra Dutch Institute for Fundamental Energy Research (DIFFER) besluttede at udvikle en ny metode til at levere afgørende beviser, hvilket viste sig at være en succes.
De to eksisterende modeller for heterogen katalyse giver forskellige forudsigelser om, hvordan hydrogenreaktionen afhænger af platinoverfladens struktur. Ved hjælp af målinger kunne forskerne bestemme brintets reaktivitet og dermed bevise, hvilken model der er korrekt. Den buede platinkrystal var afgørende for dette, som blev lavet af det hollandske firma i Zaandam for første gang. "Fordi platinoverfladen er buet, atomstrukturen ændres meget gradvist langs overfladen, "forklarer Juurlink." Du kan sammenligne denne struktur med en trappe, hvis trin mod kanterne bliver smallere og smallere. I midten ligner det mere en balsal. "Det viste sig, at brintens reaktivitet var lineært afhængig af, hvor tæt trinene er på hinanden. Jo længere fra hinanden trinene var, desto mindre reaktivt hydrogen var. "Og så er modellen, der forudsagde en ikke-lineær adfærd, forkert, " han siger.
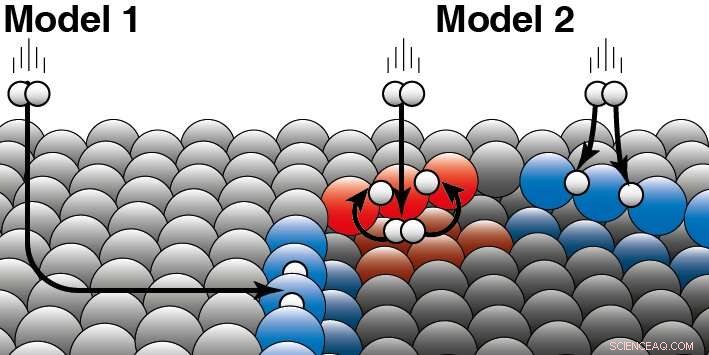
En katalysator fremskynder en kemisk reaktion uden at blive forbrugt. Ved heterogen katalyse, katalysatoren er sædvanligvis et fast stof og reaktanterne en gas eller væske. Juurlink forklarer forskellen mellem de to modeller:'De to modeller er baseret på forskellige antagelser om, hvordan kinetisk energi fra brintmolekylet "lækker væk" under kollisionen med platinoverfladen.' For at præcisere dette, han giver et eksempel:'Hvis en hund er i et ishul, han er måske endt der på to måder. Enten gled han over isen fra siden og faldt ned i ishullet, eller han sprang direkte ind i ishullet fra siden. ' Deres forskning viser nu, at brintmolekyler hovedsageligt reagerer direkte ud af gasfasen ved trinkanten af platin (Model 2). Model 1, det forudsætter at de fleste molekyler ender i kanterne ved at 'skate' over den flade platinoverflade og først derefter reagere er derfor ikke korrekt. Forskerne så forskelle mellem de to forskellige typer kanter (rød og blå), der forekommer naturligt på platinkatalysatorer. Hydrogen kan lande på toppen eller bunden af en sådan kant. For begge typer trinkanter, forskerne er i stand til at beslutte, hvilken del der reagerer direkte på oversiden (som vist i blå) eller først lander på undersiden (som i rødt). Kredit:Leiden University
Undersøgelsen blev udført i ultrahøjt vakuum og giver vigtig indsigt. "Vi ved nu bedre, hvordan vi beregner hastigheden af kemiske reaktioner - en af modellerne bidrager ikke væsentligt, "siger Juurlink." Desuden vi ved nu, at disse buede krystaloverflader tilbyder en unik, ny mulighed for at lære, hvordan kemiske reaktioner rent faktisk opstår på overflader. Vi vil helt sikkert lave mere research med det. "
Næsten alle større kemiske industrielle processer anvender heterogen katalyse. Katalysatorer er nogle gange dyre og sjældne, såsom platin, en fælles katalysator, der findes i brændselsceller og biludstødningssystemer. "Det usædvanlige er, at vi normalt ikke engang rigtig ved, hvordan og hvorfor sådanne katalysatorer fremskynder kemiske reaktioner, "siger Juurlink. Bedre indsigt i dette, hvordan og hvorfor vil bidrage til at gøre den kemiske industri mere bæredygtig." Baseret på en bedre forståelse af, hvad der sker på atomniveau, vi kan udvikle nye katalysatorer, "siger Juurlink." Katalysatorer, der forårsager mindre energitab og er mindre afhængige af dyre og sjældne materialer. "
Sidste artikelGør ammoniak grønnere
Næste artikelForskere designer nyt responsivt porøst materiale inspireret af proteiner
 Varme artikler
Varme artikler
-
 Intet laboratorium påkrævet:Ny teknologi kan diagnosticere infektioner på få minutterMcMaster University-forsker Richa Pandey viser ny teknologi, der kan analysere en medicinsk prøve og returnere en nøjagtig, endeligt resultat på få minutter. Kredit:McMaster University Ideen om at
Intet laboratorium påkrævet:Ny teknologi kan diagnosticere infektioner på få minutterMcMaster University-forsker Richa Pandey viser ny teknologi, der kan analysere en medicinsk prøve og returnere en nøjagtig, endeligt resultat på få minutter. Kredit:McMaster University Ideen om at -
 Termisk lagring til energiomstillingALMA-fordampningssystemet giver mulighed for at coate små dele. Kredit:Fraunhofer-Gesellschaft I Tyskland, 55 procent af det endelige energiforbrug går til opvarmning og køling. Imidlertid, meget
Termisk lagring til energiomstillingALMA-fordampningssystemet giver mulighed for at coate små dele. Kredit:Fraunhofer-Gesellschaft I Tyskland, 55 procent af det endelige energiforbrug går til opvarmning og køling. Imidlertid, meget -
 Hudvaccination med mikronåleplaster, influenzafusionsprotein forbedrer effektiviteten af influenz…Kredit:Georgia State University En boostende hudvaccination med et bionedbrydeligt mikronåleplaster og protein konstrueret ud fra sekvenser af influenzavirus undertyper kunne forbedre effektivitet
Hudvaccination med mikronåleplaster, influenzafusionsprotein forbedrer effektiviteten af influenz…Kredit:Georgia State University En boostende hudvaccination med et bionedbrydeligt mikronåleplaster og protein konstrueret ud fra sekvenser af influenzavirus undertyper kunne forbedre effektivitet -
 Appellerende fund tyder på, hvorfor køling dæmper bananaromaerKredit:American Chemical Society Bananer er en af verdens mest populære frugter. Men hvordan de opbevares, før de når dagligvarehylderne, kan påvirke deres smag og lugt negativt. Nu i en undersø
Appellerende fund tyder på, hvorfor køling dæmper bananaromaerKredit:American Chemical Society Bananer er en af verdens mest populære frugter. Men hvordan de opbevares, før de når dagligvarehylderne, kan påvirke deres smag og lugt negativt. Nu i en undersø
- Forsker kæmper mod skotsk kost
- Skoler er mindre vigtige end forældre til at bestemme ambitioner om videregående uddannelse
- Maskinlæring afdækker signaturen for langsomt glidende jordskælvs oprindelse i seismiske data
- Forskellen mellem fotosyntese og respiration
- Michelangelo bygninger
- Flyselskaber går en usikker fremtid i møde og har brug for hjælp hurtigt:IATA


