Kemikere øger brugen af bor:At forhindre forbindelser i at nedbrydes kan hjælpe kemikere med at designe nye lægemidler

MIT kemikere har skabt en ny borholdig kemisk gruppe, der er 10, 000 gange mere stabil end bor alene. Kredit:MIT News
bor, et metalloid element, der sidder ved siden af kulstof i det periodiske system, har mange egenskaber, der gør det potentielt nyttigt som lægemiddelkomponent. Ikke desto mindre, kun fem FDA-godkendte lægemidler indeholder bor, hovedsagelig fordi molekyler, der indeholder bor, er ustabile i nærvær af molekylært oxygen.
MIT-kemikere har nu designet en borholdig kemisk gruppe, der er 10, 000 gange mere stabil end sine forgængere. Dette kunne gøre det muligt at inkorporere bor i lægemidler og potentielt forbedre lægemidlernes evne til at binde deres mål, siger forskerne.
"Det er en enhed, som medicinske kemikere kan tilføje til forbindelser, de er interesserede i, at give ønskværdige egenskaber, som intet andet molekyle vil have, " siger Ron Raines, Firmenich -professoren i kemi ved MIT og seniorforfatteren af det nye studie.
For at demonstrere potentialet i denne tilgang, Raines og hans kolleger viste, at de kunne forbedre proteinbindingsstyrken af et lægemiddel, der bruges til at behandle sygdomme forårsaget af fejlfoldning af et protein kaldet transthyretin.
MIT kandidatstuderende Brian Graham og tidligere kandidatstuderende Ian Windsor er hovedforfatteren af undersøgelsen, som vises i denne uge i Procedurer fra National Academy of Sciences . Tidligere MIT postdoc Brian Gold er også forfatter til papiret.
Hungrer efter elektroner
Bor findes oftest i jordskorpen i form af mineraler som boraks. Den indeholder en færre elektron end kulstof og er sulten efter yderligere elektroner. Når bor inkorporeres i en potentiel lægemiddelforbindelse, at hunger efter elektroner ofte får det til at interagere med et oxygenmolekyle (O2) eller en anden reaktiv form for oxygen, som kan ødelægge forbindelsen.
Det borholdige lægemiddel bortezomib, som forhindrer celler i at kunne nedbryde brugte proteiner, er et effektivt kræftkemoterapimiddel. Imidlertid, stoffet er ustabilt og ødelægges let af ilt.
Tidligere forskning har vist, at stabiliteten af borholdige forbindelser kan øges ved at tilsætte benzen, en seks-carbon ring. I 2018, Raines og hans kolleger brugte denne tilgang til at skabe en modificeret version af et lægemiddel kaldet darunavir, en proteasehæmmer, der bruges til at behandle HIV/AIDS. De fandt ud af, at dette molekyle bandt sig meget tættere til HIV-protease end den originale version af darunavir. Imidlertid, senere undersøgelser afslørede, at molekylet stadig ikke overlevede længe under fysiologiske forhold.
I det nye blad, forskerne besluttede at bruge en kemisk gruppe kaldet et carboxylat til yderligere at forankre bor i et molekyle. Et oxygenatom i carboxylatet danner en stærk kovalent binding - en type binding, der involverer deling af elektronpar mellem atomer - med bor.
"Den kovalente binding pacificerer bor, "Raines siger." Boret kan ikke længere reagere med et iltmolekyle på den måde, som bor i andre sammenhænge kan, og den bevarer stadig sine ønskelige egenskaber. "
En af disse ønskelige egenskaber er evnen til at danne reversible kovalente bindinger med lægemidlets mål. Denne reversibilitet kunne forhindre medicin i permanent at låse sig fast på forkerte mål, Siger Raines. En anden nyttig egenskab er, at den borholdige gruppe - også kendt som benzoxaboralone - danner mange svagere bindinger kaldet hydrogenbindinger med andre molekyler, hvilket hjælper med at sikre en tæt pasform, når det rigtige mål er fundet.
Større stabilitet
Da de først viste, at benzoxaboralon var signifikant mere stabil end bor i andre sammenhænge, forskerne brugte det til at skabe et molekyle, der kan binde sig til transthyretin. Dette protein, som transporterer hormoner gennem blodbanen, kan forårsage amyloide sygdomme, når det folder sig forkert og klumper. Lægemidler, der binder til transthyretin, kan stabilisere det og forhindre det i at klumpe. Forskerholdet viste, at tilsætning af benzoxaboralone til et eksisterende lægemiddel hjalp det til at binde stærkt med transthyretin.
Benzoxaboralone kan tilbyde medicinske kemikere et nyttigt værktøj, som de kan udforske i mange forskellige typer lægemidler, der binder til proteiner eller sukkermolekyler, siger Raines. Hans laboratorium arbejder nu på en ny version af darunavir, der inkorporerer benzoxaboralone. De har for nylig udviklet en måde at syntetisere denne forbindelse på og er nu i gang med at måle, hvor stærkt den binder til HIV-protease.
"Vi arbejder hårdt på dette, fordi vi tror, at dette stillads vil give meget større stabilitet og nytteværdi end nogen anden præsentation af bor i en biologisk kontekst, " siger Raines.
Denne historie er genudgivet med tilladelse fra MIT News (web.mit.edu/newsoffice/), et populært websted, der dækker nyheder om MIT-forskning, innovation og undervisning.
 Varme artikler
Varme artikler
-
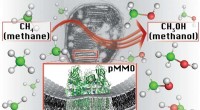 Metanforbrugende bakterier kan være fremtiden for brændstofDet primære metaboliske enzym i metanotrofe bakterier, partikelformig methanmonooxygenase (pMMO), katalyserer metan-til-methanol-omdannelsen på et sted med en kobberion. Kredit:Northwestern University
Metanforbrugende bakterier kan være fremtiden for brændstofDet primære metaboliske enzym i metanotrofe bakterier, partikelformig methanmonooxygenase (pMMO), katalyserer metan-til-methanol-omdannelsen på et sted med en kobberion. Kredit:Northwestern University -
 Værktøjssæt:Brug af lokal jord til 3D-print af store strukturer(A) Illustration af geopolymerisationstilgang udviklet til at størkne moskus til en bærende silikatkomposit, som repræsenteret ved kraften af et bildæk på vej forstærket af kompositmaterialet, genop
Værktøjssæt:Brug af lokal jord til 3D-print af store strukturer(A) Illustration af geopolymerisationstilgang udviklet til at størkne moskus til en bærende silikatkomposit, som repræsenteret ved kraften af et bildæk på vej forstærket af kompositmaterialet, genop -
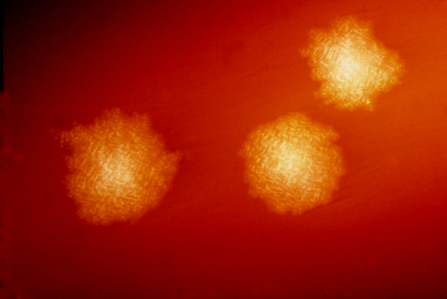 Alsidig C. difficile blockerDette fotografi afbilder Clostridium difficile-kolonier efter 48 timers vækst på en blodagarplade; Forstørret 4,8X. C. difficile, en anaerob gram-positiv stang, er den hyppigst identificerede årsag ti
Alsidig C. difficile blockerDette fotografi afbilder Clostridium difficile-kolonier efter 48 timers vækst på en blodagarplade; Forstørret 4,8X. C. difficile, en anaerob gram-positiv stang, er den hyppigst identificerede årsag ti -
 Fingeraftryk mangler videnskabeligt grundlag for retssikkerhedKredit:Carnegie Mellon University Det kan overraske mange, især dem, der er modtagelige for CSI-effekten, men fingeraftryksbeviser er ikke afgørende ud over enhver rimelig tvivl. En ny rapport fr
Fingeraftryk mangler videnskabeligt grundlag for retssikkerhedKredit:Carnegie Mellon University Det kan overraske mange, især dem, der er modtagelige for CSI-effekten, men fingeraftryksbeviser er ikke afgørende ud over enhver rimelig tvivl. En ny rapport fr
- Femte klasse videnskabsprojekt med vandgenereret elektricitet
- Endnu flere tests for de fleste testede børn i verden
- Sådan øges et tal med en procentdel
- Menneskelige fodspor går tilbage 120, 000 år fundet i Saudi-Arabien
- Internationalt forskningsprojekt undersøger lysfølsomme kulstofnanopartikler
- Har lys som en fjer,


