Fremskridt inden for taxolbiosyntese kan føre til storstilet produktion af anticancerlægemiddel
Paclitaxel er verdens bedst sælgende plantebaserede lægemiddel mod kræft og et af de mest effektive lægemidler mod kræft gennem de seneste 30 år. Det er meget udbredt til behandling af forskellige typer kræft, herunder brystkræft, lungekræft og kræft i æggestokkene.
I slutningen af 1990'erne og begyndelsen af det 21. århundrede oversteg det årlige salg af paclitaxel 1,5 milliarder USD og nåede 2,0 milliarder USD i 2001, hvilket gjorde det til det bedst sælgende lægemiddel i 2001. I 2019 var markedet for paclitaxel og dets derivater cirka 15 milliarder USD, og det forventes at nå $20 milliarder i 2025.
Som et lægemiddel mod kræft er paclitaxels molekylære struktur ekstremt kompleks med stærkt oxiderede, indviklede ringe med bro og 11 stereocentre, hvilket gør det bredt anerkendt som et af de mest udfordrende naturlige produkter at syntetisere kemisk. Siden den første totale syntese af paclitaxel blev rapporteret af forskergrupperne Holton og Nicolaou i 1994, har mere end 40 forskerhold været involveret i den totale syntese af paclitaxel.
Men selv i den korteste kemiske syntesevej til dato er det samlede udbytte af paclitaxel kun 0,118%, hvilket ikke opfylder efterspørgslen efter industriel produktion. I øjeblikket anvender den industrielle produktion af paclitaxel en semisyntetisk strategi:isolering af paclitaxel-precursorer (såsom baccatin III) fra plantecellekulturer eller Taxus-blade og derefter omdanne dem til paclitaxel ved hjælp af kemiske metoder. Den semisyntetiske strategi er dog stærkt afhængig af naturressourcer og er begrænset af den langsomme vækst af Taxus-celler eller blade og kan derfor ikke imødekomme den voksende markedsefterspørgsel.
Med den hurtige udvikling af bioteknologi er syntetisk biologistrategier for mikrobiel biosyntese af plantenaturprodukter dukket op som en kraftfuld tilgang til at producere komplekse plantenaturprodukter effektivt.
Derfor har opnåelse af effektiv, miljøvenlig og bæredygtig produktion af paclitaxel gennem syntetisk biologi tiltrukket bred opmærksomhed. At realisere de novo-syntesen af paclitaxel i et heterologt system kræver imidlertid at identificere de nøgleenzymer, der mangler i paclitaxel-biosyntesevejen, og etablere en komplet biosyntesevej for paclitaxel.
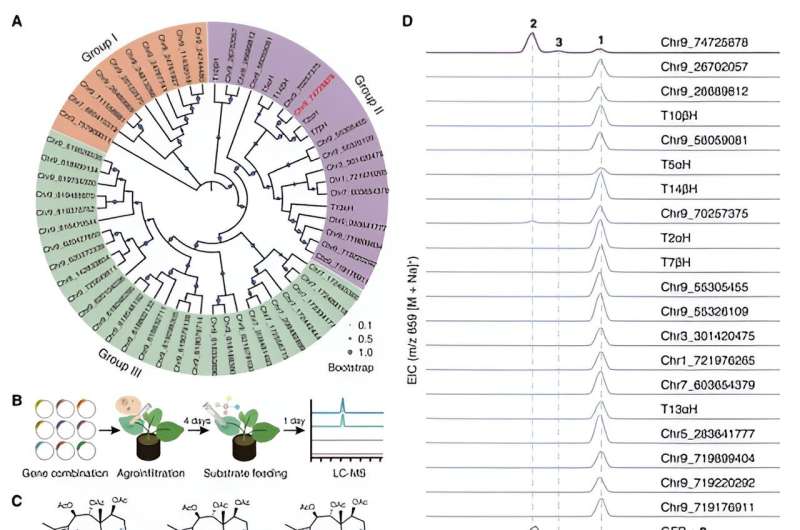
For at løse den langvarige udfordring med paclitaxel-biosyntese i Taxus har to forskerhold ledet af prof. Jianbin Yan (Agricultural Genomics Institute i Shenzhen, AGIS) og prof. Xiaoguang Lei (Peking University, PKU) samt andre forskerhold fra fem andre forskellige institutioner, herunder Tsinghua University og UCLA, har samarbejdet om med succes at identificere de manglende enzymer og opnå rekonstituering af de biosyntetiske enzymer, der fører til baccatin III.
Forskerne brugte et tobaks heterologt ekspressionssystem til at udføre aktivitetsscreening af CYP725A-genfamilien fundet specifikt i Taxus via substrat co-injektion strategi. De har med succes identificeret et biosyntetisk enzym ved navn Taxane oxetanase (TOT), der katalyserer dannelsen af oxetanringen under taxolbiosyntesevejen.
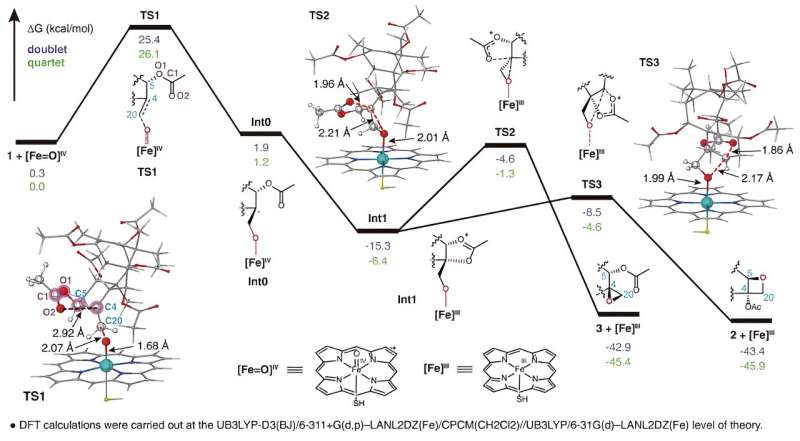
TOT katalyserer dannelsen af den unikke oxetanring gennem oxidation af C4,20-dobbeltbindingen og efterfølgende omlejring af den tilstødende acetylgruppe i C5-positionen, som afbildet i. Denne nye reaktionsmekanisme for oxetanringdannelse bryder den konventionelle forståelse af, at oxetanringen dannelse i taxolbiosyntesevejen opnås gennem en omlejringsreaktion af det tilsvarende epoxid.
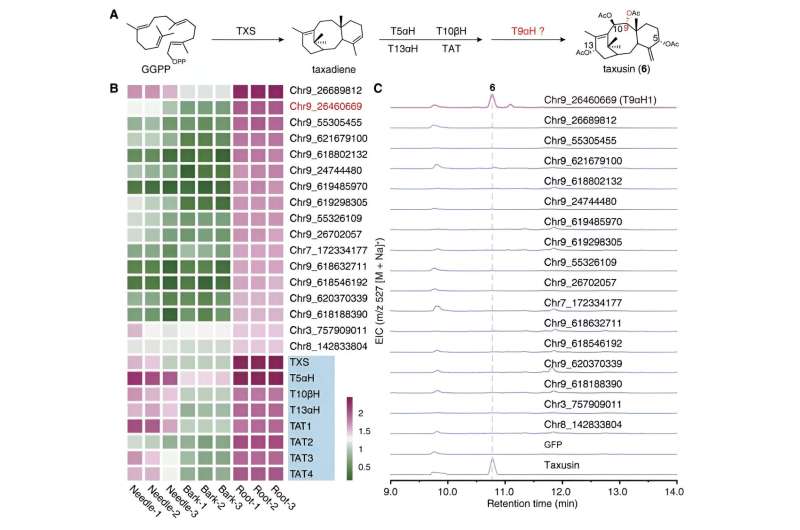
I mellemtiden, ved at fokusere på den strukturelt simplere forbindelse, taxusin, identificerede forskerne 17 kandidatgener, der koder for enzymer, der er ansvarlige for C9-oxidationen af taxaner ved hjælp af co-ekspressionsanalysen og metabolismeanalysen. Disse kandidatgener blev yderligere udsat for aktivitetsscreening ved at rekonstruere taxusin-biosyntesevejen i tobak, hvilket førte til opdagelsen af enzymet, der er ansvarligt for C9-oxidation i taxaner, som fik navnet Taxane 9α-hydroxylase (T9αH).
Med disse to nyligt identificerede enzymer TOT og T9αH i hænderne forsøgte forskere at opnå den totale biosyntese af baccatin III i tobak ved at udtrykke dem sammen med andre kendte biosyntetiske gener af taxol. De påviste med succes produktionen af baccatin III i tobak, når TOT og T9αH blev co-udtrykt med andre 7 kendte biosyntetiske gener (TXS, T5αH, T13αH, T2αH, T7βH, TAT og TBT). Desuden har de påvist, at disse ni gener er kernegenerne for baccatin III-biosyntese, da hvert gen er uundværligt for biosyntesen af baccatin III i tobak.
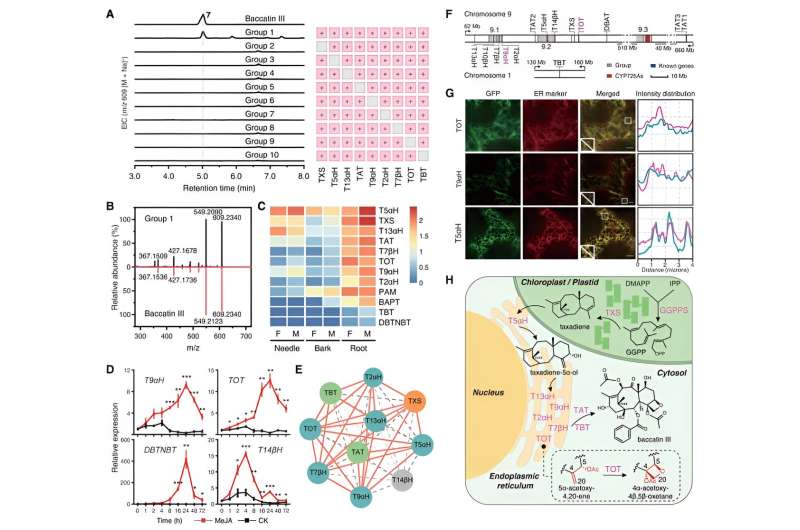
Yderligere biokemiske undersøgelser viste, at disse kernegener udviser tæt funktionel synergi og er co-reguleret af plantehormonet jasmonat, hvilket viser lignende induktionsekspressionsmønstre og stærk ekspressionskorrelation. Ved at kombinere subcellulær lokaliseringsanalyse og andre eksperimentelle resultater giver forskerne et komplet overblik over den biosyntetiske proces af baccatin III.
Udgangssubstratet GGPP katalyseres af TXS til dannelse af taxadien i kloroplaster. Efterfølgende overføres taxadien til cytoplasmaet gennem kontaktstederne af plastid-endoplasmatisk reticulum og gennemgår samordnet katalyse af seks membranbundne oxidaser (T2αH, T5αH, T7βH, T9αH, T13αH og TOT) forankret i de endoplasmiske og to cytoplasmiske reticulum. transferaser (TAT og TBT), hvilket i sidste ende resulterer i dannelsen af baccatin III.
Sammenfattende er denne undersøgelse, som er blevet offentliggjort i Science for nylig, kombinerer flere omics-analyser og omfattende funktionel validering for med succes at identificere manglende nøgleenzymer i paclitaxels biosyntesevej. Den afslører en ny mekanisme, hvorved planteceller katalyserer dannelsen af oxetanringe og opdager den korteste vej for paclitaxel heterolog biosyntese.
Ved at co-udtrykke 9 kerneenzymer i tobak opnår forskerne bioproduktionen af paclitaxel precursor baccatin III, hvilket lægger grundlaget for storskala produktion af paclitaxel og giver også teoretisk vejledning til biosyntetiske undersøgelser af hundredvis af andre taxannaturprodukter.
Flere oplysninger: Bin Jiang et al., Karakterisering og heterolog rekonstitution af Taxus biosyntetiske enzymer, der fører til baccatin III, Science (2024). DOI:10.1126/science.adj3484
Journaloplysninger: Videnskab
Leveret af Peking University
 Varme artikler
Varme artikler
-
 Hvordan kemiske reaktioner beregnesKredit:Pixabay/CC0 Public Domain Et enkelt molekyle indeholder et væld af information. Det inkluderer ikke kun antallet af hver type af atomer, men også hvordan de er arrangeret og hvordan de knyt
Hvordan kemiske reaktioner beregnesKredit:Pixabay/CC0 Public Domain Et enkelt molekyle indeholder et væld af information. Det inkluderer ikke kun antallet af hver type af atomer, men også hvordan de er arrangeret og hvordan de knyt -
 Forskere undersøger makrocykliske peptider som nye lægemiddelskabelonerNogle af disse molekyler kan krydse cellemembranen og kan åbne døre for nye lægemidler til i øjeblikket ubehandlede sygdomme. Kredit:Gwangju Institute of Science and Technology Takket være vores f
Forskere undersøger makrocykliske peptider som nye lægemiddelskabelonerNogle af disse molekyler kan krydse cellemembranen og kan åbne døre for nye lægemidler til i øjeblikket ubehandlede sygdomme. Kredit:Gwangju Institute of Science and Technology Takket være vores f -
 Stive, ømme knæ? Lab-fremstillet bruskgelé overgår den ægte vareEt hydrogel-baseret implantat kunne erstatte slidt brusk og lindre knæsmerter uden at erstatte hele leddet. Kredit:Benjamin Wiley, Duke University. Smertestillende midler i håndkøb, fysioterapi, st
Stive, ømme knæ? Lab-fremstillet bruskgelé overgår den ægte vareEt hydrogel-baseret implantat kunne erstatte slidt brusk og lindre knæsmerter uden at erstatte hele leddet. Kredit:Benjamin Wiley, Duke University. Smertestillende midler i håndkøb, fysioterapi, st -
 Ny nanopladebelægning kunne erstatte ikke-genanvendelige metalliserede film i fødevareemballageLDH nanoark med højt billedformat. en Skematisk, der viser (I) kalcinering (mellemlagsvand og anioner fjernes ved kalcinering) og (II) rekonstruktionsproces og den foretrukne væksthæmning i en opløsni
Ny nanopladebelægning kunne erstatte ikke-genanvendelige metalliserede film i fødevareemballageLDH nanoark med højt billedformat. en Skematisk, der viser (I) kalcinering (mellemlagsvand og anioner fjernes ved kalcinering) og (II) rekonstruktionsproces og den foretrukne væksthæmning i en opløsni
- Millioner svulmer i det vestlige USA, da Canada tager nødstilfælde
- Forskere udforsker at bruge lys til at svæve diske i mesosfæren
- Astrofysikere opdager planeter i ekstragalaktiske galakser ved hjælp af mikrolinsing
- Den uerstattelige rolle som mor-og-pop-rum for aldrende voksne
- Fire astronauter fra fire lande vender tilbage til Jorden efter seks måneder i kredsløb
- Hindringer, der begrænser bevarelsen af global arv fra UNESCO afsløret


