Opstår der en svagere brintbinding i større molekyler?
Selvom det er rigtigt, at svagere hydrogenbindinger kan forekomme i større molekyler, er det ikke universelt tilfældet. Styrken af en brintbinding bestemmes af flere faktorer, herunder elektronegativiteten af de involverede atomer, afstanden mellem atomerne og det omgivende miljø.
Generelt opstår stærkere hydrogenbindinger, når elektronegativitetsforskellen mellem atomerne er større, afstanden mellem atomerne er kortere, og det omgivende miljø er mere polært. Mens større molekyler kan have nogle svagere hydrogenbindinger på grund af øget sterisk hindring eller andre faktorer, kan de også have stærkere hydrogenbindinger, hvis de nødvendige betingelser er opfyldt.
 Varme artikler
Varme artikler
-
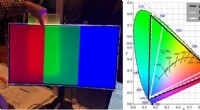 Oprettelse af skærme med rigere farver(Venstre) Foto, der viser farveforbedringseffekten ved brug af en prototype af den perovskitbaserede film. Når filmen placeres mellem baggrundsbelysningsenheden og skærmen, en spektral renere rød og g
Oprettelse af skærme med rigere farver(Venstre) Foto, der viser farveforbedringseffekten ved brug af en prototype af den perovskitbaserede film. Når filmen placeres mellem baggrundsbelysningsenheden og skærmen, en spektral renere rød og g -
 Redder gadekunst fra vandalernes graffitiKredit:CC0 Public Domain Fra Los Angeles og Lower East Side af New York City til Paris og Penang, gadekunst af berømte og knap så berømte kunstnere pryder motorveje, veje og stræder. Ud over at sk
Redder gadekunst fra vandalernes graffitiKredit:CC0 Public Domain Fra Los Angeles og Lower East Side af New York City til Paris og Penang, gadekunst af berømte og knap så berømte kunstnere pryder motorveje, veje og stræder. Ud over at sk -
 Materialer kan føre til selvhelbredende smartphonesEt nyt materiale helbreder ikke kun sig selv, men den strækker sig også op til 50 gange sin sædvanlige størrelse; disse egenskaber kan reparere din telefons batteri, hvis det revner, eller forhindre d
Materialer kan føre til selvhelbredende smartphonesEt nyt materiale helbreder ikke kun sig selv, men den strækker sig også op til 50 gange sin sædvanlige størrelse; disse egenskaber kan reparere din telefons batteri, hvis det revner, eller forhindre d -
 En rhodiumbaseret katalysator til fremstilling af organosilicium ved hjælp af mindre ædle metallerEt billede af hydrosilyleringsreaktionen ved anvendelse af den SiO2-understøttede katalysator bestående af et immobiliseret Rh-kompleks og tertiære aminer, med en omsætning på 260 (venstre) og nærmer
En rhodiumbaseret katalysator til fremstilling af organosilicium ved hjælp af mindre ædle metallerEt billede af hydrosilyleringsreaktionen ved anvendelse af den SiO2-understøttede katalysator bestående af et immobiliseret Rh-kompleks og tertiære aminer, med en omsætning på 260 (venstre) og nærmer
- At vide, hvad der fører til bygningskollaps, kan være med til at gøre afrikanske byer sikrere
- Sådan kan du blive presset til at spise sundere, genbruge og træffe bedre beslutninger hver dag
- Point Nemo, Jordens vandige kirkegård for rumfartøjer
- Nanopore åbner ny cellulær døråbning til medicintransport
- Overdreven risikabel kredit stærkt forbundet med boligkrise i de seneste årtier, undersøgelse sig…
- Statens sundhed, sikkerhedsbestemmelser giver bagslag hos konservative, viser undersøgelse


