Er guld og platin reaktive metaller?
Her er et par specifikke punkter om reaktiviteten af guld og platin:
1. Guld:
- Guld er et ædelmetal, der er meget modstandsdygtigt over for korrosion og oxidation.
- Det reagerer ikke med vand eller ilt ved stuetemperatur.
- Guld reagerer med visse kemikalier såsom klorgas (Cl2), brom (Br2) og aqua regia (en blanding af saltsyre og salpetersyre).
2. Platin:
- Platin er også et ædelmetal og er kendt for sin høje modstandsdygtighed over for korrosion og oxidation.
- Det er mindre reaktivt end guld og reagerer ikke med de fleste syrer og baser.
- Platin kan dog reagere med visse stoffer såsom klorgas (Cl2), fluor (F2) og aqua regia.
I modsætning til reaktive metaller som natrium eller kalium, der let reagerer med vand, oxygen og andre stoffer, forbliver guld og platin relativt stabile og ikke-reaktive under normale forhold. Dette gør dem værdifulde til brug i smykker, elektronik og andre applikationer, hvor korrosionsbestandighed er afgørende.
 Varme artikler
Varme artikler
-
 Tilpasning af partikelstørrelserne af Pt₅Ce-legering nanopartikler til oxygenreduktionsreaktionenIfølge forskellige mekanismer for partikelvæksten er synteseprocessen opdelt i tre sekventielle perioder, nemlig periode 1, hvor Pt4+ ioner reduceres til Pt-nanopartikler; Periode 2, hvor Pt-nanoparti
Tilpasning af partikelstørrelserne af Pt₅Ce-legering nanopartikler til oxygenreduktionsreaktionenIfølge forskellige mekanismer for partikelvæksten er synteseprocessen opdelt i tre sekventielle perioder, nemlig periode 1, hvor Pt4+ ioner reduceres til Pt-nanopartikler; Periode 2, hvor Pt-nanoparti -
 Øjeblikkelig vandrensningsmetode millioner af gange bedre end kommerciel tilgangKredit:Pixabay/CC0 Public Domain Et vanddesinfektionsmiddel, der er skabt på stedet ved hjælp af kun brint og luften omkring os, er millioner af gange mere effektivt til at dræbe vira og bakterier
Øjeblikkelig vandrensningsmetode millioner af gange bedre end kommerciel tilgangKredit:Pixabay/CC0 Public Domain Et vanddesinfektionsmiddel, der er skabt på stedet ved hjælp af kun brint og luften omkring os, er millioner af gange mere effektivt til at dræbe vira og bakterier -
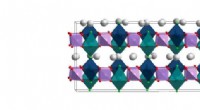 Ny genomisk metode afslører atomarrangementer af batterimaterialeLavtemperaturstrukturen af NVPF [Na3V2(PO4)2F3] løst i dette arbejde. Beregninger fra Lawrence Berkeley National Laboratory tyder på, at natriumatomerne (hvide) lettest kan bevæge sig i flyene melle
Ny genomisk metode afslører atomarrangementer af batterimaterialeLavtemperaturstrukturen af NVPF [Na3V2(PO4)2F3] løst i dette arbejde. Beregninger fra Lawrence Berkeley National Laboratory tyder på, at natriumatomerne (hvide) lettest kan bevæge sig i flyene melle -
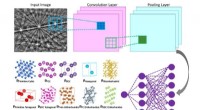 Maskinlæringsteknik fremskynder bestemmelse af krystalstrukturIllustration af den indre funktion af et konvolutionelt neuralt netværk, der beregner sandsynligheden for, at inputdiffraktionsmønsteret tilhører en given klasse (f.eks. Bravais-gitter eller rumgruppe
Maskinlæringsteknik fremskynder bestemmelse af krystalstrukturIllustration af den indre funktion af et konvolutionelt neuralt netværk, der beregner sandsynligheden for, at inputdiffraktionsmønsteret tilhører en given klasse (f.eks. Bravais-gitter eller rumgruppe
- Hvilket mål eller opgave ville højst sandsynligt blive opnået i anvendt kemi ikke ren kemi?
- Sporing af bodys mini-shuttles
- Fiskestang selfie stick og videnskabelig efterforskning viser spor til uddøde havkrybdyr
- Hvad er jordens revolutionstid?
- Forskere genskaber parfume fra det 17. århundrede af Constantijn Huygens
- Vodafone vender tilbage til profit, meddeler CEO afgang


