Hvad er de mest reaktive familier i det periodiske system, og hvorfor er de reaktive?
Alkalimetallerne er den mest reaktive familie i det periodiske system, fordi de har en enkelt valenselektron, der er løst bundet til kernen. Dette gør dem meget elektropositive, hvilket betyder, at de let mister deres valenselektron. Denne reaktivitet er det, der gør dem nyttige i en række forskellige anvendelser, såsom i batterier og som reduktionsmidler.
Gruppe 2 (jordalkalimetaller)
Jordalkalimetallerne er også meget reaktive, men ikke så meget som alkalimetallerne. Dette skyldes, at de har to valenselektroner, der er tættere bundet til kernen. Men de mister stadig let disse valenselektroner, hvilket gør dem elektropositive. Denne reaktivitet gør dem nyttige i en række forskellige anvendelser, såsom i byggeri og som gødning.
Gruppe 17 (halogener)
Halogenerne er de mest reaktive ikke-metaller i det periodiske system. Dette skyldes, at de har en høj elektronegativitet, hvilket betyder, at de har en stærk tiltrækning af elektroner. Denne reaktivitet gør dem anvendelige i en række forskellige anvendelser, såsom til desinfektion og som blegemidler.
Gruppe 18 (Ædelgasser)
Ædelgasserne er de mindst reaktive grundstoffer i det periodiske system. Dette skyldes, at de har en komplet valensskal, hvilket betyder, at de ikke har behov for at få eller miste elektroner. Denne mangel på reaktivitet gør dem nyttige i en række forskellige anvendelser, såsom i belysning og som isolatorer.
 Varme artikler
Varme artikler
-
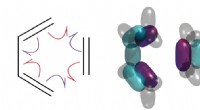 Teoretikere beviser endelig, at krøllede pile fortæller sandheden om kemiske reaktionerDiels-Alder-reaktionen er vigtig i syntesen af alle slags lægemidler, herunder D-vitamin. Men hvordan virker det? UNSW-forskere viser, at det involverer spaltning af elektronpar. Kredit:T. Schmidt
Teoretikere beviser endelig, at krøllede pile fortæller sandheden om kemiske reaktionerDiels-Alder-reaktionen er vigtig i syntesen af alle slags lægemidler, herunder D-vitamin. Men hvordan virker det? UNSW-forskere viser, at det involverer spaltning af elektronpar. Kredit:T. Schmidt -
 Fra kompost til kompositter:En miljøvenlig måde at forbedre gummi påKredit:American Chemical Society Begrebet fra skrald til skat gælder for komposteringens verden, hvor madaffald genanvendes til gødning til haver. Men hvad nu hvis kompost kunne gå ud over gødning
Fra kompost til kompositter:En miljøvenlig måde at forbedre gummi påKredit:American Chemical Society Begrebet fra skrald til skat gælder for komposteringens verden, hvor madaffald genanvendes til gødning til haver. Men hvad nu hvis kompost kunne gå ud over gødning -
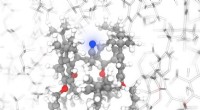 AI- og NMR-spektroskopi bestemmer atomernes konfiguration på rekordtidKredit:Michele Ceriotti / EPFL Mange lægemidler fremstilles i dag som faste stoffer i pulverform. Men for fuldt ud at forstå, hvordan de aktive ingredienser vil opføre sig en gang inde i kroppen,
AI- og NMR-spektroskopi bestemmer atomernes konfiguration på rekordtidKredit:Michele Ceriotti / EPFL Mange lægemidler fremstilles i dag som faste stoffer i pulverform. Men for fuldt ud at forstå, hvordan de aktive ingredienser vil opføre sig en gang inde i kroppen, -
 Dekontaminering af mandler og nødder med komprimeret kuldioxidBakteriekulturen udplades i et næringsmedium. Kredit:Karen Fuchs/Fraunhofer UMSICHT Der går næsten ikke en dag, uden at producenter husker mad, der er plettet af urenheder. Selv tørre fødevarer, g
Dekontaminering af mandler og nødder med komprimeret kuldioxidBakteriekulturen udplades i et næringsmedium. Kredit:Karen Fuchs/Fraunhofer UMSICHT Der går næsten ikke en dag, uden at producenter husker mad, der er plettet af urenheder. Selv tørre fødevarer, g
- Meteorer ser ud til at regne ned over New Zealand, men hvorfor er nogle lyse grønne?
- Hvad skal man vide om Chiles glubske skovbrande
- Kamæleon inspirerer smart hud, der skifter farve i solen
- Er dit drikkevand sikkert? Sådan kan du finde ud af det
- Forskere gør nye opdagelser om den molekylære struktur af naturlige produkter
- Eksperimentel demonstration af måleafhængige realiteter mulig, siger forsker


