Hvordan finter man oxidationstallet i en reaktion?
1. Identificer reaktanterne og produkterne i reaktionen.
2. Bestem ladningerne af de enkelte atomer i reaktanterne og produkterne.
- Neutrale atomer har et oxidationstal på 0.
- Monoatomiske ioner har et oxidationstal svarende til deres ladning.
- For polyatomiske ioner skal summen af de enkelte atomers oxidationstal svare til ionens samlede ladning.
3. Brug loven om bevarelse af masse til at afbalancere ligningen.
- Det samlede antal atomer af hvert grundstof skal være det samme på begge sider af ligningen.
4. Tildel oxidationsnumre til grundstofferne i reaktionen.
- Start med at tildele oxidationsnumre til de grundstoffer, der har et kendt oxidationstal, såsom brint (+1), oxygen (-2) og alkalimetaller (+1).
- Brug ladningerne af ionerne til at hjælpe dig med at tildele oxidationsnumre til de andre grundstoffer.
- Tjek, at summen af oxidationstallene for atomerne i hver forbindelse er lig med den samlede ladning af forbindelsen.
5. Beregn ændringen i oxidationstal for hvert grundstof.
- Ændringen i oxidationstallet er forskellen mellem grundstoffets oxidationstal i produktet og grundstoffets oxidationstal i reaktanten.
- En positiv ændring i oxidationstal indikerer, at grundstoffet er blevet oxideret, mens en negativ ændring i oxidationstal indikerer, at grundstoffet er blevet reduceret.
Her er et eksempel på, hvordan man finder oxidationstallene i en reaktion:
- Reaktanter:Fe(s) + 2HCl(aq) --> FeCl2(aq) + H2(g)
- Produkter:Fe(II) har et oxidationstal på +2 i FeCl2.
- Cl(-1) har et oxidationstal på -1 i HCl og FeCl2.
- H(+1) har et oxidationstal på +1 i HCl og H2.
- Da reaktionen er afbalanceret, er det samlede antal atomer af hvert grundstof det samme på begge sider af ligningen.
Ændringen i oxidationstal for hvert grundstof er:
- Fe:0 → +2 (2e- tabt)
- H:+1 → 0 (2e-forøget)
- Cl:0 → -1 (1e- opnået)
- Derfor oxideres Fe, H reduceres, og Cl reduceres.
Sidste artikelHvad er en As2O5-forbindelse?
Næste artikelHvad skal være sandt om den nettoioniske ladning i en forbindelse?
 Varme artikler
Varme artikler
-
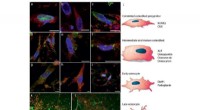 Forskere dyrker den mest naturtro knogle endnu fra vævede cellerDifferentiering af hBMSCer til osteoblaster og osteocytter:a–i) Fluorescensimmunhistokemi billeddannelse, der viser markører for a–c) tidlige stadier af osteoblastdannelse, d–f) modne osteoblaster, og
Forskere dyrker den mest naturtro knogle endnu fra vævede cellerDifferentiering af hBMSCer til osteoblaster og osteocytter:a–i) Fluorescensimmunhistokemi billeddannelse, der viser markører for a–c) tidlige stadier af osteoblastdannelse, d–f) modne osteoblaster, og -
 Forskning ser på materialets friktionsegenskaberSandia National Laboratories forskere Michael Chandross, venstre, og Nicolas Argibay viser en computersimulering og et ultrahøjt vakuum tribometer brugt til friktions- og slidtest, som er blandt de væ
Forskning ser på materialets friktionsegenskaberSandia National Laboratories forskere Michael Chandross, venstre, og Nicolas Argibay viser en computersimulering og et ultrahøjt vakuum tribometer brugt til friktions- og slidtest, som er blandt de væ -
 sekvensering, mRNA, eller måske nanokrystaller? Vidt åbent felt til Nobels KemiprisKemi Nobel er den tredje, der bliver uddelt i denne uge, efter medicin og fysik. Gennembrud i DNA-sekventering, innovativ gaslagring, nanokrystaller eller en ny chance for mRNA Covid-19-vacciner?
sekvensering, mRNA, eller måske nanokrystaller? Vidt åbent felt til Nobels KemiprisKemi Nobel er den tredje, der bliver uddelt i denne uge, efter medicin og fysik. Gennembrud i DNA-sekventering, innovativ gaslagring, nanokrystaller eller en ny chance for mRNA Covid-19-vacciner? -
 grafen, perovskites, og silicium – en ideel tandem til effektive solcellerDenne visualisering viser lag af grafen, der bruges til membraner. Kredit:University of Manchester Forskere ved universitetet i Rom Tor Vergata, det italienske teknologiske institut (IIT) og dets
grafen, perovskites, og silicium – en ideel tandem til effektive solcellerDenne visualisering viser lag af grafen, der bruges til membraner. Kredit:University of Manchester Forskere ved universitetet i Rom Tor Vergata, det italienske teknologiske institut (IIT) og dets
- Styring og visualisering af receptorsignaler i neurale celler med lys
- Fossile brændstoffer kan stadig bidrage til luftforurening, selv når bilen er slukket
- Planetfinder til beboelig zone gør det muligt at finde planeter omkring seje stjerner
- Livet på Mars? Forskere siger, at undvigende mineral styrker chancerne
- Brug af kvantemekanikkens uforudsigelige natur til at generere virkelig tilfældige tal
- Kan startups være fartøjet til at løse klimaændringer?


