Påvirker trykændringer opløseligheden af faste stoffer?
For de fleste faste opløste stoffer er virkningen af tryk på opløselighed ret lille og ofte ubetydelig. Dette skyldes, at volumenændringen ved opløsning af et fast stof i en væske normalt er lille sammenlignet med opløsningens volumen. Derfor har ændringen i tryk en minimal indvirkning på ligevægten mellem den faste og den opløste art.
Der er dog visse undtagelsestilfælde, hvor tryk kan påvirke opløseligheden af faste stoffer. Disse undtagelser involverer normalt faste stoffer, der undergår væsentlige ændringer i deres krystalstruktur eller faseadfærd under højtryksbetingelser. For eksempel:
1. Trykinducerede faseovergange :Nogle faste stoffer kan gennemgå faseovergange under højt tryk, hvilket fører til ændringer i deres opløselighed. For eksempel udviser kulstof en faseovergang fra grafit til diamant under ekstremt højt tryk, hvilket væsentligt påvirker dets opløselighed i visse opløsningsmidler.
2. Amorfe faste stoffer :Amorfe faste stoffer, som mangler en veldefineret krystalstruktur, kan vise en let stigning i opløselighed med stigende tryk. Dette skyldes, at tryk kan favorisere opløsningen af amorfe faste stoffer ved at nedbryde deres uregelmæssige molekylære arrangementer.
3. Ioniske faste stoffer :I visse tilfælde kan højt tryk påvirke opløseligheden af ioniske faste stoffer ved at ændre dissociationen af deres ioner. For eksempel kan opløseligheden af nogle tungtopløselige salte, såsom calciumcarbonat, forbedres under højt tryk på grund af ændringer i ioniseringsligevægten.
Det er værd at bemærke, at disse effekter typisk observeres ved ekstremt høje trykforhold, ofte ud over dem, man støder på i hverdagssituationer eller i de fleste laboratoriemiljøer. Under normale atmosfæriske tryk og temperaturforhold er virkningen af tryk på opløseligheden af faste stoffer normalt ubetydelig.
Sidste artikelNævn nogle af de mest sure væsker eller stoffer, der findes i hverdagen.?
Næste artikelGassers og væskers reaktioner på tryk?
 Varme artikler
Varme artikler
-
 Organiseret kaos i enzymkomplekset – overraskende indsigt og nye perspektiverDe ti enzymatiske komponenter i AROM-komplekset på arbejde, katalyserer de kemiske reaktioner skitseret i baggrunden. Kredit:Max Planck Society For proteinmolekyler, der bidrager til stofskiftet,
Organiseret kaos i enzymkomplekset – overraskende indsigt og nye perspektiverDe ti enzymatiske komponenter i AROM-komplekset på arbejde, katalyserer de kemiske reaktioner skitseret i baggrunden. Kredit:Max Planck Society For proteinmolekyler, der bidrager til stofskiftet, -
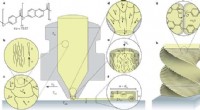 3D-udskrivning hierarkiske flydende krystal-polymerstrukturerUdskrivning af hierarkiske termotrope LCPer ved hjælp af fusioneret deponeringsmodellering. a) korte stavlignende polymerkæder dannet af en aromatisk tilfældig copolymer bestående af de stive monomere
3D-udskrivning hierarkiske flydende krystal-polymerstrukturerUdskrivning af hierarkiske termotrope LCPer ved hjælp af fusioneret deponeringsmodellering. a) korte stavlignende polymerkæder dannet af en aromatisk tilfældig copolymer bestående af de stive monomere -
 Opskalering af biohybride systemer til syntetisering af brændstoffer, kemikalierVisualisering af en bakteriecelle (øverst), der omdanner organiske molekylers kemiske energi til elektroner, der overføres til en uorganisk tinoxidkatalysator (nederst) via molekylære ledninger indlej
Opskalering af biohybride systemer til syntetisering af brændstoffer, kemikalierVisualisering af en bakteriecelle (øverst), der omdanner organiske molekylers kemiske energi til elektroner, der overføres til en uorganisk tinoxidkatalysator (nederst) via molekylære ledninger indlej -
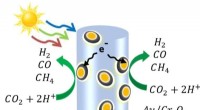 Soldrevet kemi bruger kuldioxid og vand til at fremstille råmaterialer til brændstoffer, kemikalie…Et diagram over halvledernannotrådene lavet af indium, gallium og nitrogen - dekoreret med guld- og kromoxidnanopartikler. Når lyset rammer nanotråden, frigør det elektroner og de positivt ladede hull
Soldrevet kemi bruger kuldioxid og vand til at fremstille råmaterialer til brændstoffer, kemikalie…Et diagram over halvledernannotrådene lavet af indium, gallium og nitrogen - dekoreret med guld- og kromoxidnanopartikler. Når lyset rammer nanotråden, frigør det elektroner og de positivt ladede hull
- Hvad sker der, hvis der er utilstrækkelig tilførsel af ilt under forbrændingen af et kulbrinte?…
- Ingeniører viser, hvordan wolframoxid kan bruges som katalysator i bæredygtige kemiske omdannelser
- Baby pterodactyler kunne flyve fra fødslen
- Bioplast indeholder stoffer, der er lige så giftige som dem i almindelig plast
- Hvad er en anden fætter? Optrævling af stamtræet
- Hvordan indigo pigment kan bruges i elektronik


