Hvorfor gruppe 17 grundstoffer er stærke ikke-metaller, mens 1-metaller?
Gruppe 1-metaller :Disse grundstoffer er placeret længst til venstre i det periodiske system og er kendt som alkalimetaller. De er meget reaktive og danner monoatomiske ioner. Alkalimetaller har en lav elektronegativitet, hvilket betyder, at de har en stærk tendens til at miste elektroner. Dette gør dem meget reaktive, da de let afgiver deres yderste elektron til andre grundstoffer.
Sammenligning :
- Elektronegativitet :Gruppe 17 grundstoffer har en høj elektronegativitet, mens gruppe 1 metaller har en lav elektronegativitet.
- Reaktivitet :Gruppe 17-elementer er meget reaktive og danner diatomiske molekyler, mens gruppe 1-elementer er meget reaktive og danner monoatomiske ioner.
- Ioniseringsenergi :Gruppe 17-elementer har en høj ioniseringsenergi, mens gruppe 1-elementer har en lav ioniseringsenergi.
- Smelte- og kogepunkter :Gruppe 17 grundstoffer har lave smelte- og kogepunkter, mens gruppe 1-metaller har høje smelte- og kogepunkter.
Sammenfattende er hovedårsagen til, at gruppe 17-elementer er stærke ikke-metaller, mens gruppe 1-metaller er meget reaktive metaller, på grund af deres forskelle i elektronegativitet.
 Varme artikler
Varme artikler
-
 Katalysator omdanner plastaffald til værdifulde ingredienser ved lav temperaturKredit:Osaka City University For første gang, forskere har brugt en ny katalysatorproces til at genbruge en type plastik, der findes i alt fra indkøbsposer og fødevareemballage til legetøj og elek
Katalysator omdanner plastaffald til værdifulde ingredienser ved lav temperaturKredit:Osaka City University For første gang, forskere har brugt en ny katalysatorproces til at genbruge en type plastik, der findes i alt fra indkøbsposer og fødevareemballage til legetøj og elek -
 Mindre er mere, når det kommer til at forudsige molekylers ledningsevneUChicago-studerende Manas Sajjan, venstre, og prof. David Mazziotti, holde en model, der viser et molekyle, hvorpå de testede en bedre tilgang til at forudsige ledningsevne. Kredit:Jean Lachat/Univers
Mindre er mere, når det kommer til at forudsige molekylers ledningsevneUChicago-studerende Manas Sajjan, venstre, og prof. David Mazziotti, holde en model, der viser et molekyle, hvorpå de testede en bedre tilgang til at forudsige ledningsevne. Kredit:Jean Lachat/Univers -
 Det perfekte shot af espresso hver gang med kemiForfining af espressobrygningsprocessen kan resultere i sparede penge og konsekvent velsmagende kaffe. Kredit:Charlie Litchfield, University of Oregon Den gennemsnitlige amerikaner drikker mere en
Det perfekte shot af espresso hver gang med kemiForfining af espressobrygningsprocessen kan resultere i sparede penge og konsekvent velsmagende kaffe. Kredit:Charlie Litchfield, University of Oregon Den gennemsnitlige amerikaner drikker mere en -
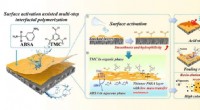 Nye syrefaste membraner til spildevandsrensning udvikletSkematisk mekanisme til fremstilling af syrefast nanofiltreringsmembran og dens overlegne separationsydelse. Kredit:CAO Yang En forskergruppe ledet af prof. Wan Yinhua fra Institute of Process Eng
Nye syrefaste membraner til spildevandsrensning udvikletSkematisk mekanisme til fremstilling af syrefast nanofiltreringsmembran og dens overlegne separationsydelse. Kredit:CAO Yang En forskergruppe ledet af prof. Wan Yinhua fra Institute of Process Eng
- Hun forsvinder fra præsidentens sprog
- Chikane inden for arkæologi forekommer med epidemiske hastigheder
- Australien forstærker teknologien til nedkæmpelse af drone
- Koralrøde alger har eksisteret i 300 millioner år længere end tidligere antaget
- Dens regnende diamanter over hele universet, tyder forskning på
- Hvad udvikler en zygote i planter?


