Hvordan opløses svovl i olie?
Når temperaturen stiger, øges opløseligheden af svovl i olie også. Dette skyldes, at højere temperaturer giver mere energi til at overvinde de intermolekylære kræfter, der holder svovlmolekylerne sammen.
Koncentrationen af svovl i olien påvirker også dens opløselighed. Når koncentrationen af svovl stiger, falder opløseligheden af svovl i olien. Dette skyldes, at svovlmolekylerne konkurrerer med hinanden om solvatisering af oliemolekylerne.
Ud over disse faktorer kan opløseligheden af svovl i olie også påvirkes af tilstedeværelsen af andre urenheder, såsom vand eller salte. Disse urenheder kan konkurrere med svovl om solvatisering af oliemolekylerne, hvilket reducerer opløseligheden af svovl.
Her er en trin-for-trin forklaring på, hvordan svovl opløses i olie:
1. Svovlmolekyler kommer i kontakt med olien.
2. Svovlmolekylerne interagerer med oliemolekylerne gennem van der Waals-kræfter.
3. Oliemolekylerne omgiver svovlmolekylerne og danner en solvatiseringsskal.
4. De solvatiserede svovlmolekyler er spredt gennem olien.
5. Svovlmolekylerne forbliver opløst i olien, indtil de fjernes ved en kemisk reaktion eller en fysisk proces såsom fordampning.
Sidste artikelHvad er en syre plus et carbonat?
Næste artikelHvordan fremstiller man 7M svovlsyre ud fra koncentreret syre?
 Varme artikler
Varme artikler
-
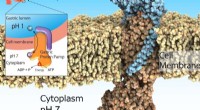 Forskere etablerer krystalstruktur af gastrisk protonpumpeDen gastriske protonpumpe, også kendt som H+, K+-ATPase, udtrykkes på overfladen af maven for at udskille mavesyren, der er uundværlig for fordøjelsen af proteiner i maden. Imidlertid, for meget s
Forskere etablerer krystalstruktur af gastrisk protonpumpeDen gastriske protonpumpe, også kendt som H+, K+-ATPase, udtrykkes på overfladen af maven for at udskille mavesyren, der er uundværlig for fordøjelsen af proteiner i maden. Imidlertid, for meget s -
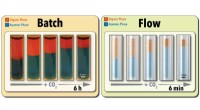 Grøn tilgang fremskynder procesoptimering og hentning af omskiftelige opløsningsmidlerKredit:North Carolina State University Forskere ved North Carolina State University har demonstreret en ny, grøn teknologi til både accelereret screening og hentning af omskiftelige opløsningsmidl
Grøn tilgang fremskynder procesoptimering og hentning af omskiftelige opløsningsmidlerKredit:North Carolina State University Forskere ved North Carolina State University har demonstreret en ny, grøn teknologi til både accelereret screening og hentning af omskiftelige opløsningsmidl -
 Upcycling svampet plastikskum fra sko, madrasser og isoleringPolyurethanskum er notorisk vanskelige at genbruge og ender på lossepladser eller i produkter med lavere værdi, såsom syntetiske tæpper. Kredit:Northwestern University Forskere har udviklet en ny
Upcycling svampet plastikskum fra sko, madrasser og isoleringPolyurethanskum er notorisk vanskelige at genbruge og ender på lossepladser eller i produkter med lavere værdi, såsom syntetiske tæpper. Kredit:Northwestern University Forskere har udviklet en ny -
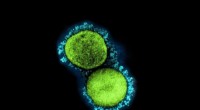 Åndeprøver kan snuse til COVID-19Et transmissionselektronmikrograf af SARS-CoV-2-viruspartikler (UK B.1.1.7-variant), isoleret fra en patientprøve og dyrket i cellekultur. Kredit:NIAID Siden maj 2021 har chauffører, der krydser S
Åndeprøver kan snuse til COVID-19Et transmissionselektronmikrograf af SARS-CoV-2-viruspartikler (UK B.1.1.7-variant), isoleret fra en patientprøve og dyrket i cellekultur. Kredit:NIAID Siden maj 2021 har chauffører, der krydser S
- Er din hund aggressiv? En dyrlæge forklarer 'rage syndrom'
- Undersøgelse løser hvorfor drikke giver dig munchies
- Da de første varmblodede dinosaurer strejfede rundt på Jorden
- Jordens grønnere nærmer sig sin grænse
- I 2040, kunstig intelligens kunne hæmme den nukleare stabilitet
- Mickey og matematik? Disney lancerer uddannelsesapps


