Når opløst i vand, hvilke forbindelser er bedre ledere af elektricitet?
Ioniske forbindelser er sammensat af positivt ladede ioner (kationer) og negativt ladede ioner (anioner). Når disse forbindelser opløses i vand, adskilles ionerne og bliver omgivet af vandmolekyler. Vandmolekylerne interagerer med ionerne og danner et hydreringslag omkring hver ion. Dette hydreringslag hjælper med at stabilisere ionerne og forhindre dem i at rekombinere.
De adskilte ioner i vandet kan bevæge sig frit, og de kan føre en elektrisk strøm. Jo flere ioner der er til stede i vandet, jo bedre kan opløsningen lede elektricitet.
I modsætning hertil kovalente forbindelser , såsom sukker (C12H22O11), er dårlige ledere af elektricitet, når de opløses i vand. Kovalente forbindelser er sammensat af atomer, der deler elektroner, og disse elektroner er ikke frie til at bevæge sig. Når kovalente forbindelser opløses i vand, adskilles molekylerne ikke til ioner, så der er ingen frie ioner til at føre en elektrisk strøm.
 Varme artikler
Varme artikler
-
 Spinat brugt i neutronundersøgelser kunne afsløre hemmeligheden bag stærkere plantevækstUppsala Universitets forsker Marvin Seibert bruger neutroner til at studere RuBisCO, et rigeligt enzym, der er essentielt for livet på jorden. Hans team håber at bestemme, hvordan planter og andre org
Spinat brugt i neutronundersøgelser kunne afsløre hemmeligheden bag stærkere plantevækstUppsala Universitets forsker Marvin Seibert bruger neutroner til at studere RuBisCO, et rigeligt enzym, der er essentielt for livet på jorden. Hans team håber at bestemme, hvordan planter og andre org -
 Adskillelse af gasser ved hjælp af fleksible molekylsigterMolekylærsigternes dynamiske natur og fleksibilitet er afgørende for at forstå deres ydeevne til transport af små molekyler. Kredit:University of Liverpool Forskere ved University of Liverpool og
Adskillelse af gasser ved hjælp af fleksible molekylsigterMolekylærsigternes dynamiske natur og fleksibilitet er afgørende for at forstå deres ydeevne til transport af små molekyler. Kredit:University of Liverpool Forskere ved University of Liverpool og -
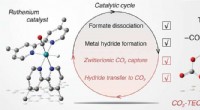 Overvågning af mellemprodukter i CO2 -omdannelse til formiat ved hjælp af metalkatalysatorTriethanolamin (TEOA) er aktivt engageret i centrale reaktionstrin i den fotokatalytiske cyklus til omdannelse af kuldioxid (CO2) af rutheniumcarbonylkomplekser. Kredit: Journal of the American Chemic
Overvågning af mellemprodukter i CO2 -omdannelse til formiat ved hjælp af metalkatalysatorTriethanolamin (TEOA) er aktivt engageret i centrale reaktionstrin i den fotokatalytiske cyklus til omdannelse af kuldioxid (CO2) af rutheniumcarbonylkomplekser. Kredit: Journal of the American Chemic -
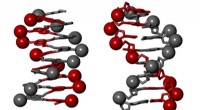 Biomimetisk kemi - DNA-mimiker overliste viralt enzymRepræsentationer af en B-DNA dobbelt helix og en enkelt spiralformet foldamer efterligner. Kredit:Ivan Huc, LMU Ikke alene kan syntetiske molekyler efterligne strukturerne i deres biologiske model
Biomimetisk kemi - DNA-mimiker overliste viralt enzymRepræsentationer af en B-DNA dobbelt helix og en enkelt spiralformet foldamer efterligner. Kredit:Ivan Huc, LMU Ikke alene kan syntetiske molekyler efterligne strukturerne i deres biologiske model
- Går du amok? Tyrkiet ser ud til at pistacienødder opvarmer ny øko-by
- Fysikere demonstrerer afblandingsadfærd af roterende partikler
- Sådan fisker du efter crayfish & crawdads i Oregon
- Kenyas domstol blokerer Østafrikas første kulværk
- Hvorfor Kina er ved at fremstå som førende inden for bæredygtigt og økologisk landbrug
- Forskere får ny indsigt i et dynamisk protein målrettet mod kræftbehandling


