Hvad er stærkere hydrogenbinding eller kemisk binding?
Kemiske bindinger involverer deling eller overførsel af elektroner mellem atomer, hvilket resulterer i en stærk elektrostatisk tiltrækning, der holder atomerne sammen. Styrken af en kemisk binding afhænger af forskellige faktorer, såsom elektronegativiteten af de involverede atomer, bindingsrækkefølgen og tilstedeværelsen af ensomme elektronpar.
På den anden side er hydrogenbindinger intermolekylære kræfter, der opstår mellem et brintatom, der er kovalent bundet til et elektronegativt atom (såsom N, O eller F) og et andet elektronegativt atom med et ensomt elektronpar. Hydrogenbindinger dannes på grund af den elektrostatiske tiltrækning mellem den partielle positive ladning på brintatomet og den partielle negative ladning på det elektronegative atom.
Mens hydrogenbindinger kan bidrage væsentligt til den overordnede struktur og stabilitet af molekyler og supramolekylære samlinger, er de typisk svagere end kovalente eller ioniske bindinger. Styrken af en brintbinding er påvirket af faktorer såsom elektronegativiteten af de involverede atomer, afstanden mellem hydrogenbindingsdonoren og acceptoren og tilstedeværelsen af konkurrerende hydrogenbindingsinteraktioner.
Sammenfattende er kemiske bindinger, såsom kovalente og ioniske bindinger, generelt stærkere end hydrogenbindinger.
Sidste artikelHvad er stoffet eller blandingen i en guldring?
Næste artikelHvad produceres kuldioxid ved begge processer?
 Varme artikler
Varme artikler
-
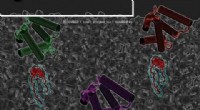 Afsløring af en nøglemekanisme i samlingen af Avian Sarcoma Virus, en 100-årig onkogen virus, d…Kredit:University of Alabama i Birmingham Et vigtigt skridt i retroviral vækst inde i en celle, som beskrevet af Jamil Saad, Ph.d., og kolleger, er portrætteret på forsiden af The Journal of Bi
Afsløring af en nøglemekanisme i samlingen af Avian Sarcoma Virus, en 100-årig onkogen virus, d…Kredit:University of Alabama i Birmingham Et vigtigt skridt i retroviral vækst inde i en celle, som beskrevet af Jamil Saad, Ph.d., og kolleger, er portrætteret på forsiden af The Journal of Bi -
 Løsning af problemet:Organisk damp inducerer opløsning af molekylære salteForskere fra Institute of Industrial Science, University of Tokyo, finder ud af, at organiske dampe kan inducere opløsning af molekylære salte (dvs. organisk delikvence), svarende til vanddamp-inducer
Løsning af problemet:Organisk damp inducerer opløsning af molekylære salteForskere fra Institute of Industrial Science, University of Tokyo, finder ud af, at organiske dampe kan inducere opløsning af molekylære salte (dvs. organisk delikvence), svarende til vanddamp-inducer -
 Mysteriet om en Picasso afsløret af videnskabsmændKredit:Museu Picasso, Barcelona. Foto:Gasull Fotografia I sommeren 1917 i Barcelona, Picasso arbejdede på fire malerier inspireret af Ballets Russes, bruge et lignende sæt materiale til dem alle,
Mysteriet om en Picasso afsløret af videnskabsmændKredit:Museu Picasso, Barcelona. Foto:Gasull Fotografia I sommeren 1917 i Barcelona, Picasso arbejdede på fire malerier inspireret af Ballets Russes, bruge et lignende sæt materiale til dem alle, -
 Programmering af pH:Ny teknik kan fremskynde DNA-synteseKredit:Pixabay/CC0 Public Domain pH - koncentrationen af protoner i en vandig opløsning - angiver, hvor sur opløsningen er. Det regulerer en bred vifte af naturlige og konstruerede kemiske proces
Programmering af pH:Ny teknik kan fremskynde DNA-synteseKredit:Pixabay/CC0 Public Domain pH - koncentrationen af protoner i en vandig opløsning - angiver, hvor sur opløsningen er. Det regulerer en bred vifte af naturlige og konstruerede kemiske proces
- Hvorfor er det ikke altid vores skyld, hvis vi vælger usunde fødevarer
- Ingeniører kigger ind i nanopartikler for at udforske, hvordan deres form forbedrer energilagring
- Hvad Love Island kan fortælle os om kærlighedens historie
- Ny indsigt i de koptiske klostres rolle i økonomien i det sene antikke Egypten
- Ny nanobead -tilgang kan revolutionere sensorteknologi
- Første størrelsesbaserede kromatografiteknik til undersøgelse af levende celler


