Hvad er mere opløseligt i vand NaF eller MgO?
Opløseligheden af en forbindelse i vand afhænger af polariteten af forbindelsen og opløsningsmidlets evne til at opløse forbindelsen. NaF er en ionforbindelse, hvilket betyder, at den består af positivt og negativt ladede ioner. Vand er et polært opløsningsmiddel, hvilket betyder, at det har en positiv ende og en negativ ende. Den positive ende af vandmolekylet vil blive tiltrukket af de negative ioner i NaF, og den negative ende af vandmolekylet vil blive tiltrukket af de positive ioner i NaF. Denne tiltrækning mellem vandmolekylerne og ionerne i NaF vil få NaF til at opløses i vand.
MgO er også en ionisk forbindelse, men den er mindre opløselig i vand end NaF. Dette skyldes, at ionerne i MgO er stærkere tiltrukket af hinanden end ionerne i NaF. Den stærkere tiltrækning mellem ionerne i MgO betyder, at det er sværere for vandmolekylerne at opløse forbindelsen, og derfor er MgO mindre opløseligt i vand.
Sidste artikelEr 3 Tetraphenylcyclopentadienon opløseligt i methanol?
Næste artikelEr vand mere polært end methanol?
 Varme artikler
Varme artikler
-
 Lille tornado øger ydeevnen af elektrospray-ioniseringsmassespektrometriDRILL-enheden er forbundet til et massespektrometer for at sortere ladede dråber og forbedre desolvation af ioniserede biomolekyler til analyse. Enheden kræver ingen ændring af massespektrometeret, og
Lille tornado øger ydeevnen af elektrospray-ioniseringsmassespektrometriDRILL-enheden er forbundet til et massespektrometer for at sortere ladede dråber og forbedre desolvation af ioniserede biomolekyler til analyse. Enheden kræver ingen ændring af massespektrometeret, og -
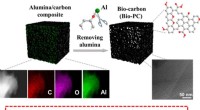 Grænseflade-induceret fremstilling af porøst kulstof med forbedrede iboende aktive stederUnder ikke-oxidationsbetingelser blev in-situ dannet aluminiumoxid/carbon-grænseflade udviklet som en vugge til generering af tilgængelige aktive steder. Det kan også justere den porøse struktur af re
Grænseflade-induceret fremstilling af porøst kulstof med forbedrede iboende aktive stederUnder ikke-oxidationsbetingelser blev in-situ dannet aluminiumoxid/carbon-grænseflade udviklet som en vugge til generering af tilgængelige aktive steder. Det kan også justere den porøse struktur af re -
 Forskere udnytter carbenernes kraft til at fremstille stoffer nemmere og mere sikkertKredit:CC0 Public Domain På trods af at de er nogle af de mest alsidige byggesten i organisk kemi, kan forbindelser kaldet carbener være for varme til at håndtere. I laboratoriet undgår kemikere of
Forskere udnytter carbenernes kraft til at fremstille stoffer nemmere og mere sikkertKredit:CC0 Public Domain På trods af at de er nogle af de mest alsidige byggesten i organisk kemi, kan forbindelser kaldet carbener være for varme til at håndtere. I laboratoriet undgår kemikere of -
 Aflytning af australske edderkoppers hemmeligheder unikt silkeKurve-spindderkoppen i sin naturlige form med sin unikke hummerpottespind og silke, som nu er blevet afsløret som enestående robust. Kredit:Professor Mark Elgar, University of Melbourne Et interna
Aflytning af australske edderkoppers hemmeligheder unikt silkeKurve-spindderkoppen i sin naturlige form med sin unikke hummerpottespind og silke, som nu er blevet afsløret som enestående robust. Kredit:Professor Mark Elgar, University of Melbourne Et interna
- Uber lancerer elcykler, scootere i Paris
- Smart øretelefon vil måle, hvordan astronauter sover
- Hvorfor har sukker en stærkere intermolekylær kraft end ammoniak?
- De fleste forskere er enige om, at en anden pangea er sikker,
- Undersøgelse identificerer bedre, billigere måder at dæmme op for arsenforgiftning i Bangladesh
- Når citroner giver dig liv:Herpetofauna-tilpasning til citrusplantager i Belize


