Hvor mange natriumatomer er repræsenteret i 15,59 g fosfat, Na3PI4?
1. Beregn molmassen af Na3PI4:
- Molær masse af Na =22,99 g/mol
- Molær masse af P =30,97 g/mol
- Molær masse af I =126,90 g/mol
Den molære masse af Na3PI4 =(3 x 22,99 g/mol) + (1 x 30,97 g/mol) + (4 x 126,90 g/mol) =380,69 g/mol
2. Beregn antallet af mol Na3PI4 i 15,59 g:
- Mol af Na3PI4 =Masse / Molær masse
- Mol Na3PI4 =15,59 g / 380,69 g/mol =0,04096 mol
3. Beregn antallet af natriumatomer pr. mol Na3PI4:
- Der er 3 natriumatomer pr. mol Na3PI4.
4. Beregn det samlede antal natriumatomer i 15,59 g Na3PI4:
- Samlet antal natriumatomer =(mol Na3PI4) x (Antal natriumatomer pr. mol Na3PI4)
- Samlet antal natriumatomer =0,04096 mol x 3 atomer/mol =0,12288 atomer
Derfor er der cirka 0,12288 natriumatomer repræsenteret i 15,59 g fosfat, Na3PI4.
 Varme artikler
Varme artikler
-
 Nye fingeraftryk tilføjet til kemisk identifikationsdatabaseNIST -forskningskemiker Kelly Telu injicerer en prøve i et massespektrometer, et laboratorieinstrument, som forskere bruger til at identificere ukendte kemiske forbindelser. Kredit:M. Delorme/NIST
Nye fingeraftryk tilføjet til kemisk identifikationsdatabaseNIST -forskningskemiker Kelly Telu injicerer en prøve i et massespektrometer, et laboratorieinstrument, som forskere bruger til at identificere ukendte kemiske forbindelser. Kredit:M. Delorme/NIST -
 Den kommende forstyrrelse af OLED-teknologierEn organisk lysemitterende diode (OLED) er en selvlysende, tyndfilmskomponent lavet af organiske halvledende materialer. Da der ikke er behov for siliciumchips, kun pigmentmolekyler disse lys kan prod
Den kommende forstyrrelse af OLED-teknologierEn organisk lysemitterende diode (OLED) er en selvlysende, tyndfilmskomponent lavet af organiske halvledende materialer. Da der ikke er behov for siliciumchips, kun pigmentmolekyler disse lys kan prod -
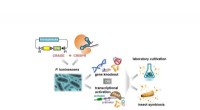 Udtrækning af hemmeligheder bag sekundære metabolitterVed at kombinere CRAGE- og CRISPR-teknologier har forskerne en meget nemmere metode til at karakterisere sekundære metabolitter. Kredit:Cell Chemical Biology (2021). DOI:10.1016/j.chembiol.2021.08.009
Udtrækning af hemmeligheder bag sekundære metabolitterVed at kombinere CRAGE- og CRISPR-teknologier har forskerne en meget nemmere metode til at karakterisere sekundære metabolitter. Kredit:Cell Chemical Biology (2021). DOI:10.1016/j.chembiol.2021.08.009 -
 Befugtende ejendom af Li metal med grafitKontaktvinkeleksperimenter af Li-metal og grafitmaterialer:(a-c) stærkt orienteret pyrolytisk grafit (HOPG); (d-f) porøst carbonpapir (PCP); (g-i) lithieret porøst carbonpapir (litieret PCP). Kredit:©
Befugtende ejendom af Li metal med grafitKontaktvinkeleksperimenter af Li-metal og grafitmaterialer:(a-c) stærkt orienteret pyrolytisk grafit (HOPG); (d-f) porøst carbonpapir (PCP); (g-i) lithieret porøst carbonpapir (litieret PCP). Kredit:©
- Hvad er virkningen af PH på levende organismer?
- Globalt projekt observerer sjældne meteorregn og meteoritfald
- Boeing leverer den første 787 i et år
- Nye undersøgelser af gammel beton kunne lære os at gøre som romerne
- Smeltende sne hjælper med at absorbere kuldioxid
- Hvordan fødevarebanker hjælper amerikanere, der har problemer med at få nok at spise


