Hvordan ville MG ændre sig for at få ædle gasstruktur?
Her er hvorfor:
* ædle gaskonfiguration: Ædle gasser er elementerne i gruppe 18 i den periodiske tabel. De er meget stabile, fordi de har en fuld ydre skal af elektroner. For eksempel har Neon (NE) konfigurationen 2, 8.
* Magnesiums konfiguration: Magnesium har kun to elektroner i sin ydre skal.
* taber elektroner: Ved at miste sine to ydre elektroner opnår magnesium den samme elektronkonfiguration som neon, som er en stabil konfiguration.
Når magnesium mister disse to elektroner, danner det en magnesiumion (mg²⁺) . Denne ion har en +2 ladning, fordi den har mistet to negativt ladede elektroner.
Fortæl mig, hvis du har flere spørgsmål!
Sidste artikelHvad bruger til berylium?
Næste artikelHvad opløses cyclohexanol bedst i?
 Varme artikler
Varme artikler
-
 Syntetiske fysiologer konstruerer ny receptor slukket med grønt lysMed den nyudviklede receptor, grøn betyder stop for visse cellulære processer. Kredit:IST Austria Optogenetik, tilgangen til at bruge lys til at styre centrale processer, har revolutioneret, hvord
Syntetiske fysiologer konstruerer ny receptor slukket med grønt lysMed den nyudviklede receptor, grøn betyder stop for visse cellulære processer. Kredit:IST Austria Optogenetik, tilgangen til at bruge lys til at styre centrale processer, har revolutioneret, hvord -
 Ny katalysator med en dobbelt funktion til brint- og plastproduktionBochum -teamet:Dulce Morales, Steffen Cychy, Stefan Barwe, Dennis Hiltrop, Martin Muhler og Wolfgang Schuhmann (fra venstre). Kredit:RUB, Marquard Kemikere ved Ruhr-Universität Bochum (RUB) har ud
Ny katalysator med en dobbelt funktion til brint- og plastproduktionBochum -teamet:Dulce Morales, Steffen Cychy, Stefan Barwe, Dennis Hiltrop, Martin Muhler og Wolfgang Schuhmann (fra venstre). Kredit:RUB, Marquard Kemikere ved Ruhr-Universität Bochum (RUB) har ud -
 Madprotein kan fjerne skarphed og bitterhed i ekstra jomfru olivenolieKredit:CC0 Public Domain Forskere har undersøgt de potentielle sundhedsfremmende kvaliteter af ekstra jomfru olivenolie (EVOO) i årtier, herunder dets mulige medicinske værdi til forebyggelse af k
Madprotein kan fjerne skarphed og bitterhed i ekstra jomfru olivenolieKredit:CC0 Public Domain Forskere har undersøgt de potentielle sundhedsfremmende kvaliteter af ekstra jomfru olivenolie (EVOO) i årtier, herunder dets mulige medicinske værdi til forebyggelse af k -
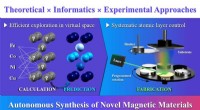 Mod autonom forudsigelse og syntese af nye magnetiske materialerKredit:Tokyo University of Science I materialevidenskab udforskes kandidater til nye funktionelle materialer normalt på en trial-and-error måde gennem beregninger, syntetiske metoder og materialean
Mod autonom forudsigelse og syntese af nye magnetiske materialerKredit:Tokyo University of Science I materialevidenskab udforskes kandidater til nye funktionelle materialer normalt på en trial-and-error måde gennem beregninger, syntetiske metoder og materialean
- Mauna Loa Fakta for Kids
- Forskere demonstrerer hastighed, præcision af in situ planetarisk dating enhed
- Japan sender tiltrængte forsyninger til rumstationen
- Hvor bling gør os til mennesker
- Gældsbelastede virksomheder er mere tilbøjelige til at risikere arbejdssikkerhed
- Overraskende lighed mellem stribede sorte huller og høj temperatur superledere


