Hvad opløses cyclohexanol bedst i?
Her er hvorfor:
* "Ligesom opløser som" Princip: Polære molekyler har en tendens til at opløses i andre polære molekyler, og ikke -polære molekyler har en tendens til at opløses i andre ikke -polære molekyler.
* Hydrogenbinding: Hydroxylgruppen i cyclohexanol kan danne hydrogenbindinger med andre polære molekyler, hvilket yderligere øger dens opløselighed.
Eksempler på gode opløsningsmidler til cyclohexanol:
* Vand: Vand er et meget polært opløsningsmiddel og kan danne hydrogenbindinger med cyclohexanol. Cyclohexanol er imidlertid ikke helt blandbar med vand, hvilket betyder, at den ikke opløses fuldt ud i alle proportioner.
* ethanol: Ethanol er også et polært opløsningsmiddel og kan danne hydrogenbindinger med cyclohexanol. Det er mere blandbart med cyclohexanol end vand.
* methanol: En anden polær alkohol, der er et godt opløsningsmiddel til cyclohexanol.
* acetone: Acetone er et polært opløsningsmiddel med en ketongruppe, og det kan danne dipol-dipol-interaktioner med cyclohexanol.
Cyclohexanol opløses dårligt i ikke -polære opløsningsmidler som:
* Hexan
* Diethylether
* Toluen
Bemærk: Den nøjagtige opløselighed af cyclohexanol afhænger af det specifikke opløsningsmiddel og temperaturen.
Sidste artikelHvordan ville MG ændre sig for at få ædle gasstruktur?
Næste artikelHvad er forskellen mellem syresalt og normalt salt?
 Varme artikler
Varme artikler
-
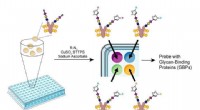 Ny TSRI-metode fremskynder undersøgelser af kulhydratbiologiEn ny metode til at samle et glycan-array. Kredit:Wu Lab / Scripps Research Institute 28. februar, 2018 - Næsten alle levende celler er besat med forgrenede kulhydratkæder kaldet glykaner. Glykane
Ny TSRI-metode fremskynder undersøgelser af kulhydratbiologiEn ny metode til at samle et glycan-array. Kredit:Wu Lab / Scripps Research Institute 28. februar, 2018 - Næsten alle levende celler er besat med forgrenede kulhydratkæder kaldet glykaner. Glykane -
 Team opdager dobbelt helixstruktur i syntetisk makromolekyleLou Madsen (tv.) er lektor i Kemisk Institut og har ledet et internationalt tværfagligt samarbejde om opdagelsen af den dobbelte helixstruktur af en polymer kaldet PBDT. Ying Wang (th.) er en tidlig
Team opdager dobbelt helixstruktur i syntetisk makromolekyleLou Madsen (tv.) er lektor i Kemisk Institut og har ledet et internationalt tværfagligt samarbejde om opdagelsen af den dobbelte helixstruktur af en polymer kaldet PBDT. Ying Wang (th.) er en tidlig -
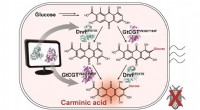 Mikrobiel produktion af et naturligt rødt farvestof karminsyreEn skematisk biosyntesevej til produktion af karminsyre fra glucose. Biokemisk reaktionsanalyse og computersimuleringsassisteret enzymteknik blev brugt til at identificere og forbedre enzymerne (DnrFP
Mikrobiel produktion af et naturligt rødt farvestof karminsyreEn skematisk biosyntesevej til produktion af karminsyre fra glucose. Biokemisk reaktionsanalyse og computersimuleringsassisteret enzymteknik blev brugt til at identificere og forbedre enzymerne (DnrFP -
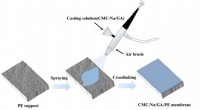 Pervaporationsmembraner viser løfte om genvinding af alkalisk spildevandEn (CMC-Na/GA)/PE-kompositmembran blev fremstillet ved spray-coating og viste fremragende egenskaber til alkalisk vandgenvinding. Kredit:Jianzhong Xia, Pei Li Industrielle processer genererer ofte
Pervaporationsmembraner viser løfte om genvinding af alkalisk spildevandEn (CMC-Na/GA)/PE-kompositmembran blev fremstillet ved spray-coating og viste fremragende egenskaber til alkalisk vandgenvinding. Kredit:Jianzhong Xia, Pei Li Industrielle processer genererer ofte
- Astronomer opdager røntgenstråleudsendende klumper udsendt fra den binære PSR B1259–63/LS 2883
- Store havobservationssatelliter begynder at levere videnskabelige data
- Transportørers usikre procedurer gør livet nemt for SIM-byttetrickstere
- Udvikling af en højenergi-opløsning, lanthanhexaborid nanotråd-baseret feltemissionspistol
- Extinction Rebellion:forstyrrelser og anholdelser kan medføre sociale forandringer
- Hvad er mikroudtryk?


