Hvor mange orbitalboks i NA?
1. Elektronkonfiguration:
* Natrium har et atomnummer på 11, hvilket betyder, at det har 11 elektroner.
* Dens elektronkonfiguration er:1S² 2s² 2p⁶ 3S¹
2. Orbitalkasser:
* 1S²: Dette repræsenterer 1s orbital, som kan indeholde maksimalt 2 elektroner. Så der er 1 Orbital Box for 1s.
* 2s²: Dette repræsenterer 2'erne orbital, også med maksimalt 2 elektroner. Der er 1 Orbital Box for 2s.
* 2p⁶: Dette repræsenterer 2p -underskaller, der har tre orbitaler (2px, 2py, 2pz). Hver orbital kan indeholde 2 elektroner, så der er 3 orbitalkasser til 2p.
* 3s¹: Dette repræsenterer 3S -orbitalen og holder 1 elektron. Der er 1 Orbital Box i 3'ere.
3. Samlede orbitalkasser:
Tilføjelse af alle orbitalkasser:1 + 1 + 3 + 1 = 6 Orbitalkasser
Derfor er der 6 orbitalkasser i et natriumatom.
Sidste artikelHar den flydende stofstilstand et større volumen end dens solide tilstand?
Næste artikelHvad er DQ i uorganisk kemi?
 Varme artikler
Varme artikler
-
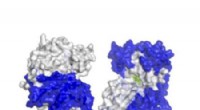 Udvikling af et enzym mod antibiotika-resistent miltbrandDette konstruerede enzym med bidder af antistof klæbet til det kan bryde kapslen af B. anthracis-bakterier fra hinanden, så immunsystemet kan kæmpe tilbage. Kredit:Tilpasset fra ACS Infectious Disea
Udvikling af et enzym mod antibiotika-resistent miltbrandDette konstruerede enzym med bidder af antistof klæbet til det kan bryde kapslen af B. anthracis-bakterier fra hinanden, så immunsystemet kan kæmpe tilbage. Kredit:Tilpasset fra ACS Infectious Disea -
 Katalysatorer til klimabeskyttelseForløber for en kobberbaseret katalysator syntetiseret ved Straubing-grenen af instituttet. Kredit:Fraunhofer IGB Hvordan kan vi nå de internationalt aftalte klimamål? Fraunhofer Institute for I
Katalysatorer til klimabeskyttelseForløber for en kobberbaseret katalysator syntetiseret ved Straubing-grenen af instituttet. Kredit:Fraunhofer IGB Hvordan kan vi nå de internationalt aftalte klimamål? Fraunhofer Institute for I -
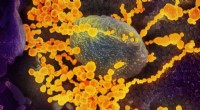 Forskere viser, at selvsteriliserende polymerer virker mod SARS-CoV-2Dette scanningselektronmikroskopbillede viser SARS-CoV-2 (runde guldobjekter), der dukker op fra overfladen af celler dyrket i laboratoriet. Kredit:NIAID-RML Forskere fra North Carolina State Un
Forskere viser, at selvsteriliserende polymerer virker mod SARS-CoV-2Dette scanningselektronmikroskopbillede viser SARS-CoV-2 (runde guldobjekter), der dukker op fra overfladen af celler dyrket i laboratoriet. Kredit:NIAID-RML Forskere fra North Carolina State Un -
 Smart blæk tilføjer nye dimensioner til 3D-udskrivningEt eksempel fra forskningen viser, hvordan et 3D-printet objekt sammensat af hydrogel (G1) kan ændre størrelse efter udskrivning. Selvom dette eksempel tjener til at demonstrere resultatet, andre obje
Smart blæk tilføjer nye dimensioner til 3D-udskrivningEt eksempel fra forskningen viser, hvordan et 3D-printet objekt sammensat af hydrogel (G1) kan ændre størrelse efter udskrivning. Selvom dette eksempel tjener til at demonstrere resultatet, andre obje
- Cheops gennemgår den endelige gennemgang før forsendelse til lanceringsstedet
- Forsøger mineraler planter med energi?
- Vurdering af luftkvalitetsprognoser for London
- Pas på kløften – betyder aldersforskel i forhold noget?
- Hvordan motorvejsbroer synger – eller stønner – i regnen for at afsløre deres helbred
- Forskere bringer optisk kommunikation på siliciumchips


