Hvorfor blev grundlag for klassificeringselementet i den periodiske tabel ændret fra atommasse til nummer?
1. Isotoper:
* Opdagelse: I begyndelsen af det 20. århundrede opdagede forskere isotoper - atomer af det samme element med forskellige atommasser på grund af det forskellige antal neutroner. Dette udfordrede ideen om, at atommasse var det definerende kendetegn for et element.
* implikation: Det blev klart, at atommasse ikke var et pålideligt grundlag for at organisere elementer, fordi elementer med lignende kemiske egenskaber kunne have forskellige atommasser på grund af isotoper.
2. Moseleys eksperimenter:
* Bidrag: Henry Moseley udførte i 1913 eksperimenter ved anvendelse af røntgenspektroskopi. Han fandt, at hyppigheden af røntgenstråler, der blev udsendt af et element, var direkte relateret til antallet af protoner i dets kerne (atomnummer).
* Betydning: Dette gav et mere grundlæggende og konsistent grundlag for klassificering af elementer, da atomnummer forblev konstant for alle isotoper af et givet element.
3. Periodisk lov og atomnummer:
* Forbindelse: Den periodiske lov, der siger, at egenskaberne ved elementer er periodiske funktioner i deres atomnumre, blev størknet af Moseleys arbejde. Denne lov forklarede de tilbagevendende mønstre for kemiske og fysiske egenskaber, der blev observeret i den periodiske tabel.
* Ny ordre: Arrangering af elementer ved at øge atomnummeret i stedet for atommasse resulterede i et mere nøjagtigt og konsekvent arrangement, der afspejlede elementernes underliggende rækkefølge.
Kortfattet:
* Opdagelsen af isotoper demonstrerede, at atommasse ikke var en pålidelig indikator for et elements identitet.
* Moseleys arbejde etablerede atomnummer som en mere grundlæggende egenskab, der bestemte et elements position i den periodiske tabel.
* Arrangering af elementer med atomnummer reflekterede bedre den periodiske lov og de tilbagevendende egenskaber ved elementer.
Skiftet fra atommasse til atomnummer var en betydelig fremgang i vores forståelse af elementerne og deres organisation, hvilket førte til en mere nøjagtig og forudsigelig periodisk tabel.
Sidste artikelHvordan bestemte du den relative atommasse af ilt?
Næste artikelHvad er den atommasse af isotoper clorine?
 Varme artikler
Varme artikler
-
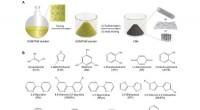 Forskerhold foreslår en effektiv strategi til fremstilling af kulstof nanomaterialerFig. 1:Fremstilling af CMer. (A) Skematisk illustration af forberedelsesprocessen for CMer. (B) Strukturer af de undersøgte SOMer til CM-forberedelsen. Kredit:University of Science and Technology of C
Forskerhold foreslår en effektiv strategi til fremstilling af kulstof nanomaterialerFig. 1:Fremstilling af CMer. (A) Skematisk illustration af forberedelsesprocessen for CMer. (B) Strukturer af de undersøgte SOMer til CM-forberedelsen. Kredit:University of Science and Technology of C -
 Vindere af $20M konkurrence laver beton for at fange kuldioxidTesla CEO Elon Musk, venstre, giver hånd med XPRIZE-grundlægger og administrerende formand Peter Diamandis under præsentationen af XPRIZE for Childrens Literacy i Los Angeles, i denne onsdag, 15. ma
Vindere af $20M konkurrence laver beton for at fange kuldioxidTesla CEO Elon Musk, venstre, giver hånd med XPRIZE-grundlægger og administrerende formand Peter Diamandis under præsentationen af XPRIZE for Childrens Literacy i Los Angeles, i denne onsdag, 15. ma -
 Nyopdaget kobber- og grafitkombination kan føre til mere effektive lithium-ion-batterierEn første af sin slags kobber- og grafitkombination, der blev opdaget i grundlæggende energiforskning ved det amerikanske energiministeriums Ames Laboratory, kunne have konsekvenser for at forbedre en
Nyopdaget kobber- og grafitkombination kan føre til mere effektive lithium-ion-batterierEn første af sin slags kobber- og grafitkombination, der blev opdaget i grundlæggende energiforskning ved det amerikanske energiministeriums Ames Laboratory, kunne have konsekvenser for at forbedre en -
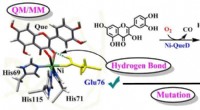 Forskere får indsigt i, hvordan enzymer opnår specifikke reaktionerSkematisk illustration af de afgørende roller af Glu76-rest i Ni-QueD. Kredit:Prof. LIs gruppe Katalytisk dioxygenaktivering og selektiv oxidativ spaltning af C-C-bindinger er blevet forsknings-ho
Forskere får indsigt i, hvordan enzymer opnår specifikke reaktionerSkematisk illustration af de afgørende roller af Glu76-rest i Ni-QueD. Kredit:Prof. LIs gruppe Katalytisk dioxygenaktivering og selektiv oxidativ spaltning af C-C-bindinger er blevet forsknings-ho
- Hvad er dinatriumphosphats rolle i fermentering?
- WHO siger, at luftforurening dræber 7 millioner om året, skærper retningslinjerne
- Faktorer der påvirker et valgsted for en vandkraftstation
- Brug af vedvarende selvlysende nanokrystaller til at skabe 3D-røntgenstråler
- Hvad viser et prisme om sollys?
- Forekommer nogen metalliske elementer normalt som gasser?


