Hvad ISS det samlede reduktionspotentiale for en celle, hvor natrium (NA) reduceres og zink (Zn) oxideret?
1. Identificer halvreaktionerne
* reduktion (ved katoden): Na⁺ (aq) + e⁻ → NA (s)
* oxidation (ved anoden): Zn (S) → Zn²⁺ (aq) + 2e⁻
2. Slå op på standardreduktionspotentialer
Du skal finde standard reduktionspotentialer (E °) for hver halvreaktion. Disse findes typisk i en tabel med standard reduktionspotentialer.
* na⁺ (aq) + e⁻ → NA (s) E ° =-2,71 V
* zn²⁺ (aq) + 2e⁻ → Zn (s) E ° =-0,76 V
3. Bestem det samlede cellepotentiale (E ° celle)
* For celle-reaktionen vendes reduktionspotentialet for oxidationen halvreaktion. Dette betyder, at vi vil bruge det negative af standardreduktionspotentialet for zinkhalvreaktionen.
* Det samlede cellepotentiale beregnes som:
E ° celle =E ° (reduktion) + E ° (oxidation)
E ° celle =-2,71 V + (+0,76 V)
E ° celle =-1,95 V
Konklusion
Det samlede reduktionspotentiale for den celle, hvor natrium reduceres, og zink oxideres -1,95 V . Denne negative værdi indikerer, at reaktionen er ikke spontan under standardbetingelser.
Sidste artikelHvad fra stof fremstilles en type atom?
Næste artikelHvorfor er der ikke kendt nogen kemisk forbindelse af helium?
 Varme artikler
Varme artikler
-
 Modermælk som medicinafgivelsesanordningKredit:CC0 Public Domain At behandle syge babyer med modermælk kan en dag blive en realitet, ifølge en artikel i Kemi- og ingeniørnyheder (C&EN), det ugentlige nyhedsmagasin fra American Chemica
Modermælk som medicinafgivelsesanordningKredit:CC0 Public Domain At behandle syge babyer med modermælk kan en dag blive en realitet, ifølge en artikel i Kemi- og ingeniørnyheder (C&EN), det ugentlige nyhedsmagasin fra American Chemica -
 Nyt kompositmateriale, der kan køle sig selv ned under ekstreme temperaturerKredit:CC0 Public Domain Et banebrydende materiale, inspireret af naturen, der kan regulere sin egen temperatur og ligeså kunne bruges til at behandle forbrændinger og hjælpe rumkapsler til at mod
Nyt kompositmateriale, der kan køle sig selv ned under ekstreme temperaturerKredit:CC0 Public Domain Et banebrydende materiale, inspireret af naturen, der kan regulere sin egen temperatur og ligeså kunne bruges til at behandle forbrændinger og hjælpe rumkapsler til at mod -
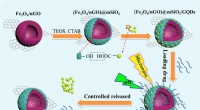 N-dopede carbonindkapslede overgangsmetalkatalysatorer for at optimere ydeevnen af zink-luftbatter…Fe@NCG blev fremstillet ved pyrolysering af opløsningsmiddelfri dannede Fechitosan-chelater og yderligere nitrogen-urinstof med lille molekyle. Den dannede katalysator udviser bifunktionel katalytisk
N-dopede carbonindkapslede overgangsmetalkatalysatorer for at optimere ydeevnen af zink-luftbatter…Fe@NCG blev fremstillet ved pyrolysering af opløsningsmiddelfri dannede Fechitosan-chelater og yderligere nitrogen-urinstof med lille molekyle. Den dannede katalysator udviser bifunktionel katalytisk -
 Genbrug af 1 kg tøj sparer 25 kg CO2, viser undersøgelseEn stigning på 10 % i brugtsalg kan spare 3 % af CO2-udledningen og 4 % af vandet. Kredit:Moda re- (Cáritas) UPCs INTEXTER har foretaget en analyse for at beregne andelen af fibre, der bruges i d
Genbrug af 1 kg tøj sparer 25 kg CO2, viser undersøgelseEn stigning på 10 % i brugtsalg kan spare 3 % af CO2-udledningen og 4 % af vandet. Kredit:Moda re- (Cáritas) UPCs INTEXTER har foretaget en analyse for at beregne andelen af fibre, der bruges i d
- Hvilken retning er herbiciderne på vej?
- Undersøgelse ændrer langvarige koncepter for celleafkodning
- Hvad er grupper af stjerner, hvis positioner på himlen ser ud til at ændre sig, når Jorden bevæg…
- Forskere hjælper med at lukke sikkerhedshullet i populær krypteringssoftware
- Hvad er fedt primært opdelt og omdannet til, så energi, der er opbevaret i disse molekyler, kan hø…
- Nye strukturelle oplysninger om funktionalisering af guld nanopartikler


