Er alle proteiner mere opløselige i ikke -polære opløsningsmidler end vand?
Her er hvorfor:
* Polaritet: Proteiner består af aminosyrer, der har forskellige sidekæder med forskellige polariteter. Nogle sidekæder er hydrofile (vandelskende), og andre er hydrofobe (vandfryd).
* struktur: Den tredimensionelle struktur af et protein påvirker også dets opløselighed. Proteiner med en høj andel af hydrofobe aminosyrer på deres overflade har en tendens til at være mindre opløselige i vand.
* ikke -polære opløsningsmidler: Mens nogle proteiner med overvejende hydrofobe overflader muligvis er mere opløselige i ikke -polære opløsningsmidler som organiske væsker, er dette ikke altid tilfældet. Den specifikke interaktion mellem proteinet og opløsningsmidlet er afgørende.
Eksempler:
* albumin: Et protein, der findes i blod, er meget opløseligt i vand på grund af dets mange hydrofile aminosyrer.
* keratin: Fundet i hår og negle er stort set hydrofobt og er derfor mere opløseligt i ikke -polære opløsningsmidler.
I resumé bestemmes opløseligheden af et protein af samspillet mellem dets aminosyresammensætning, struktur og solventets egenskaber.
Sidste artikelHvordan afhjælper du korrosion?
Næste artikelEr sukker og vand en ophængningsløsningskolloider?
 Varme artikler
Varme artikler
-
 Cellekemi oplyst af laserlysRaman mikrospektroskopi hjælper forskere med at observere cellekemi ved at fokusere en laserstråle på et sted i en celle og derefter fange lys udsendt efter interaktioner med cellulære molekyler, som
Cellekemi oplyst af laserlysRaman mikrospektroskopi hjælper forskere med at observere cellekemi ved at fokusere en laserstråle på et sted i en celle og derefter fange lys udsendt efter interaktioner med cellulære molekyler, som -
 Hvordan plankton og bakterier former havsprayEt fotografi af havspray. Kredit:Vicki H. Grassian. Når havene ebber og flyder, de resulterende bølger og stænk danner små bobler. Boblerne brister og frigiver en damp - kaldet havspray -aerosol -
Hvordan plankton og bakterier former havsprayEt fotografi af havspray. Kredit:Vicki H. Grassian. Når havene ebber og flyder, de resulterende bølger og stænk danner små bobler. Boblerne brister og frigiver en damp - kaldet havspray -aerosol - -
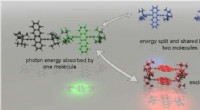 Vejen åbner for at minimere spild i solenergiopsamlingFotonenergiopdeling udføres direkte af to molekyler, ikke via en excimer-tilstand (i rødt). Singlet fissionsmaterialer skal undgå excimerdannelse for at nå det fulde potentiale til at forbedre fotovol
Vejen åbner for at minimere spild i solenergiopsamlingFotonenergiopdeling udføres direkte af to molekyler, ikke via en excimer-tilstand (i rødt). Singlet fissionsmaterialer skal undgå excimerdannelse for at nå det fulde potentiale til at forbedre fotovol -
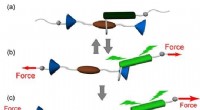 Nysgerrige sammenlåste molekyler viser dobbelt responsFigur 1. Skematisk illustration af driften af en rotaxan-baseret mekanophor, viser (a) kraftfri tilstand, (b) reversibel, og (c) irreversible svar. Forskere udforskede en mærkelig sammenkoblet molek
Nysgerrige sammenlåste molekyler viser dobbelt responsFigur 1. Skematisk illustration af driften af en rotaxan-baseret mekanophor, viser (a) kraftfri tilstand, (b) reversibel, og (c) irreversible svar. Forskere udforskede en mærkelig sammenkoblet molek
- Volvo Cars trodser et aftagende marked for at nå rekordsalg
- Forskere studerer videospilbrugsmønstre og forskellene i køn blandt unge
- En kemiker syntetiserer tinjodid i henhold til den kemiske reaktion vist nedenfor starterne med 15,0…
- Tips til multiplicering af radikaler
- Er kuren mod kræft en virus?
- Ny Saturn-masse exoplanet opdaget af astronomer


