Hvilke ioner har den samme elektronkonfiguration som Argon AR?
1. Forstå Argons elektronkonfiguration
Argon (AR) har et atomnummer på 18, hvilket betyder, at det har 18 protoner og 18 elektroner. Dens elektronkonfiguration er:
1S² 2S² 2P⁶ 3S² 3P⁶
2. Identificer ioner med det samme antal elektroner
For at have den samme elektronkonfiguration som argon skal en ion også have 18 elektroner. Dette kan opnås af:
* At vinde elektroner: Anioner (negativt ladede ioner) dannes ved at vinde elektroner.
* taber elektroner: Kationer (positivt ladede ioner) dannes ved at miste elektroner.
3. Bestem ionerne
Her er ionerne med den samme elektronkonfiguration som Argon:
* k⁺ (kaliumion): Kalium (K) har 19 elektroner. Ved at miste en elektron bliver det k⁺ med 18 elektroner.
* ca²⁺ (calciumion): Calcium (CA) har 20 elektroner. Ved at miste to elektroner bliver det Ca²⁺ med 18 elektroner.
* cl⁻ (chloridion): Chlor (CL) har 17 elektroner. Ved at få en elektron bliver det CL⁻ med 18 elektroner.
* s²⁻ (sulfidion): Svovl (er) har 16 elektroner. Ved at få to elektroner bliver det S²⁻ med 18 elektroner.
Kortfattet: Ionerne K⁺, Ca²⁺, Cl⁻ og S²⁻ har alle den samme elektronkonfiguration som Argon. Dette skyldes, at de alle har 18 elektroner, ligesom Argon.
Sidste artikelHvordan er brintbindinger brudt?
Næste artikelHvordan påvirker volumentemperaturen og densiteten gastrykket?
 Varme artikler
Varme artikler
-
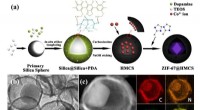 MOF@hule mesoporøse kulstofsfærer som bifunktionelle elektrokatalysatorer(a) Skematisk illustration af syntetisk procedure for ZIF@HMCS. (b) TEM-billede af ZIF@HMCS-25%. (c) HAADF-STEM-billeder og EDS-kortlægninger af ZIF@HMCS-25%. Kredit:©Science China Press Med den h
MOF@hule mesoporøse kulstofsfærer som bifunktionelle elektrokatalysatorer(a) Skematisk illustration af syntetisk procedure for ZIF@HMCS. (b) TEM-billede af ZIF@HMCS-25%. (c) HAADF-STEM-billeder og EDS-kortlægninger af ZIF@HMCS-25%. Kredit:©Science China Press Med den h -
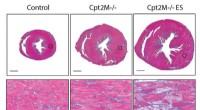 Undersøgelse viser, at fedt brændstof er nødvendigt for at vende hjertehypertrofiForskere ved Purdue University arbejder på at lære mere om forstørrelse af hjertet forårsaget af forhøjet blodtryk, diabetes, og fedme. Disse tværsnitsbilleder af et musehjerte viser den hurtige forst
Undersøgelse viser, at fedt brændstof er nødvendigt for at vende hjertehypertrofiForskere ved Purdue University arbejder på at lære mere om forstørrelse af hjertet forårsaget af forhøjet blodtryk, diabetes, og fedme. Disse tværsnitsbilleder af et musehjerte viser den hurtige forst -
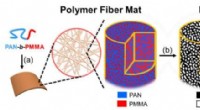 Porøs kulfiberforskning et skridt nærmere brug i bilindustrienSyntese af porøse kulfibre og belastning af MnO2. (a) En diblokcopolymer af polyacrylonitril-blok-polymethylmethacrylat (PAN-b-PMMA) spindes ind i en polymerfibermåtte. I den forstørrede udsigt, blokc
Porøs kulfiberforskning et skridt nærmere brug i bilindustrienSyntese af porøse kulfibre og belastning af MnO2. (a) En diblokcopolymer af polyacrylonitril-blok-polymethylmethacrylat (PAN-b-PMMA) spindes ind i en polymerfibermåtte. I den forstørrede udsigt, blokc -
 Forskere opnår højentropi carbid i elektrisk lysbueplasmaKredit:Tomsk Polytekniske Universitet Forskere fra Tomsk Polytechnic University har syntetiseret højentropi carbid bestående af fem forskellige metaller ved hjælp af en vakuumfri elektrisk lysbuem
Forskere opnår højentropi carbid i elektrisk lysbueplasmaKredit:Tomsk Polytekniske Universitet Forskere fra Tomsk Polytechnic University har syntetiseret højentropi carbid bestående af fem forskellige metaller ved hjælp af en vakuumfri elektrisk lysbuem
- Hvilken egenskab beviser, at molekylerne altid bevæger sig?
- Hvor mange æg æggestokk producerer reproduktivt system?
- Fra Katrina til COVID-19:Sorte samfund i New Orleans blev uforholdsmæssigt påvirket
- UNICEF:En tredjedel af verdens børn savnede fjernundervisning
- Det sydlige Ocean tager varmen fra klimaændringer
- Megacity trafik sod bidrager til global opvarmning


