Hvad sker der med en gas, hvis dens intermolekylære rum reduceres?
1. Stigning i tryk:
* Gasmolekylerne har mindre plads til at bevæge sig rundt, hvilket fører til flere kollisioner med hinanden og containerens vægge.
* Denne øgede kollisionshastighed betyder et højere tryk.
2. Potentiale for likvidation:
* Når det intermolekylære rum falder, bliver de attraktive kræfter mellem molekyler mere markante.
* Hvis trykket og/eller temperaturen er lavt nok, kan gassen kondensere til en væske. Dette skyldes, at molekylerne er tæt nok til at overvinde deres kinetiske energi og danne en flydende tilstand.
3. Ændring i densitet:
* Gasens densitet øges, når molekylerne er pakket tættere sammen.
4. Ændring i kinetisk energi (mindre sandsynligt):
* Mens det intermolekylære rum påvirker kollisioner og tryk, ændrer det ikke direkte molekylernes kinetiske energi. Den kinetiske energi af en gas bestemmes primært af dens temperatur.
5. Ideel gasadfærd afviger:
* Den ideelle gaslov antager, at gasmolekyler ikke har nogen volumen og ikke interagerer med hinanden.
* Når det intermolekylære rum falder, nedbrydes disse antagelser, og gasens opførsel afviger fra den ideelle gaslov.
Kortfattet: At reducere det intermolekylære rum for en gas øger sit tryk, gør det mere sandsynligt at flyve, øger dens densitet og får dens opførsel til at afvige fra ideel gasopførsel.
 Varme artikler
Varme artikler
-
 Forskere udvikler nanoporøs super-multi-element katalysatorKredit:Japan Science and Technology Agency (JST) En fælles forskergruppe ledet af forskningsassistent Cai ZeXing og professor Takeshi Fujita ved School of Environmental Science and Engineering, Ko
Forskere udvikler nanoporøs super-multi-element katalysatorKredit:Japan Science and Technology Agency (JST) En fælles forskergruppe ledet af forskningsassistent Cai ZeXing og professor Takeshi Fujita ved School of Environmental Science and Engineering, Ko -
 Ny, holdbar katalysator til nøglebrændstofcellereaktion kan vise sig nyttig i miljøvenlige køret…En faktor, der holder den udbredte brug af miljøvenlige brintbrændselsceller tilbage i biler, lastbiler og andre køretøjer er prisen for de platinkatalysatorer, der får cellerne til at fungere. En til
Ny, holdbar katalysator til nøglebrændstofcellereaktion kan vise sig nyttig i miljøvenlige køret…En faktor, der holder den udbredte brug af miljøvenlige brintbrændselsceller tilbage i biler, lastbiler og andre køretøjer er prisen for de platinkatalysatorer, der får cellerne til at fungere. En til -
 Forskere smider nye beregningsværktøjer til at lave mere præcise forudsigelser af proteinstruktur…Forskere fra Rice University blev inspireret af smedens gamle arbejde, da de forfinede deres beregningsmodeller for, hvordan proteiner foldes. Modellerne er beregnet til at hjælpe strukturbiologer, de
Forskere smider nye beregningsværktøjer til at lave mere præcise forudsigelser af proteinstruktur…Forskere fra Rice University blev inspireret af smedens gamle arbejde, da de forfinede deres beregningsmodeller for, hvordan proteiner foldes. Modellerne er beregnet til at hjælpe strukturbiologer, de -
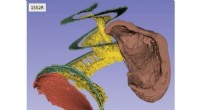 Enestående 3D-billeder af menneskets øres anatomi til genoprettelse af hørelsenBillede af det indre øre. Kredit:Canadian Light Source Ved at bruge avancerede teknikker ved den canadiske lyskilde (CLS) ved University of Saskatchewan, forskere har skabt tredimensionelle billed
Enestående 3D-billeder af menneskets øres anatomi til genoprettelse af hørelsenBillede af det indre øre. Kredit:Canadian Light Source Ved at bruge avancerede teknikker ved den canadiske lyskilde (CLS) ved University of Saskatchewan, forskere har skabt tredimensionelle billed
- Observation af planteplankton via satellit
- Strakt kvantemagnetisme afdækket ved kvantesimulering
- Vand på månen:Forskning afslører dens type og overflod - hvilket øger udforskningsplanerne
- Hvordan fungerer en kuglepen?
- Sådan fungerer gasturbinemotorer
- Seværdighed:turister strømmer til Florida for måneraketopsendelse


