Hvordan påvirker katalysatorer kollisionsteori?
Grundlæggende om kollisionsteori:
* Kollisioner: Kemiske reaktioner sker, når reaktantmolekyler kolliderer med tilstrækkelig energi og korrekt orientering.
* Aktiveringsenergi (EA): Den minimale energi, der kræves for, at en kollision skal være effektiv og resultere i en reaktion.
* reaktionshastighed: Bestemt af hyppigheden af vellykkede kollisioner.
Hvordan katalysatorer fungerer:
1. alternativ reaktionsvej: Katalysatorer giver en alternativ reaktionsvej med en lavere aktiveringsenergi . Dette betyder, at færre molekyler er nødt til at have den minimale energi for at en reaktion kan forekomme.
2. Øget kollisionsfrekvens: Nogle katalysatorer kan øge hyppigheden af effektive kollisioner ved:
* Tilvejebringelse af en overflade til reaktantmolekyler til adsorb: Dette bringer dem tættere sammen, hvilket øger sandsynligheden for kollisioner.
* letter dannelsen af et ustabilt mellemprodukt: Dette mellemprodukt kan reagere lettere med andre molekyler.
3. sænkning af energibarrieren: Katalysatorer kan stabilisere reaktionens overgangstilstand, som er den højenergi-mellemprodukt, der dannes under reaktionen. Dette sænker effektivt den energibarriere, der skal overvindes.
Konsekvenser af sænkning af aktiveringsenergi:
* hurtigere reaktionshastigheder: Da flere kollisioner fører til vellykkede reaktioner, øges reaktionshastigheden markant.
* lavere temperaturer til reaktion: Reaktioner kan forekomme ved lavere temperaturer, fordi aktiveringsenergibarrieren reduceres.
* øget udbytte: Flere molekyler reagerer på et givet tidspunkt, hvilket potentielt fører til et højere udbytte af produkter.
Eksempel:
Forestil dig et bjergpas som aktiveringsenergibarriere. Uden en katalysator er molekyler nødt til at klatre op på bjerget for at reagere. Med en katalysator skabes en tunnel gennem bjerget, hvilket gør det meget lettere for molekyler at passere og reagere.
Vigtig note: Katalysatorer selv forbruges ikke i reaktionen. They simply facilitate the reaction and can be used again and again.
Sidste artikelKan du give 5 forbindelser og deres anvendelser?
Næste artikelHvad er en skelnen mellem alkalimetaller?
 Varme artikler
Varme artikler
-
 Sølvforinger:Tilføjelse af sølv til nanoclusters kan gøre underværker for deres luminescensKrystaller af det sølvdoterede kompleks viste lys rød fotoluminescens under UV-lys, hvorimod krystaller af den udopede struktur ikke udsendte noget lys. Dette pegede på sølvets rolle i at modificere k
Sølvforinger:Tilføjelse af sølv til nanoclusters kan gøre underværker for deres luminescensKrystaller af det sølvdoterede kompleks viste lys rød fotoluminescens under UV-lys, hvorimod krystaller af den udopede struktur ikke udsendte noget lys. Dette pegede på sølvets rolle i at modificere k -
 Malarias hemmelighed for at overleve i det afdækkede blodBilleder, der viser hæmkrystallisering. Det venstre billede viser normal krystallisation, og det højre viser dette i fravær af PV5 -proteinet. Kredit:Francis Crick Institute Ny forskning fra Franc
Malarias hemmelighed for at overleve i det afdækkede blodBilleder, der viser hæmkrystallisering. Det venstre billede viser normal krystallisation, og det højre viser dette i fravær af PV5 -proteinet. Kredit:Francis Crick Institute Ny forskning fra Franc -
 Ny katalysator opgraderer drivhusgas til vedvarende kulbrinterDr. Cao-Thang Dinh, venstre, og Dr. Md Golam Kibria demonstrerer deres nye katalysator. I et papir offentliggjort i dag i Science, deres team demonstrerede den mest effektive og stabile proces til at
Ny katalysator opgraderer drivhusgas til vedvarende kulbrinterDr. Cao-Thang Dinh, venstre, og Dr. Md Golam Kibria demonstrerer deres nye katalysator. I et papir offentliggjort i dag i Science, deres team demonstrerede den mest effektive og stabile proces til at -
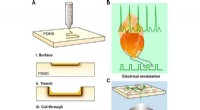 Laserskrivning af nitrogen-doteret siliciumcarbid til biologisk moduleringSkematiske illustrationer af laserskriveprocessen og dens anvendelser. (A) CO2-laser skriver et mønster på et PDMS-substrat, hvor mønsteret kan være (i) på overfladen, (ii) en skyttegrav, eller (iii)
Laserskrivning af nitrogen-doteret siliciumcarbid til biologisk moduleringSkematiske illustrationer af laserskriveprocessen og dens anvendelser. (A) CO2-laser skriver et mønster på et PDMS-substrat, hvor mønsteret kan være (i) på overfladen, (ii) en skyttegrav, eller (iii)
- Hvad er forskellen mellem tværgående bølge og langsgående bølge?
- Hvad hedder gigantiske tidevandsbølger?
- Forstærkning af strålingen fra molekyler efter excitation for at forbedre molekylær laserspektros…
- Kan ferie mad hjælpe med at redde planeten?
- Forskere vinder World Food Prize for arbejdet med Global Seed Vault
- Røntgenlasersyn afslører lægemiddelmål


