Når det tryk, der udøves på en begrænset gas ved konstant temperatur, er fordoblet volumen af IS?
Dette er direkte relateret til Boyle's Law , der siger:
* For en fast mængde af en ideel gas, der holdes ved en konstant temperatur, er tryk og volumen omvendt proportional.
Matematisk er dette repræsenteret som:
* p₁v₁ =p₂v₂
Hvor:
* P₁ =oprindeligt tryk
* V₁ =indledende bind
* P₂ =endelig pres
* V₂ =slutvolumen
Hvis du fordobler trykket (p₂ =2p₁), skal volumenet halveres (v₂ =v₁/2) for at holde ligningen afbalanceret.
Sidste artikelHvad er de uafhængige variabler i et lavakupeksperiment?
Næste artikelHvad var den første del af Atom, der blev opdaget?
 Varme artikler
Varme artikler
-
 Mantis rejer perfekt skjoldEn mantis-reje krøller et skjoldlignende segment på halen, kaldet en telson, for at beskytte sig selv mod slag fra en rivaliserende mantis-rejes kraftfulde dactylklub. Kredit:Roy Caldwell/UC Berkeley
Mantis rejer perfekt skjoldEn mantis-reje krøller et skjoldlignende segment på halen, kaldet en telson, for at beskytte sig selv mod slag fra en rivaliserende mantis-rejes kraftfulde dactylklub. Kredit:Roy Caldwell/UC Berkeley -
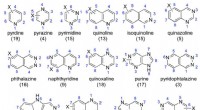 Mod en bedre forståelse af struktur-metabolisme-forhold i human aldehydoxidase (opdatering)Eksempler på de undersøgte azaaromatiske stilladser:antallet af testede forbindelser er angivet i parentes. Kredit:(c) Procedurer fra National Academy of Sciences (2017). DOI:10.1073/pnas.1618881114
Mod en bedre forståelse af struktur-metabolisme-forhold i human aldehydoxidase (opdatering)Eksempler på de undersøgte azaaromatiske stilladser:antallet af testede forbindelser er angivet i parentes. Kredit:(c) Procedurer fra National Academy of Sciences (2017). DOI:10.1073/pnas.1618881114 -
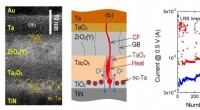 En optimeret struktur af memristiv enhed til neuromorfe computersystemerHøjopløselig transmissionselektronmikroskopibillede (a) og skematisk (b) af tværsnittet af flerlags memristive strukturen i området for den ledende filament (CF), afhængigheden af resistive tilstand
En optimeret struktur af memristiv enhed til neuromorfe computersystemerHøjopløselig transmissionselektronmikroskopibillede (a) og skematisk (b) af tværsnittet af flerlags memristive strukturen i området for den ledende filament (CF), afhængigheden af resistive tilstand -
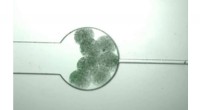 Celler konstruerer levende kompositpolymerer til biomedicinske anvendelserSwarmbots, levende celler konstrueret til at producere monomermolekyler, vokse, indtil de fornemmer, at deres befolkningstæthed har nået et vist niveau, hvorpå de sprængte op, tillader monomerer at bl
Celler konstruerer levende kompositpolymerer til biomedicinske anvendelserSwarmbots, levende celler konstrueret til at producere monomermolekyler, vokse, indtil de fornemmer, at deres befolkningstæthed har nået et vist niveau, hvorpå de sprængte op, tillader monomerer at bl
- Støvsugerproducenten Dyson planlægger udvidelse til den britiske elbilside
- Hvorfor coronavirus-pandemien er særlig farlig for immigranter
- Video:Hvad er ESA's Moonlight-initiativ?
- EU-forbrug resulterer i høje kulstofemissioner fra tropisk skovrydning, nye undersøgelser viser
- Ny metode til at bestemme, hvor sikre bygninger er efter et jordskælv
- Hvordan klarer Amazonas regnskov tørke?


