Hvad er den molære absorption af kobber-II-sulfatpentahydrat, hvis absorbans 0,17 ved 650nm?
* molarorptivitet er en konstant: Det er en specifik egenskab af et stof ved en bestemt bølgelængde. Den beskriver, hvor stærkt et stof absorberer lys ved den bølgelængde.
* Beer-Lambert Law: For at beregne moltabsorptivitet har du brug for øl-Lambert-lovligningen:
`` `
A =εbc
`` `
Hvor:
* A =absorbans (du leverede dette som 0,17)
* ε =molær absorptivitet (hvad du vil finde)
* B =sti -længden af lysstrålen gennem opløsningen (i CM) - du har ikke leveret dette.
* c =koncentration af opløsningen (i mol/l) - du har ikke leveret dette.
hvad du har brug for at vide:
1. sti -længde (b): Længden af cuvette eller container, der holder din løsning. Dette er typisk 1 cm.
2. koncentration (c): Koncentrationen af kobber (II) sulfatpentahydratopløsning. Dette er afgørende for beregningen.
Eksempel:
Lad os antage, at sti -længden er 1 cm, og koncentrationen af dit kobber (II) sulfatpentahydratopløsning er 0,05 mol/l.
Derefter kan du beregne molabsorptivitet ved hjælp af øl-Lambert-loven:
`` `
0,17 =ε * 1 cm * 0,05 mol/l
ε =0,17 / (1 cm * 0,05 mol / l)
ε =3,4 l/(mol*cm)
`` `
Vigtig note:
* Kobber (II) sulfatpentahydrat i sig selv er ikke en stærk kromofor (et molekyle, der absorberer lys kraftigt). Dens absorbans ved 650 nm kan skyldes urenheder eller andre faktorer.
* For nøjagtigt at bestemme den molære absorptivitet har du brug for en opløsning af kendt koncentration og måle absorbansen ved 650 nm ved hjælp af et spektrofotometer.
 Varme artikler
Varme artikler
-
 Forsker gør beskidt stanniol til biobrændstofkatalysatorAhmed Osman. Kredit:Queens University Belfast En forsker ved Queens University Belfast har opdaget en måde at omdanne snavset aluminiumsfolie til en biobrændstofkatalysator, som kunne være med til
Forsker gør beskidt stanniol til biobrændstofkatalysatorAhmed Osman. Kredit:Queens University Belfast En forsker ved Queens University Belfast har opdaget en måde at omdanne snavset aluminiumsfolie til en biobrændstofkatalysator, som kunne være med til -
 Oleo Sponge succesfuld under virkelige forhold ud for Californiens kystEt team af Argonne-forskere testede med succes Oleo-svampen ud for det sydlige Californiens kyst i april. Fra venstre mod højre:Argonnes Seth Darling, Jeff Elam og Ed Barry. Kredit:Argonne National La
Oleo Sponge succesfuld under virkelige forhold ud for Californiens kystEt team af Argonne-forskere testede med succes Oleo-svampen ud for det sydlige Californiens kyst i april. Fra venstre mod højre:Argonnes Seth Darling, Jeff Elam og Ed Barry. Kredit:Argonne National La -
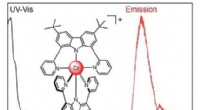 Et nyt kromkompleks udsender lys i uhåndgribelig NIR-II-bølgelængdeKredit:Wiley Mange applikationer, fra fiberoptisk telekommunikation til biomedicinske billeddannelsesprocesser kræver stoffer, der udsender lys i det nær-infrarøde område (NIR). Et forskerhold i S
Et nyt kromkompleks udsender lys i uhåndgribelig NIR-II-bølgelængdeKredit:Wiley Mange applikationer, fra fiberoptisk telekommunikation til biomedicinske billeddannelsesprocesser kræver stoffer, der udsender lys i det nær-infrarøde område (NIR). Et forskerhold i S -
 Ny teknik omdanner problemfrit ammoniak til grøn brintKredit:CC0 Public Domain Northwestern University forskere har udviklet en yderst effektiv, miljøvenlig metode til at omdanne ammoniak til brint. Skitseret i en nylig publikation i tidsskriftet Jo
Ny teknik omdanner problemfrit ammoniak til grøn brintKredit:CC0 Public Domain Northwestern University forskere har udviklet en yderst effektiv, miljøvenlig metode til at omdanne ammoniak til brint. Skitseret i en nylig publikation i tidsskriftet Jo
- Forskere opdager, hvor flydende en væske kan være
- Ikke længere vand under broen, statistik giver nye data om havniveauer
- Georgia rumhavn landhandel er slået fra, siger webstedsejer
- Oversvømmelsesrisiko for nye boliger i England og Wales vil stige i ugunstigt stillede områder
- Rejsegiganten Expedia siger, at det vil reducere 3, 000 job
- US Navy øjne grafen nanobånd for ultimativt magt kontrolsystem


