Hvad er mekanismen til dannelse af phthalisk anhydrid?
Mekanisme til dannelse af phthalisk anhydrid
Phthalisk anhydrid produceres industrielt gennem katalytisk oxidation af ortho-xylen Brug af vanadium pentoxid (V2O5) som katalysator. Her er en sammenbrud af mekanismen:
Trin 1:Oxidation af ortho-xylen til phthalinsyre
* Ortho-xylen (C8H10) reagerer med ilt (O2) i nærvær af V2O5 ved høje temperaturer (ca. 350-400 ° C) og tryk (ca. 1-2 atm).
* Katalysatoren V2O5 hjælper med at aktivere iltmolekylet og lette oxidationsprocessen.
* To methylgrupper (-CH3) på ortho-xylenmolekylet oxideres til carboxylsyregrupper (-COOH), der danner phthalsyre (C8H6O4).
Trin 2:Dehydrering af phthalinsyre til phthalisk anhydrid
* Den phthalinsyre, der er dannet i trin 1, dehydreres derefter ved opvarmning af den yderligere (ca. 200-300 ° C).
* Denne proces fjerner et molekyle vand (H2O) fra phthalinsyre, hvilket fører til dannelse af phthalisk anhydrid (C8H4O3).
samlet reaktion:
C8H10 + 3O2 → C8H4O3 + 2H2O
Bemærk:
* Reaktionen er meget eksoterm og producerer en betydelig mængde varme.
* Tilstedeværelsen af en katalysator er afgørende for, at reaktionen forekommer med en rimelig hastighed.
* Reaktionen udføres typisk i en kontinuerlig proces med en fast katalysator.
* Det phthaliske anhydrid oprenses derefter ved destillation.
Alternative metoder:
Mens den katalytiske oxidation af ortho-xylen er den mest almindelige industrielle metode, findes der andre metoder til fremstilling af phthalisk anhydrid. Disse inkluderer:
* Oxidation af naphthalen :Denne metode involverer oxidation af naphthalen ved anvendelse af luft i nærvær af en vanadiumkatalysator.
* diels-alder-reaktion :Denne metode involverer reaktionen af maleisk anhydrid med cyclopentadien.
Oxidation af ortho-xylen foretrækkes imidlertid generelt på grund af dets høje udbytte og relativt lave omkostninger til råvarer.
Sidste artikelHvorfor er fuldstændigt fyldte orbitaler mere stabile?
Næste artikelHvilken metalforbindelse er grøn og uopløselig?
 Varme artikler
Varme artikler
-
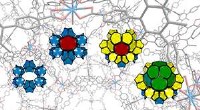 To simple byggeklodser producerer komplekst 3D-materialeSelvmontering af et metal-organisk stel. Kredit:Northwestern University Forskere fra Northwestern University har bygget et strukturelt komplekst materiale fra to simple byggesten, der er den metal
To simple byggeklodser producerer komplekst 3D-materialeSelvmontering af et metal-organisk stel. Kredit:Northwestern University Forskere fra Northwestern University har bygget et strukturelt komplekst materiale fra to simple byggesten, der er den metal -
 Bananplanteekstrakt kan være nøglen til mere cremet, længerevarende isSmå fibre ekstraheret fra bananplante rachis (cirklet) kunne hjælpe med at bremse issmeltningen. Kredit:Robin Zuluaga Gallego Ingen tvivl om det, is er en god fornøjelse på en varm dag. Det er, in
Bananplanteekstrakt kan være nøglen til mere cremet, længerevarende isSmå fibre ekstraheret fra bananplante rachis (cirklet) kunne hjælpe med at bremse issmeltningen. Kredit:Robin Zuluaga Gallego Ingen tvivl om det, is er en god fornøjelse på en varm dag. Det er, in -
 Video:Hvor effektive er stofmasker mod coronavirus?Kredit:The American Chemical Society U.S. Centers for Disease Control anbefaler, at den brede offentlighed bærer ansigtsmasker i stof for at hjælpe med at mindske alles chancer for at få COVID-19.
Video:Hvor effektive er stofmasker mod coronavirus?Kredit:The American Chemical Society U.S. Centers for Disease Control anbefaler, at den brede offentlighed bærer ansigtsmasker i stof for at hjælpe med at mindske alles chancer for at få COVID-19. -
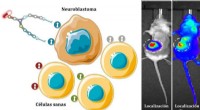 Syntetiske molekyler leverer lægemidler direkte til neuroblastomcellerKredit:Angewandte Chemie-International Edition 58 (2019) Forskere fra Universidad Politécnica de Madrid er involveret i udviklingen af specifikke molekylære stilladser, som er i stand til at lev
Syntetiske molekyler leverer lægemidler direkte til neuroblastomcellerKredit:Angewandte Chemie-International Edition 58 (2019) Forskere fra Universidad Politécnica de Madrid er involveret i udviklingen af specifikke molekylære stilladser, som er i stand til at lev
- Hvad er kakaopulver lavet af?
- Udvinding af data - den seneste femårige PA DEP-rapport om virkninger og afhjælpning af underjordi…
- Verden har brug for 8,1 billioner dollars investeringer i naturen inden 2050 for at tackle den tredo…
- Ny undersøgelse afslører, hvordan 'frie radikaler' driver celledeling og afslører en potentiel ny…
- For at grønne byer bliver mainstream, vi skal lære af lokale succeshistorier og skalere op
- Hvad er atomer, der let mister elektroner?


