Hvorfor er fuldstændigt fyldte orbitaler mere stabile?
1. Hunds regel og elektronelektronafvisning:
* Hunds regel Stater, at elektroner individuelt vil besætte orbitaler inden for et underskal, før de parrer sig sammen i den samme orbital. Dette skyldes, at elektroner i forskellige orbitaler oplever mindre frastødelse fra hinanden.
* Når en orbital er fuldstændigt fyldt, er alle elektroner parret, hvilket minimerer elektronelektronafvisning. Dette minimerer systemets energi, hvilket gør den mere stabil.
2. Exchange Energy:
* Når elektroner har den samme spin i forskellige orbitaler inden for et underskal, kan de udveksle positioner. Denne udveksling bidrager til en stabiliserende effekt kaldet udvekslingsenergi .
* I en helt fyldt orbital er alle elektroner parret, hvilket maksimerer udvekslingsenergien, hvilket yderligere bidrager til stabilitet.
3. Symmetri og degeneration:
* Helt fyldte orbitaler har en højere grad af symmetri. Denne symmetri fører til en højere degeneration af orbitaler, hvilket betyder, at de har det samme energiniveau.
* Denne degeneration kombineret med den minimerede elektronelektroniske frastødning bidrager til systemets stabilitet.
4. Afskærmning:
* Elektroner i fyldte orbitaler beskytter effektivt kernen mod de ydre elektroner. Dette betyder, at de ydre elektroner oplever en svagere attraktion fra kernen, hvilket gør dem mindre tilbøjelige til at blive fjernet.
5. Lavere energi:
* Den samlede effekt af disse faktorer er, at fuldstændigt fyldte orbitaler har lavere energi end delvist fyldte orbitaler. Denne lavere energistat svarer til en mere stabil konfiguration.
Kortfattet:
Kombinationen af minimeret elektronelektronafvisning, maksimeret udvekslingsenergi, øget symmetri og degeneration og effektiv afskærmning bidrager alle til den forbedrede stabilitet af fuldstændigt fyldte orbitaler.
Sidste artikelHvordan lægger de gassen inde i en sodavand?
Næste artikelHvad er mekanismen til dannelse af phthalisk anhydrid?
 Varme artikler
Varme artikler
-
 Udvikling af bæredygtige membraner til fremtidig energiDr. Suzana Nunes (til venstre), KAUST-professor i kemi- og miljøvidenskab og teknik, og Dr. Stefan Chisca (til højre), KAUST-forsker, undersøger en beholder med polymeren, der bruges til at fremstille
Udvikling af bæredygtige membraner til fremtidig energiDr. Suzana Nunes (til venstre), KAUST-professor i kemi- og miljøvidenskab og teknik, og Dr. Stefan Chisca (til højre), KAUST-forsker, undersøger en beholder med polymeren, der bruges til at fremstille -
 Nye molekyler afledt af cannabidiol er designet med mere potente antioxidanterImmunologi professor Eduardo Muñoz. Kredit:University of Córdoba I dag, cannabidiol er en stjernekomponent, ikke kun i kosmetikkens verden, men også inden for medicin og ernæring på grund af dets
Nye molekyler afledt af cannabidiol er designet med mere potente antioxidanterImmunologi professor Eduardo Muñoz. Kredit:University of Córdoba I dag, cannabidiol er en stjernekomponent, ikke kun i kosmetikkens verden, men også inden for medicin og ernæring på grund af dets -
 En grønnere måde at tage bitterheden ud af olivenKredit:American Chemical Society Oliven er en del af middelhavskosten, som har været forbundet med en reduceret forekomst af hjerte-kar-sygdomme, Alzheimers sygdom og andre tilstande. Imidlertid,
En grønnere måde at tage bitterheden ud af olivenKredit:American Chemical Society Oliven er en del af middelhavskosten, som har været forbundet med en reduceret forekomst af hjerte-kar-sygdomme, Alzheimers sygdom og andre tilstande. Imidlertid, -
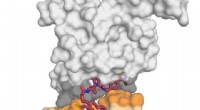 Et dødskys for at bedøve de undrugbareBilledet viser E3 -ligaseproteinet VHL (i gråt) i kompleks med det lille molekyle MZ1 (i hindbær) og kysser proteinet BRD4 (i gult). Efter at have modtaget dette dødelige kys, BRD4 er målrettet mod ne
Et dødskys for at bedøve de undrugbareBilledet viser E3 -ligaseproteinet VHL (i gråt) i kompleks med det lille molekyle MZ1 (i hindbær) og kysser proteinet BRD4 (i gult). Efter at have modtaget dette dødelige kys, BRD4 er målrettet mod ne
- Hvad er oxidationstallet for nitrogen i salpetersyre?
- Matematik kaster lys over, hvad forsinkelser i at blive gravid betyder for udsigterne til at få en …
- Kroppen har et meget effektivt indre forsvar, som kan fjerne enhver mængde af et uønsket stof?
- Hvorfor ikke at vide, hvad de skal gøre, er ikke altid en dårlig ting for ledere
- På trods af god fremgang, 100% lavemissionsenergi er stadig langt væk for Storbritannien
- Familier med universitetsbørn er mere tilbøjelige til at miste deres hjem under lavkonjunkturer


