Hvad er lighederne i hydrofillisk og hydrofob?
Her er sammenbruddet:
* Hydrofil: Disse molekyler elsker vand (Fra de græske ord "hydro" betyder vand og "filos", der betyder kærlig). De opløses let i vand og danner hydrogenbindinger med vandmolekyler. Dette skyldes, at de normalt er polære, hvilket betyder, at de har ujævnt fordelt afgifter, hvilket giver dem mulighed for at interagere med de polære vandmolekyler. Eksempler inkluderer sukker, salt og alkohol.
* Hydrofob: Disse molekyler frygter vand (Fra de græske ord "hydro" betyder vand og "fobos", der betyder frygt). De blander sig ikke godt med vand og har en tendens til at klumpe sammen i dens nærvær. Dette skyldes, at de normalt er ikke-polære, hvilket betyder, at de har jævnt distribueret afgifter, hvilket gør det vanskeligt for dem at danne bindinger med de polære vandmolekyler. Eksempler inkluderer olie, fedt og fedt.
Den vigtigste lighed er, at begge typer molekyler demonstrerer, hvordan vand interagerer med andre stoffer. De er to sider af den samme mønt, der definerer, hvordan forskellige forbindelser opfører sig i et vandigt miljø.
 Varme artikler
Varme artikler
-
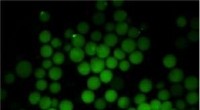 Små geler opsuger intestinale toksinerMikrogeler er vist ovenfor med sukkermotiver efter binding fluorescensmærkede lektiner. Kredit:Alexander Kuehne Bakterielle infektioner, der er målrettet mod tarmen, kan forårsage tilstande, der s
Små geler opsuger intestinale toksinerMikrogeler er vist ovenfor med sukkermotiver efter binding fluorescensmærkede lektiner. Kredit:Alexander Kuehne Bakterielle infektioner, der er målrettet mod tarmen, kan forårsage tilstande, der s -
 Brug af matematik til at forudsige SARS-CoV-2-proteinmutationerEt team af forskere brugte matematik til at forudsige, hvilke områder af SARS-CoV-2 spike-proteinet der er mest tilbøjelige til at mutere. Kredit:Jill Hemman/ORNL, U.S.A. Dept. of Energy Oak Ridge
Brug af matematik til at forudsige SARS-CoV-2-proteinmutationerEt team af forskere brugte matematik til at forudsige, hvilke områder af SARS-CoV-2 spike-proteinet der er mest tilbøjelige til at mutere. Kredit:Jill Hemman/ORNL, U.S.A. Dept. of Energy Oak Ridge -
 Discovery åbner nye veje til at designe lægemidler til at bekæmpe lægemiddelresistent malariaKredit:CC0 Public Domain For første gang, UBC-forskere har vist en nøgleforskel i de tredimensionelle strukturer af et centralt metabolisk enzym i parasitten, der forårsager malaria sammenlignet m
Discovery åbner nye veje til at designe lægemidler til at bekæmpe lægemiddelresistent malariaKredit:CC0 Public Domain For første gang, UBC-forskere har vist en nøgleforskel i de tredimensionelle strukturer af et centralt metabolisk enzym i parasitten, der forårsager malaria sammenlignet m -
 Verifikation af whisky ved hjælp af laserlysKredit:CC0 Public Domain Forskere fra University of St Andrews har udviklet en innovativ ny teknik ved hjælp af lasere til nøjagtigt at måle ægtheden af nogle af verdens mest eksklusive whiskyer
Verifikation af whisky ved hjælp af laserlysKredit:CC0 Public Domain Forskere fra University of St Andrews har udviklet en innovativ ny teknik ved hjælp af lasere til nøjagtigt at måle ægtheden af nogle af verdens mest eksklusive whiskyer
- Ammoniakblanding med ilt og ammoniak Ozon?
- 250, 000 tons forsendelses CO2-emissioner sparet takket være maskinlæringsindsigt
- Er molekyler højre- eller venstrehåndede? Egenskaber for chiral på attosecond niveau
- Sådan fungerer håndtering af bagage
- Hvor meget argon er der i luften?
- Mælkeprotein kan hjælpe med at øge blåbærs sundhed


