Hvad er den generelle formel for en aromatisk?
Hückels regel: Dette er den vigtigste regel for bestemmelse af aromatik. Det siger, at en forbindelse er aromatisk, hvis den har:
* en cyklisk struktur: Molekylet skal danne en lukket ring.
* plane geometri: Alle atomer i ringen skal ligge i det samme plan.
* et konjugeret system: Ringen skal have skiftende enkelt- og dobbeltbindinger (eller ensomme par), der muliggør delokalisering af elektroner.
* (4n + 2) π Elektroner: Dette er den vigtigste del af Hückels styre. Molekylet skal have et specifikt antal π -elektroner (elektroner i P -orbitaler, der bidrager til det delokaliserede system). Dette nummer skal være lig med 4n + 2, hvor n er ethvert heltal (0, 1, 2, 3 osv.).
Eksempler på aromatiske forbindelser:
* benzen (C6H6): Har 6 π elektroner (4n + 2 =6 når n =1)
* pyridin (C5H5N): Har 6 π -elektroner, med nitrogenet, der bidrager med et elektron til systemet.
* furan (C4H4O): Har 6 π -elektroner, med det ilt, der bidrager med to elektroner til systemet.
Bemærk:
* Ikke alle cykliske forbindelser med skiftende dobbeltbindinger er aromatiske. For eksempel er cyclooctatetraene (C8H8) ikke aromatisk, fordi det ikke er plan.
* Nogle forbindelser kan have flere aromatiske ringe, som naphthalen (C10H8).
Selvom der ikke er en enkelt formel, tillader egenskaberne ved Hückels regel os at bestemme, om en forbindelse er aromatisk eller ej.
 Varme artikler
Varme artikler
-
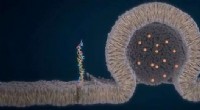 Sådan dannes en kanal mellem to organellerKreditering:Je-Kyung Ryu Kanalen, gennem hvilken to cellekomponenter udveksler materiale, ser ud til at dannes ved kanten af deres kontaktflade, og ikke i midten. Dette blev opdaget af de Leiden
Sådan dannes en kanal mellem to organellerKreditering:Je-Kyung Ryu Kanalen, gennem hvilken to cellekomponenter udveksler materiale, ser ud til at dannes ved kanten af deres kontaktflade, og ikke i midten. Dette blev opdaget af de Leiden -
 Molekylær dynamiksimulering kaster nyt lys over metanhydratdannelseMethanhydrat hentet fra havbunden ud for Oregons kyst, USA. Kredit:Wikimedia Commons I et papir, der blev offentliggjort i denne uge i PNAS , forskere ved University of Amsterdams Van t Hoff Ins
Molekylær dynamiksimulering kaster nyt lys over metanhydratdannelseMethanhydrat hentet fra havbunden ud for Oregons kyst, USA. Kredit:Wikimedia Commons I et papir, der blev offentliggjort i denne uge i PNAS , forskere ved University of Amsterdams Van t Hoff Ins -
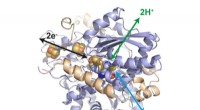 Enzymsystem til brintindustrienStruktur af hydrogenasen fra Desulfovibrio desulfuricans. I sit aktive center, en jern-svovl-klynge katalyserer oxidation af hydrogen til protoner samt reduktion af protoner til hydrogen. Yderligere j
Enzymsystem til brintindustrienStruktur af hydrogenasen fra Desulfovibrio desulfuricans. I sit aktive center, en jern-svovl-klynge katalyserer oxidation af hydrogen til protoner samt reduktion af protoner til hydrogen. Yderligere j -
 For brintkraft, verdslige materialer kan være næsten lige så gode som dyr platinForskere brugte plasma til at skabe nye katalysatorer, der er meget billigere end og næsten lige så effektive som standard, platin-gruppe versioner. Kredit:Princeton University Som alle, der har k
For brintkraft, verdslige materialer kan være næsten lige så gode som dyr platinForskere brugte plasma til at skabe nye katalysatorer, der er meget billigere end og næsten lige så effektive som standard, platin-gruppe versioner. Kredit:Princeton University Som alle, der har k
- Hvilket gruppe 18 -element i jordtilstand har maksimalt to fuldstændigt fyldte energiskaller Kr he …
- Hvad er betydningen af absolut hastighed i feltfysik?
- Ny NASA-mission for at opdage brug af plantevand fra rummet
- Universiteter kan gøre mere for at støtte deres studerende med handicap
- Er det sværere at fremskynde et bevægende objekt?
- Sådan beregnes apotemet til en polygon


