Hvad er volumenet på 19,87 mol ammoniumchlorid (NH4CL) ved STP?
* STP (standardtemperatur og tryk): STP er defineret for gasser, typisk ved 0 ° C (273,15 K) og 1 ATM -tryk.
* ammoniumchlorid: Ammoniumchlorid er et fast stof ved STP. Faststoffer har et fast volumen og form, i modsætning til gasser, der udvides til at fylde deres beholder.
hvad du kan beregne:
* molmasse af NH4CL: Du kan beregne den molære masse af ammoniumchlorid, som er ca. 53,49 g/mol.
* masse af 19,87 mol NH4CL: Du kan finde massen på 19,87 mol NH4Cl ved at multiplicere molen med den molære masse:19,87 mol * 53,49 g/mol =1063,7 g
For at bestemme mængden af solid NH4CL har du brug for dens densitet.
Her er hvorfor densitet er vigtig:
* densitet (ρ): Densitet er masse pr. Enhedsvolumen (ρ =m/v).
* bind: Du kan omarrangere densitetsligningen for at løse for volumen:v =m/ρ
For at beregne volumenet på 19,87 mol NH4CL, skal du kende dens densitet ved Stp.
Sidste artikelHvad er C i kemi?
Næste artikelHvor mange vandmolekyler frigives, når C12H22O11 dannes?
 Varme artikler
Varme artikler
-
 Opdag, hvad der får durian til at stinkeBillede af en durian. Kredit:Martin Steinhaus Forskere ved Leibniz-Institut for Food Systems Biology ved det tekniske universitet i München (Leibniz-LSB@TUM) har bekræftet tilstedeværelsen af de
Opdag, hvad der får durian til at stinkeBillede af en durian. Kredit:Martin Steinhaus Forskere ved Leibniz-Institut for Food Systems Biology ved det tekniske universitet i München (Leibniz-LSB@TUM) har bekræftet tilstedeværelsen af de -
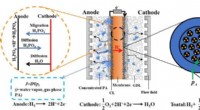 Forudsigelse af fordeling af phosphorsyre og vand i højtemperatur polymerelektrolytmembranbrændsel…Skematisk af katodekatalysatorlaget baseret på agglomerat-antagelsen. Kredit:Sun Mu Højtemperatur polymer elektrolytmembran brændselscelle (HT-PEMFC) kan anvendes i elektriske køretøjer og marine s
Forudsigelse af fordeling af phosphorsyre og vand i højtemperatur polymerelektrolytmembranbrændsel…Skematisk af katodekatalysatorlaget baseret på agglomerat-antagelsen. Kredit:Sun Mu Højtemperatur polymer elektrolytmembran brændselscelle (HT-PEMFC) kan anvendes i elektriske køretøjer og marine s -
 Banebrydende rødt lys-aktiveret anti-tumor prodrug reducerer bivirkningerPhorbiplatins kontrollerbare aktiveringsegenskab og overlegne antitumoraktivitet bidrager væsentligt til udviklingen af fotoaktiverbare anticancer-prodrugs, især Pt(IV) prodrugs, der kan aktiveres v
Banebrydende rødt lys-aktiveret anti-tumor prodrug reducerer bivirkningerPhorbiplatins kontrollerbare aktiveringsegenskab og overlegne antitumoraktivitet bidrager væsentligt til udviklingen af fotoaktiverbare anticancer-prodrugs, især Pt(IV) prodrugs, der kan aktiveres v -
 Teknik afslører, hvordan krystaller dannes på overfladerProcessen med hvordan krystaller dannes på en flad overflade, som vist på dette elektronmikroskopbillede, har været svært at studere i detaljer indtil nu. Kredit:Robert Macfarlane Krystallisations
Teknik afslører, hvordan krystaller dannes på overfladerProcessen med hvordan krystaller dannes på en flad overflade, som vist på dette elektronmikroskopbillede, har været svært at studere i detaljer indtil nu. Kredit:Robert Macfarlane Krystallisations
- Molekyleændring kan forbedre oparbejdning af brugt nukleart brændstof
- Hvornår var den første månelanding?
- Hvad skal man have på til en klimakrise
- Hvor er månen i kredsløb, når vi overhovedet ikke kan se den?
- Omdannelse af gas til brændstoffer med bedre legeringer
- Små prisforskelle koster investorer milliarder


