Hvad er den videnskabelige proces, når vand går ned, koger det?
1. Varmeoverførsel:
* Energiindgang: Når du opvarmer vand, tilføjer du energi til dets molekyler. Denne energi overføres fra varmekilden (som en komfur eller ild) til vandmolekylerne gennem ledning eller konvektion.
2. Øget molekylær bevægelse:
* vibrationer: Når vandmolekylerne absorberer energi, begynder de at vibrere og bevæge sig hurtigere.
* mellem molekyler: Den øgede bevægelse får molekylerne til at sprede sig fra hinanden og skabe mere plads mellem dem.
3. Når kogepunktet:
* damptryk: Den øgede bevægelse af vandmolekyler øger også det pres, de udøver på deres omgivelser. Dette kaldes damptryk.
* atmosfærisk tryk: På samme tid udøver luften over vandet et tryk på overfladen. Dette er atmosfærisk pres.
* kogepunkt: Når damptrykket af vandmolekylerne bliver lig med det atmosfæriske tryk, begynder vandet at koge. Kogepunktet for vand er 100 ° C (212 ° F) ved standard atmosfæretryk.
4. Faseændring:
* væske til gas: På kogepunktet har vandmolekylerne nok energi til at overvinde de attraktive kræfter, der holder dem sammen i flydende tilstand. De slipper fri fra overfladen og slipper ud i luften som vanddamp (gas).
* bobler: Denne flugt er det, vi ser som bobler, der dannes i kogende vand. Boblerne er fyldt med vanddamp.
5. Fortsat opvarmning:
* Fordampning: Selv efter at have nået kogepunktet, fortsætter vandet med at absorbere varme og fordampe. Denne proces fortsætter, indtil alt det flydende vand er omdannet til damp.
Nøglepunkter:
* Vandets kogepunkt kan ændres afhængigt af det atmosfæriske tryk. I højere højder, hvor det atmosfæriske tryk er lavere, koges vandet ved en lavere temperatur.
* Kogning er en fysisk ændring, ikke en kemisk ændring. Vandmolekylerne er stadig H₂O, men deres tilstand er ændret fra væske til gas.
Fortæl mig, hvis du har andre spørgsmål!
 Varme artikler
Varme artikler
-
 Video:Nobelprisen i kemi 2017:Cryo-elektronmikroskopi forklaretKredit:The American Chemical Society Jacques Dubochet, Joachim Frank og Richard Henderson har krævet årets Nobelpris i kemi. Trioen tjente prisen for deres arbejde med kryo-elektronmikroskopi, so
Video:Nobelprisen i kemi 2017:Cryo-elektronmikroskopi forklaretKredit:The American Chemical Society Jacques Dubochet, Joachim Frank og Richard Henderson har krævet årets Nobelpris i kemi. Trioen tjente prisen for deres arbejde med kryo-elektronmikroskopi, so -
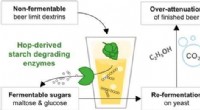 Humlet øl uden eksploderende flasker og for meget alkoholKredit:American Chemical Society Den glemte kunst at tør-hoppe øl for at forbedre smagen er tilbage på mode. Men denne praksis har undertiden uønskede bivirkninger, såsom et uventet højt alkoholin
Humlet øl uden eksploderende flasker og for meget alkoholKredit:American Chemical Society Den glemte kunst at tør-hoppe øl for at forbedre smagen er tilbage på mode. Men denne praksis har undertiden uønskede bivirkninger, såsom et uventet højt alkoholin -
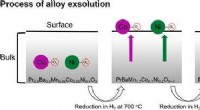 Højtydende selvsamlet katalysator til SOFCProcessen med legeringsopløsning. Kredit:UNIST En nylig undersøgelse tilknyttet UNIST har introduceret en ny katalysator, der markant kan forbedre ydeevnen af perovskitelektroder i Solid Oxide F
Højtydende selvsamlet katalysator til SOFCProcessen med legeringsopløsning. Kredit:UNIST En nylig undersøgelse tilknyttet UNIST har introduceret en ny katalysator, der markant kan forbedre ydeevnen af perovskitelektroder i Solid Oxide F -
 Ny måleteknik kan spare pulpfabrikker millionerKredit:CC0 Public Domain Ny forskning ved Karlstad Universitet viser, at pulpfabrikker kan spare millioner ved at bruge en ny måleteknik. Denne nye teknik muliggør kontrol af pulpningsprocessen, h
Ny måleteknik kan spare pulpfabrikker millionerKredit:CC0 Public Domain Ny forskning ved Karlstad Universitet viser, at pulpfabrikker kan spare millioner ved at bruge en ny måleteknik. Denne nye teknik muliggør kontrol af pulpningsprocessen, h
- Børnesport altid aflyst på grund af regnvåde grunde? Grøn infrastruktur kan hjælpe
- 10 komplette falskheder om mad
- Hvad er den tilstand, hvor krop reagerer på fødevarer eller stoffer?
- Hvorfor ser folk på den nordlige halvkugle alle konstellationer gennem året?
- Et par eksempler på væske-væske opløsninger tak?
- Undersøgelse:Passive investorer letter aktivisters evne til at være aggressiv


