Hvorfor eksisterer molekyler uafhængigt, men hvorfor ikke atom?
* atomer er de grundlæggende byggesten til stof. De er den mindste enhed i et element, der bevarer de kemiske egenskaber ved dette element. Mens atomer kan eksistere isoleret (som ædelgasser), findes de normalt bundet sammen i molekyler eller større strukturer.
* molekyler dannes, når to eller flere atomer binder sammen. Disse bindinger kan være ioniske (overførsel af elektroner) eller kovalente (deling af elektroner). Denne binding giver molekyler unikke egenskaber, der adskiller sig fra de individuelle atomer, der udgør dem.
Hvorfor tænker vi på molekyler som eksisterende uafhængigt?
* stabilitet: Molekyler er ofte mere stabile end isolerede atomer. Bindingerne mellem atomer sænker deres samlede energi, hvilket gør dem mindre reaktive.
* observerbare egenskaber: Molekyler har forskellige egenskaber som smeltepunkt, kogepunkt, farve og reaktivitet. Vi kan let observere og studere disse egenskaber, hvilket giver os en fornemmelse af deres uafhængige eksistens.
* Kemiske reaktioner: Kemiske reaktioner involverer brud og dannelse af bindinger mellem atomer, hvilket i sidste ende resulterer i dannelsen af nye molekyler.
Hvorfor findes ikke atomer altid uafhængigt?
* reaktivitet: De fleste atomer er meget reaktive, hvilket betyder, at de let interagerer med andre atomer for at danne mere stabile forbindelser.
* octet regel: Mange atomer stræber efter at opnå en stabil elektronkonfiguration (som ædelgasser) ved at vinde, miste eller dele elektroner. Dette involverer ofte binding med andre atomer.
* attraktionskræfter: Atomer tiltrækkes af hinanden af forskellige kræfter, herunder elektrostatisk og van der Waals -styrker. Disse kræfter fører ofte til dannelse af molekyler eller større strukturer.
I det væsentlige findes både atomer og molekyler i forskellige tilstande afhængigt af deres miljø og reaktivitet. Mens individuelle atomer kan eksistere, er de ofte mere stabile og findes ofte i form af molekyler eller større strukturer.
Sidste artikelHvilken type syre findes i smoothies?
Næste artikelHvordan påvirker katalysatorer energien fra en reaktion?
 Varme artikler
Varme artikler
-
 Forskere observerer direkte membranbindingen af α-synuclein i levende cellerForskere fra University of Konstanz og Free University of Amsterdam, i samarbejde med Bruker BioSpin udviklingsteamet, har for første gang haft held med den direkte spektroskopiske påvisning af bindin
Forskere observerer direkte membranbindingen af α-synuclein i levende cellerForskere fra University of Konstanz og Free University of Amsterdam, i samarbejde med Bruker BioSpin udviklingsteamet, har for første gang haft held med den direkte spektroskopiske påvisning af bindin -
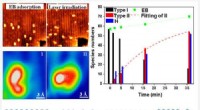 Forskere opdager CH-bindingsaktiveringsreaktioner ved lav temperatur ved foto-inducerede midlerHøjopløselig STM, der visualiserer reaktionens mellemtilstande og reaktionsvejen for EB-dehydrogenering på TiO2. Kredit:WANG Haochen CH-bindingen er meget vigtig i organisk kemi. Kemiske reaktione
Forskere opdager CH-bindingsaktiveringsreaktioner ved lav temperatur ved foto-inducerede midlerHøjopløselig STM, der visualiserer reaktionens mellemtilstande og reaktionsvejen for EB-dehydrogenering på TiO2. Kredit:WANG Haochen CH-bindingen er meget vigtig i organisk kemi. Kemiske reaktione -
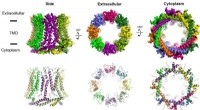 Nyt kig på mærkelige huller involveret i smag, Alzheimers, astmaVed hjælp af kryo-elektronmikroskopi, Furukawas laboratorium kompilerede et 3D-billede, der beskriver det nøjagtige arrangement af proteinerne, der former hver CALHM-pore. På billedet:CALHM1 set fra s
Nyt kig på mærkelige huller involveret i smag, Alzheimers, astmaVed hjælp af kryo-elektronmikroskopi, Furukawas laboratorium kompilerede et 3D-billede, der beskriver det nøjagtige arrangement af proteinerne, der former hver CALHM-pore. På billedet:CALHM1 set fra s -
 Video:Den utilsigtede opdagelse af LSDKredit:The American Chemical Society Cykeldagen den 19. april hylder ikke den tohjulede transportform, men den farverige tur taget af den schweiziske kemiker Albert Hoffman, der ved et uheld opdag
Video:Den utilsigtede opdagelse af LSDKredit:The American Chemical Society Cykeldagen den 19. april hylder ikke den tohjulede transportform, men den farverige tur taget af den schweiziske kemiker Albert Hoffman, der ved et uheld opdag
- Hvordan stråler solen energi?
- Alder og køn? Hollandsk udvikle analysator til Twitter
- Månesten fundet af astronauter stammer sandsynligvis fra Jorden
- Hvilke organismer har fire kammerede hjerter?
- Hvad hvis ren luft-fordele under COVID-19-nedlukningen fortsatte efter pandemien?
- Kan kun sol- og kemiske ændringer producere lys?


